Clear Sky Science · ar
الرنا الطويل المرتبط الشيخوخة TRMP وTRMP-S يعززان سرطان المعدة عبر تفعيل IGFL4
لماذا هذا البحث مهم
لا يزال سرطان المعدة من أكثر أنواع السرطان فتكا في العالم، ويرجع ذلك إلى حد كبير إلى أنه غالبًا ما يُكتشف في مراحل متأخرة ويصعب علاجه. يكشف هذا البحث كيف أن جزيئين وراثيين غير معروفين إلى حد كبير، يُدعيان TRMP وTRMP-S، يساعدان الأورام المعدية على النمو والانتشار. من خلال توضيح سلسلة الأحداث التي يطلقانها داخل خلايا السرطان وفي البيئة المناعية المحيطة بالورم، يشير العمل إلى طرق جديدة قد تساعد الأطباء مستقبلًا على تشخيص المرضى مبكرًا وتصميم علاجات موجهة وأكثر فعالية.
رسائل مخفية في حمضنا النووي
يظن معظم الناس أن الجينات عبارة عن مخططات لصنع البروتينات، لكن حمضنا النووي ينتج أيضًا رناَّت طويلة غير مشفرة (lncRNAs) لا تُنتج بروتينات ومع ذلك تؤثر بقوة على سلوك الخلايا. يُعد TRMP ونظيره المختصر الناتج عن القص TRMP-S اثنين من هذه الرناّيات الطويلة. ارتبطا سابقًا بالشيخوخة والتحكم بدورة الخلية في خلايا الرئة والقولون، لكن دورهما في سرطان المعدة كان غير معروف. وبما أن الرناّيات الطويلة يمكن أن تعمل كعلامات للتشخيص وكمستهدفات للعلاج، سعى الباحثون لاكتشاف ما إذا كان TRMP وTRMP-S يدفعان خلايا المعدة نحو السرطان وكيفية تفاعلهما مع جزيئات أخرى لتحقيق ذلك.
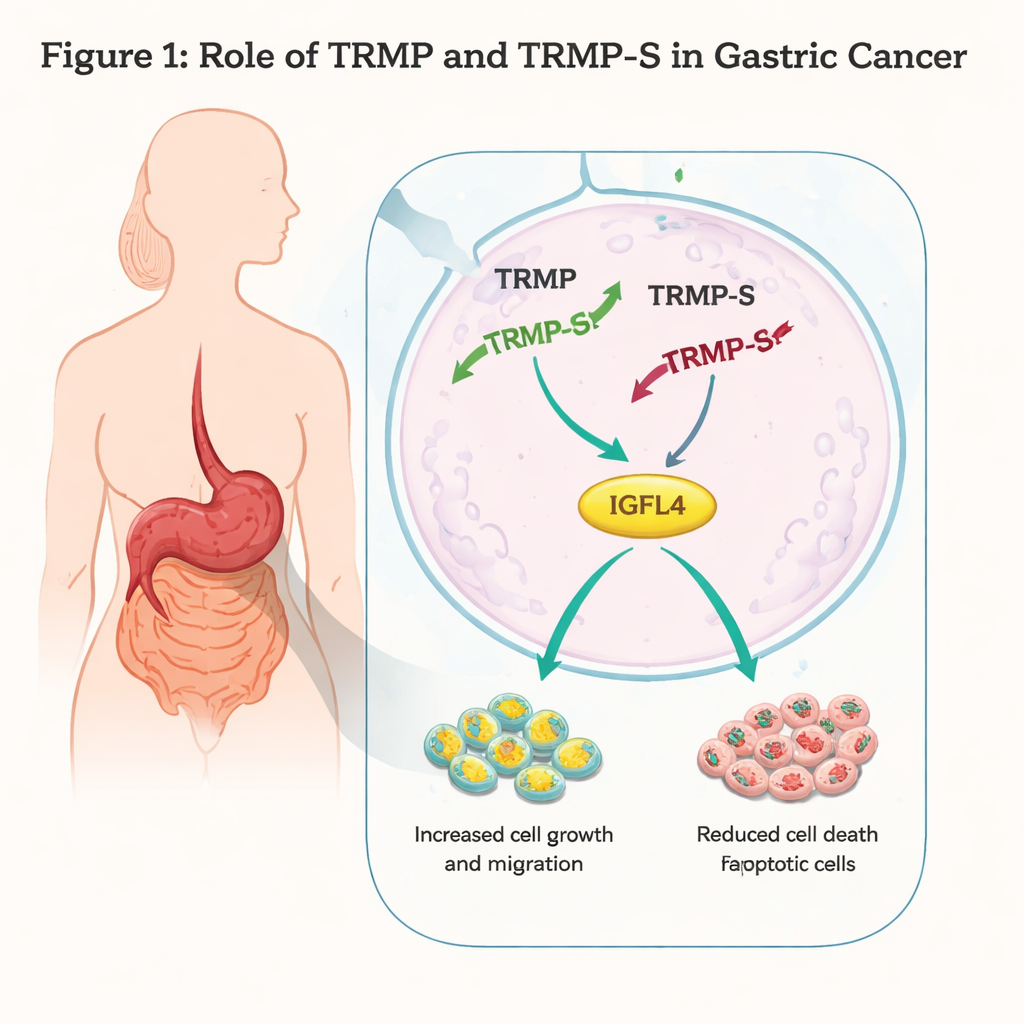
إيقاف مسرِّع السرطان
عمل الباحثون مع خطي خلایا بشریة لسرطان المعدة، AGS وMKN45، واستخدموا أدوات جينية لخفض مستويات TRMP-S وTRMP. عندما كتموا TRMP-S، نما سرطان الخلايا بطرف أقل، وتشكلت مستعمرات أقل، وكانت قدرتها على الهجرة عبر حواجز اصطناعية أو إغلاق الجروح في طبق أقل. أظهرت التحليلات بتقنية قياس التدفق وتحليلات البروتين أن عددًا أكبر من الخلايا خاضعة لموت مبرمج (الاستماتة) وأن دورة الخلية توقفت في طور G1، وهو «نقطة تفتيش» أساسية قبل نسخ الحمض النووي. ارتفعت مستويات p73، وهو عضو في عائلة كابحات الأورام p53، عند فقدان TRMP-S، ما يتوافق مع تحكم أقوى في دورة الخلية وزيادة الموت الخلوي. تشير هذه النتائج مجتمعة إلى أن TRMP-S يعمل عادة كمسرع لخلايا سرطان المعدة.
شريك رئيسي: إشارة IGFL4
لفهم كيف يمارس TRMP وTRMP-S تأثيراتهما، استخرج الفريق بيانات مرضى كبيرة من مستودع The Cancer Genome Atlas ومجموعة كورية لسرطان المعدة. بحثوا عن جينات مرتفعة الشذوذ في الأورام ومرتبطة إيجابيًا بمستويات TRMP، ثم بنوا نموذج «خطر» مكوَّنًا من ستة جينات تنبأ ببقاء المرضى على قيد الحياة — حيث ارتبطت الدرجات الأعلى بنتائج أسوأ. من بين هذه الجينات، برزت IGFL4: عضو في عائلة ذات صلة بعوامل النمو الشبيهة بالأنسولين، والمعروفة بدفعها للنمو والبقاء في العديد من السرطانات. في خلايا سرطان المعدة، أدى تقليل TRMP-S إلى خفض حاد في مستويات RNA والبروتين لـ IGFL4، بينما أظهرت تجربة ترسيب المناعة للرنا أن كلًا من TRMP وTRMP-S يرتبطان ماديًا ببروتين IGFL4. وأدى تقليل TRMP مباشرة إلى نفس التأثير المهدئ على IGFL4، مما يوحي بأن هذه الرناّيات الطويلة تساعد في تثبيت أو دعم إنتاج هذه الإشارة المحفزة للنمو.
تباطؤ الانتشار وإعادة تشكيل المشهد المناعي
عندما استخدم الباحثون رنا صغرى متداخلة لكتم IGFL4 نفسه، تباطأت خلايا سرطان المعدة في نموها، وقلت هجرتها، وأظهرت قدرة أضعف على اجتياز الأغشية وإغلاق الجروح. كشفت تحليلات بيانات أورام المرضى أن مستويات IGFL4 كانت أعلى بكثير في أورام المعدة مقارنةً بالنسيج المعدي الطبيعي، ومرتفعة أيضًا في العديد من أنواع السرطان الأخرى. والأهم من ذلك، أظهرت الأورام ذات التعبير العالي لـ IGFL4 أنماطًا مميزة من تغلغل الخلايا المناعية: مزيد من الخلايا البلعمية غير المتمايزة (M0) وأقل من خلايا البلازما والوحيدات واليوزينوفيليات والعدلات. أشارت الدرجات المناعية الحاسوبية إلى أن الأورام ذات IGFL4 المرتفع قد تستجيب بشكل أفضل للعلاجات المناعية الحديثة التي تعيق نقاط التفتيش المناعية، مما يوحي بأن IGFL4 قد يساعد في تحديد المرضى المناسبين لهذه العلاجات.
رنا صغير يدفع للخلف
كشف البحث أيضًا عن توازن مضاد لهذا المسار المحفز للسرطان. من خلال ارتباطات بين تعبير الميكروRNA والجينات في بيانات المرضى، حدَّد المؤلفون miR-129-5p كرنا صغير مرتبط سالبًا بكل من TRMP وIGFL4. في خلايا سرطان المعدة، أدى إضافة miR-129-5p إلى خفض مستويات IGFL4 وإبطاء النمو، بينما أدى حجب miR-129-5p إلى زيادة IGFL4 وتسريع التكاثر. لم يؤثر مرشح آخر، miR-4739، بشكل يُذكر على IGFL4 فتم استبعاده. تدعم هذه النتائج سلسلة تنظيمية تتكون من TRMP وTRMP-S وmiR-129-5p وIGFL4 تشكّل شبكة تضبط بدقة مدى عدوانية نمو خلايا سرطان المعدة وتفاعلها مع محيطها.
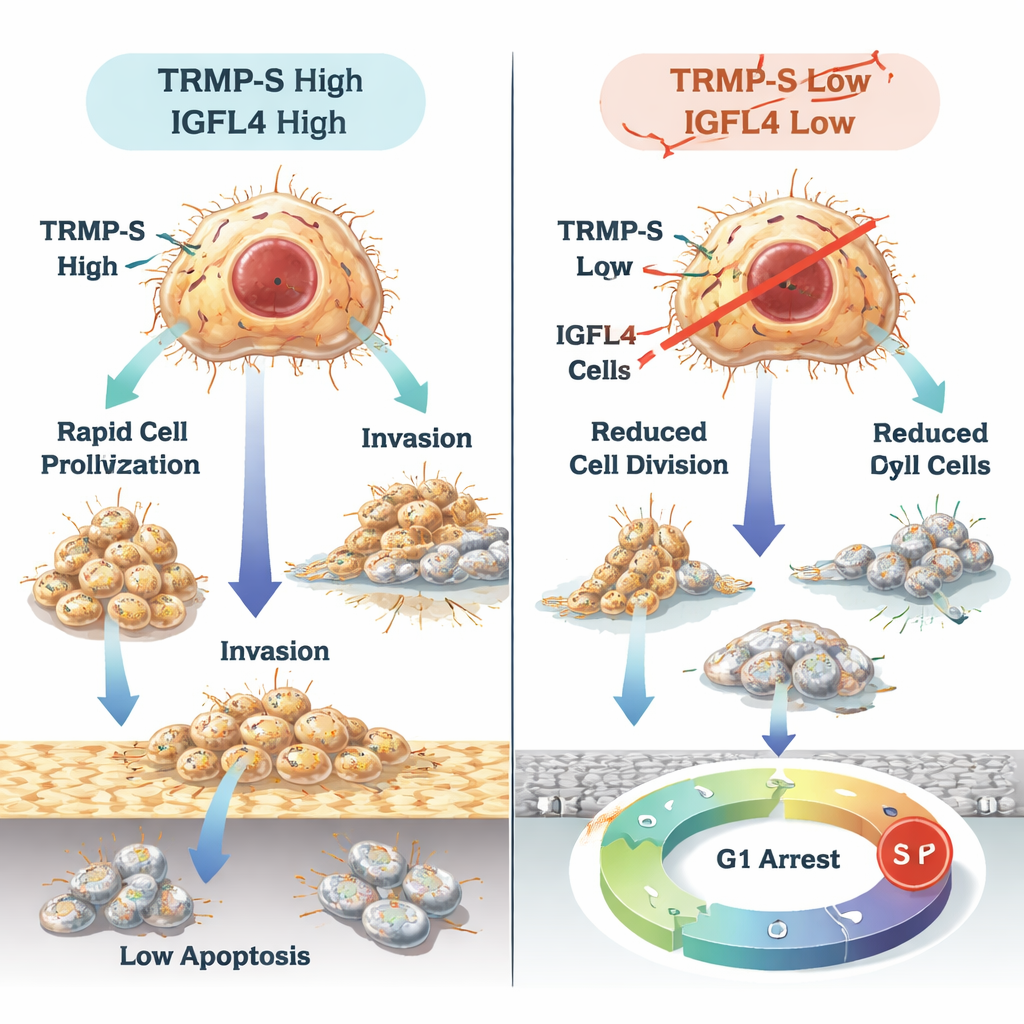
ماذا قد يعني هذا للمرضى
بعبارات بسيطة، تُظهر هذه الدراسة أن TRMP وTRMP-S يعملان كمخرجين خلف الكواليس يقومان بتشغيل IGFL4 ويساعدان خلايا سرطان المعدة على النمو والانتشار وتفادي آليات الكبح الطبيعية. في المقابل، يعمل الرنا الصغير miR-129-5p كفرملة على IGFL4، وتساهم IGFL4 نفسها في تشكيل كيفية تجمع الخلايا المناعية حول الأورام ومدى فعالية العلاجات التي تُنَشِّط الجهاز المناعي. وعلى الرغم من الحاجة إلى مزيد من البحوث والاختبارات السريرية، تمثل TRMP وTRMP-S وIGFL4 وmiR-129-5p مجموعة واعدة من العلامات للتنبؤ بالتكهن ومن أهداف محتملة لأدوية تهدف إلى إبطاء أو إيقاف سرطان المعدة.
الاستشهاد: Zhang, M., Mi, Y., Li, F. et al. Senescence-associated LncRNAs TRMP and TRMP-S promote gastric cancer by activating IGFL4. Sci Rep 16, 6740 (2026). https://doi.org/10.1038/s41598-026-37106-9
الكلمات المفتاحية: سرطان المعدة, الرنا الطويل غير المشفر, TRMP, IGFL4, البيئة المجهرية للورم