Clear Sky Science · ar
تحديد RBX1 كمُنظّم لتَنسخ LIPT1 ودوره في موت الخلايا المحفز بالنحاس في خلايا الورم الأرومي الحُبيبي
لماذا النحاس وأورام الدماغ مهمان
الورم الأرومي الدبقي المتعدد هو أحد أخطر أنواع سرطان الدماغ، حيث يعيش معظم المرضى فترة قصيرة فقط بعد التشخيص رغم الخضوع لعمليات جراحية وعلاجات إشعاعية وكيميائية مكثفة. تستكشف هذه الدراسة حليفًا غير متوقع لمواجهة هذه الأورام: المعدن النحاس. يفحص الباحثون شكلًا جديدًا من موت الخلايا يتم تحفيزه بواسطة النحاس ويحددون مسارًا جزيئيًا قد يساعد الأطباء على استغلال هذه العملية لإضعاف الأورام وربما تعزيز هجوم جهاز المناعة ضد الخلايا السرطانية.
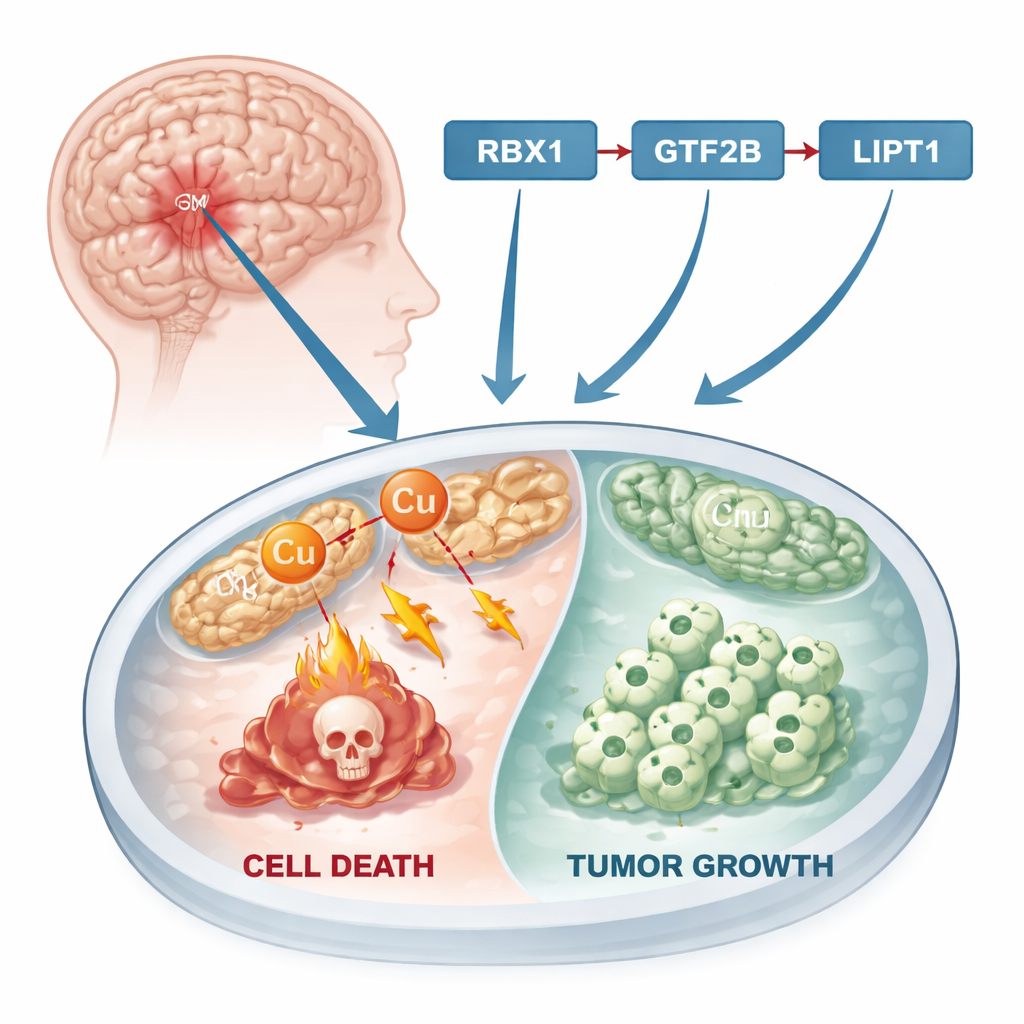
طريقة جديدة لموت الخلايا
لعقود، ركز بحث السرطان على أشكال مألوفة من موت الخلايا مثل الاستماتة، حيث تُوقف الخلايا التالفة نفسها بهدوء. مؤخرًا اكتشف العلماء مسارًا مختلفًا يُدعى موت الخلايا المحفز بالنحاس، أو «الكوبرُبتُوسيس» (cuproptosis). في هذه العملية، يتراكم النحاس الزائد داخل مصانع الطاقة في الخلية، الميتوكوندريا. هناك يعطّل البروتينات الأساسية، مما يؤدي إلى تكوّن تكتلات سامة وينهي حياة الخلية في النهاية. وبما أن العديد من الأورام تتميز باضطراب في أيض المعادن وارتفاع مستويات النحاس مقارنة بالأنسجة الطبيعية، فإن الكوبرُبتُوسيس يقدم نقطة ضغط محتملة: إذا تمكن الباحثون من دفع الخلايا الورمية نحو هذا النمط المميت المرتبط بالنحاس، فقد يبطئون أو يوقفون نمو السرطان.
إبراز جين أساسي في الورم الأرومي الدبقي
بدأ المؤلفون بمسح مجموعة من الجينات المعروفة بالفعل بتورطها في الكوبرُبتُوسيس وسألوا كيف تتصرف في عينات الورم الأرومي الدبقي مقارنةً بأنسجة الدماغ الطبيعية. تميز جين واحد على نحو خاص، اسمه LIPT1. كان أكثر نشاطًا في أنسجة الورم الأرومي الدبقي وفي عدة خطوط خلوية للورم مقارنة بالخلايا الدماغية الطبيعية. والأهم من ذلك، أن المرضى الذين كانت أورامهم تظهر نشاطًا أعلى لـ LIPT1 كان لديهم ميل للبقاء لفترة أطول بدون عودة السرطان بعد العلاج. كما ارتبطت المستويات العالية من LIPT1 بوجود أكبر لخلايا CD8 T، القاتلة الخطّية للسرطان في جهاز المناعة، مما يوحي بأن هذا الجين قد يساعد في جعل بيئة الورم أكثر عرضة للهجوم المناعي.
ماذا يحدث عندما يتم خفض مفتاح موت النحاس
لاختبار ما إذا كان LIPT1 يؤثر فعلًا على موت الخلايا المحفز بالنحاس، عرض الفريق خلايا الورم الأرومي الدبقي لمركب دوائي حامِل للنحاس يُحفّز الكوبرُبتُوسيس بشكل موثوق. ثم استخدموا أدوات جينية لتقليل مستويات LIPT1. عندما تم قمع LIPT1، أصبحت الخلايا الورمية أكثر مقاومة لقتل النحاس، ونجت بمعدل أعلى، وأظهرت قدرات أقوى على الهجرة والغزو—سلوكيات مرتبطة بسرطان أكثر عدوانية. في مزروعات مختلطة من خلايا الورم وخلايا CD8 البشرية، أدى خفض LIPT1 أيضًا إلى تقليل إفراز جزيئات الإشارة المناعية وجعل الخلايا السرطانية أصعب على خلايا T أن تُدمرها. معًا تشير هذه التجارب إلى أن LIPT1 يزيد الحساسية لموت الخلايا المحفز بالنحاس ويدعم النشاط المناعي المضاد للورم.
متابعة سلسلة الأوامر حتى RBX1
التحدي التالي كان فهم لماذا يتم تشغيل LIPT1 بشكل أعلى في الورم الأرومي الدبقي. من خلال جمع عدة قواعد بيانات جينية وبروتينية كبيرة، حدَّد الباحثون عامل نسخ—نوع من مفاتيح التشغيل الرئيسة لنشاط الجين—يدعى GTF2B الذي يرتبط بالقرب من جين LIPT1 ومن المحتمل أن يعزز تعبيره. ثم تساءلوا عمّا يسيطر على GTF2B نفسه. برزت بروتين ثانية، RBX1، كمرشح قوي. RBX1 جزء من نظام الوسم والإتلاف في الخلية الذي يحدد بروتينات أخرى لتفككها. في خلايا الورم الأرومي الدبقي، كانت مستويات RBX1 أقل منها في خلايا الدماغ الطبيعية، بينما كان GTF2B وLIPT1 أعلى. أظهرت تجارب مخبرية أن RBX1 يمكنه إرفاق وسمّات صغيرة «أيّنوني للتدمير» بـ GTF2B، ما يؤدي إلى تحلله؛ عندما ازداد RBX1، انخفضت مستويات GTF2B ونشاط LIPT1، وإيقاف آلية التحلل الخلوي عكس هذا التأثير.
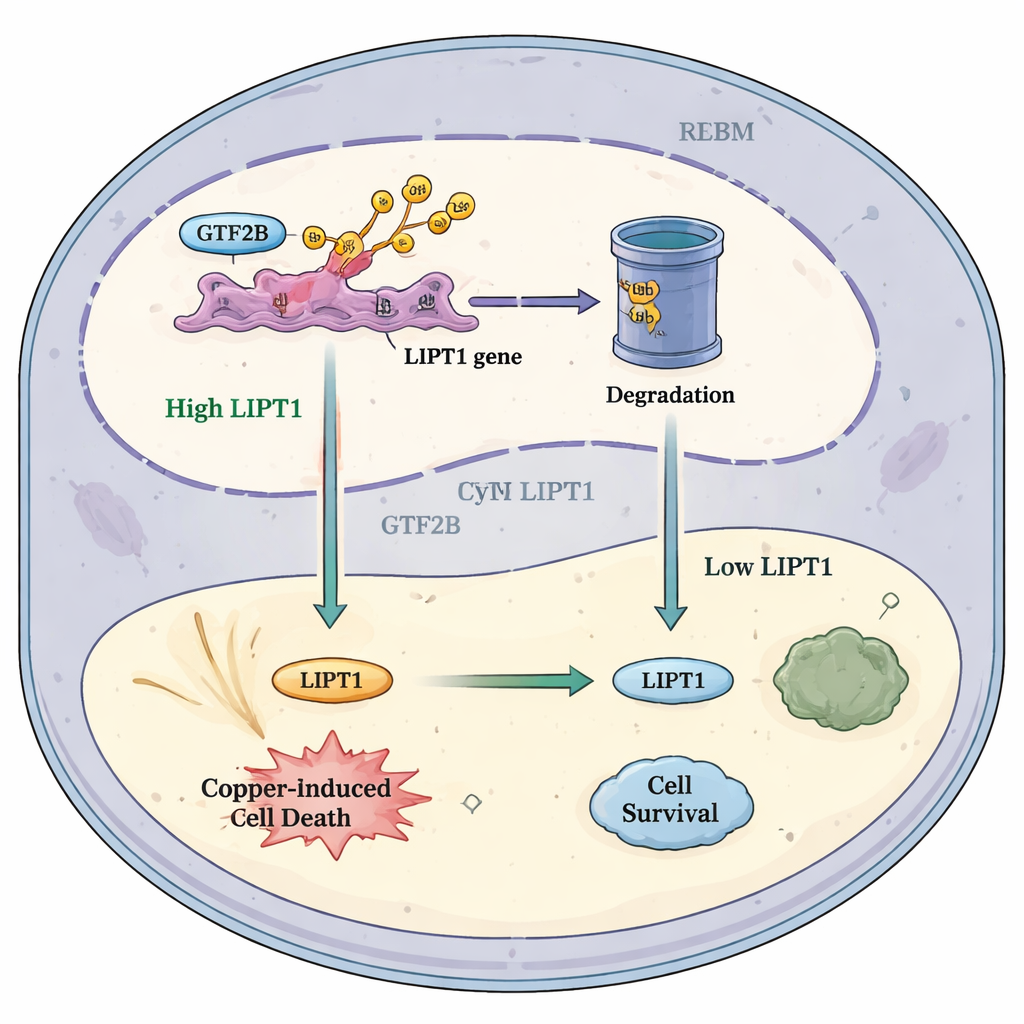
كيف قد يساعد هذا المسار العلاجات المستقبلية
بوضع هذه النتائج معًا، يقترح المؤلفون نموذجًا بسيطًا: في الظروف الصحية، يحافظ RBX1 على ضوابط على GTF2B، مقيدًا مدى قوة تحفيزه لجين LIPT1. في الورم الأرومي الدبقي، يقلُّ RBX1 ما يعني أن GTF2B يُحال أقل للتفكك. يرفع فائض GTF2B بعد ذلك LIPT1، مما يزيد حساسية الخلايا الورمية لموت الخلايا المحفز بالنحاس ويجذب المزيد من الخلايا المناعية المقاتلة للسرطان. يشير هذا النموذج إلى أن ضبط هذا المسار RBX1–GTF2B–LIPT1 بعناية، ربما إلى جانب أدوية تستهدف النحاس والعلاجات المناعية، قد يغيّر التوازن داخل أورام الدماغ نحو الانحلال الذاتي. رغم أن هناك عملًا كبيرًا ينتظر قبل أن يصل هذا المفهوم إلى المرضى، تسلط الدراسة الضوء على تقاطع واعد بين بيولوجيا المعادن، تنظيم الجينات، ومناعة السرطان قد يفتح سبل علاجية جديدة لأحد أكثر أنواع السرطان صعوبة.
الاستشهاد: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
الكلمات المفتاحية: السركومة النخاعية الدبقية المتعددة, موت الخلايا المحفز بالنحاس, LIPT1, علم المناعة الورمي, مسار RBX1