Clear Sky Science · ar
دمج تعلّم الآلة والنمذجة الفيزيائية للتصميم التنبؤي للمواد النانوية المحمّلة بالجيمسيتابين
أدوية سرطان أذكى حسب التصميم
أدوية السرطان مثل الجيمسيتابين يمكن أن تنقذ الأرواح، لكنها غالباً ما تتصرف كأدوات فجة بدلاً من آلات دقيقة: تتحلل بسرعة، وتفشل في الوصول إلى هدفها، وتسبب آثاراً جانبية قاسية. يستعرض هذا البحث كيف يمكن لأجهزة الكمبيوتر مساعدة العلماء في «الاختبار المسبق» لحوامل الدواء النانوية الجديدة على الشاشة بدلاً من الاكتفاء بالتجارب المخبرية، لجعل علاجات الجيمسيتابين أكثر فاعلية، أطول أمداً، وأكثر أماناً محتملًا للمرضى.
لماذا تهم الحوامل الصغيرة
يملأ العلاج الكيميائي التقليدي الجسم بجزيئات دوائية تدور في كل مكان، وليس داخل الأورام فقط. تقدم المواد النانوية المركبة — جسيمات مصممة أصغر بآلاف المرات من حبة رمل — وسيلة لتعبئة الجيمسيتابين بحيث يكون محمياً في مجرى الدم ويتم توصيله بصورة أكثر مباشرة إلى الخلايا السرطانية. رقمان يحددان إلى حد كبير ما إذا كان التصميم مفيداً. كفاءة التحميل تُظهر مقدار الدواء الذي ينتهي به المطاف داخل كل جسيم، بينما تقيس كفاءة التغليف النسبة المئوية من الدواء الابتدائي الذي يُحتجز بنجاح بدلاً من أن يُهدر. قيم مرتفعة لكليهما تعني حقناً أقل، وكمية ناقل أقل، وفرصة أفضل لضرب الورم بقوة دون إرهاق بقية الجسم.
من التجربة والخطأ إلى التصميم الموجه بالبيانات
تصميم هذه الحوامل النانوية يدوياً يشبه محاولة ضبط راديو بمئات المقابض — حجم الجسيم، الشحنة السطحية، المواد، الطبقات، وطرق التحضير كلها تتفاعل بطرق معقدة. حتى الآن، كان الباحثون يغيرون إعداداً أو اثنين في كل مرة ويقيسون الناتج، دورة بطيئة ومكلفة تكشف جزءاً صغيراً فقط من الصورة الكاملة. في هذا العمل، جمع المؤلفون 59 وصفة محمّلة بالجيمسيتابين تم التحقق منها بعناية من الأدبيات العلمية وأغنوها بأمثلة إضافية مبنية على الفيزياء تم توليدها حاسوبياً. سمح لهم هذا المزيج من البيانات باختبار عدة نهج في تعلّم الآلة — برامج حاسوبية تتعلم الأنماط من البيانات — للتنبؤ بكفاءتي التحميل والتغليف من خيارات التصميم وحدها.
جعل الفيزياء توجه الخوارزميات
معظم أنظمة تعلّم الآلة هي ملائمة قوية للمنحنيات: يمكنها اكتشاف الأنماط لكنها لا تعرف متى تكون الإجابة مخالفة لقوانين الطبيعة. لتجنب التنبؤات غير الواقعية، بنى الباحثون طريقة هجينة تمزج بين البيانات وقواعد فيزيائية أساسية حول كيفية تحرك جزيئات الدواء، ارتباطها، وتوازنها في نظام مغلق. في إطارهم، أي تنبؤ قد يوحي، على سبيل المثال، بخلق دواء أكثر مما أُضيف في الأصل، أو تجاهل كيفية انتشار الجزيئات خلال مادة ما، يُعاقب بلطف أثناء التدريب. هذا النهج «المُعلَم بالفيزياء» يدفع النموذج نحو إجابات منطقية كيميائياً وفيزيائياً، خصوصاً في مناطق فضاء التصميم التي تقل فيها القياسات الحقيقية.
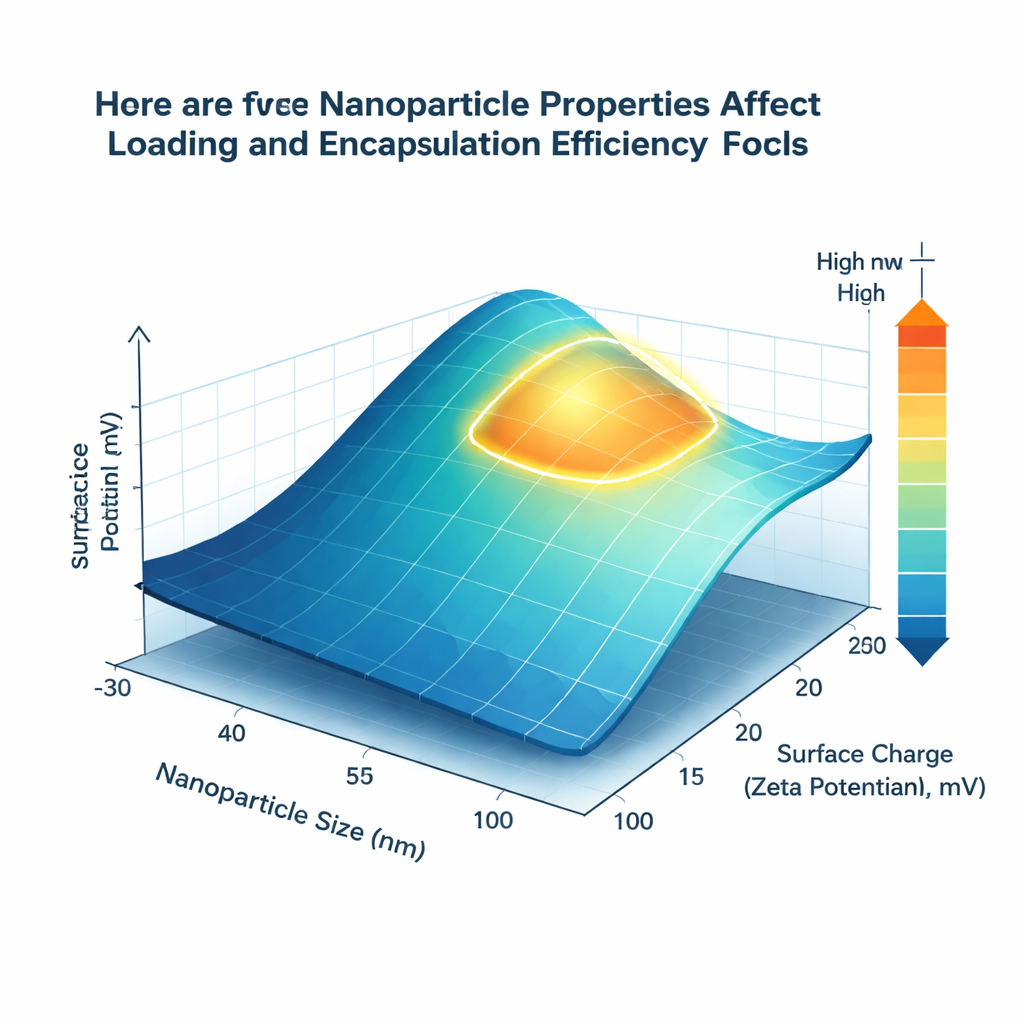
ما الذي اكتشفته النماذج
من بين التقنيات المختبرة، أعطى خوارزمية تجميعية متقدمة تُدعى XGBoost أدق التنبؤات، مطابقةً عن كثب النتائج التجريبية المبلغ عنها لكلتا الكفاءتين الرئيسيتين. لكن إلى جانب الدقة، أراد الفريق قواعد تصميم مفهومة. باستخدام طريقة تُدعى SHAP، التي تصنف مدى قوة تأثير كل عامل في رفع أو خفض التنبؤ، وجدوا أن حجم الجسيم والشحنة السطحية يهيمنان باستمرار على الأداء. قدمت الحوامل النانوية ذات القطر بين نحو 80 و150 نانومتراً أفضل توازن بين المساحة السطحية والحجم الداخلي، مما زاد كل من التحميل والتغليف. ارتبطت الشحنة السطحية الموجبة الخفيفة، في نطاق +15 إلى +25 ميليفولت، بتحسن احتجاز الجيمسيتابين، ربما لأن الأسطح الحاملة الموجبة الشحنة تتفاعل بشكل ملائم مع مجموعات الدواء سالبة الشحنة.
خريطة رقمية لعلاجات سرطانية مستقبلية
النتيجة النهائية ليست دواءً جاهزاً بل أداة تخطيط قوية. يقدم البحث نوعاً من «خريطة التصميم» التي توجه الباحثين نحو وصفات حوامل نانوية من المرجح أن تحتفظ بالجيمسيتابين وتحميه جيداً، مع تجنب ملايين التركيبات غير الموفقة. يؤكد المؤلفون أن تنبؤاتهم لا تزال بحاجة إلى تأكيد في دراسات مخبرية وحيوانية جديدة، وأن مجموعة بياناتهم — رغم جمعها بعناية — متواضعة الحجم. ومع ذلك، يوضح هذا الإطار الموجه بالفيزياء لتعلّم الآلة كيف يمكن لأجهزة الكمبيوتر تضييق البحث عن حوامل دوائية للسرطان أفضل، مما يخفض التكاليف ويسرّع الرحلة من الأفكار إلى علاجات أكثر دقة وملاءمة للمرضى.
الاستشهاد: Rahdar, A., Fathi-karkan, S. & Shirzad, M. Integrating machine learning and physics-based modeling for predictive design of gemcitabine-loaded nanocomposites. Sci Rep 16, 6268 (2026). https://doi.org/10.1038/s41598-026-37098-6
الكلمات المفتاحية: الطب النانوي, جيمسيتابين, توصيل الأدوية, تعلّم الآلة, جسيمات نانوية