Clear Sky Science · ar
تسلسل الأمبليكُون بتقنيات أوكسفورد نانوبور كبديل تشخيصي لفيروسات اللنتيفيروسات في المجترات الصغيرة لدى الأغنام
عدوى خفية في الأغنام اليومية
تحمل الأغنام في أنحاء العالم في صمت فيروسات يمكن أن تضعف صحتها وتقصّر عمرها وتكبّد المزارعين خسائر مالية — وغالباً من دون أعراض واضحة لسنوات. تستكشف هذه الدراسة طريقة جديدة لكشف تلك العدوى الخفية باستخدام تقنية تسلسل DNA محمولة، مقدمة خطوة محتملة في كيفية حماية رفاه الحيوان ودخل المزارع وحتى الأمن الغذائي.
مرض بطيء ومكلف يصعب رصده
تركز الدراسة على فيروسات اللنتيفيروسات في المجترات الصغيرة (SRLV)، وهي مجموعة من الفيروسات التي تصيب الأغنام والماعز. في الأغنام، تسبب مرض الميدي-فيزنا، وهو عدوى طويلة الأمد قد تؤدي إلى مشاكل في التنفس، والتهاب مفاصل، وأمراض دماغية، والتهاب مزمن في الضرع. العديد من الحيوانات المصابة لا تظهر عليها علامات واضحة، ومع ذلك يقلل الفيروس من إنتاج الحليب، ويزيد وفيات الحملان، ويجبر على الذبح المبكر. في بعض القطيع الحلوب الأوروبية، بما في ذلك إسبانيا واليونان، قد يكون نحو نصف الحيوانات مصاباً، مما يجعل هذا أحد أهم أمراض الأغنام في المزارع المكثفة.
لماذا تفشل الاختبارات الحالية في كشف العديد من الحيوانات المصابة
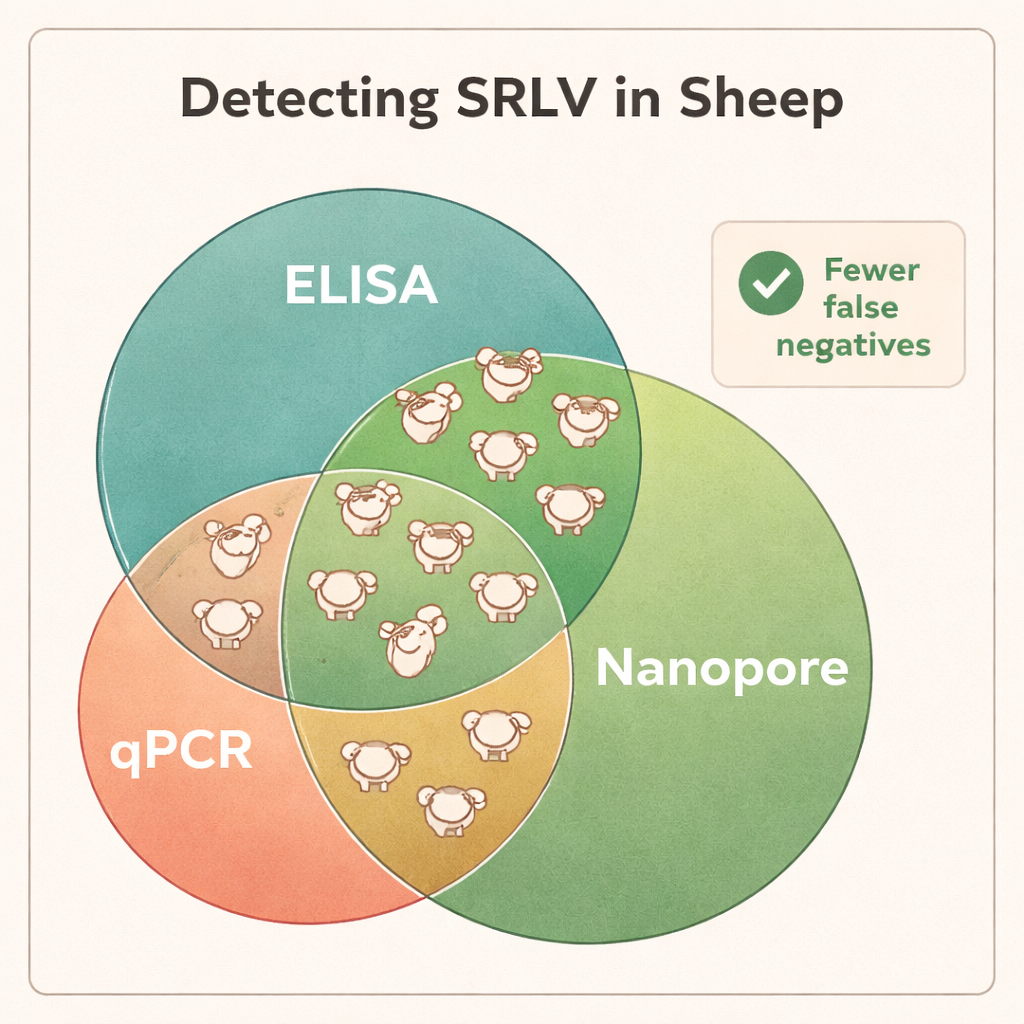
حالياً تعتمد المزارع أساساً على اختبارات الدم التي تبحث عن الأجسام المضادة (ELISA) أو على اختبارات الحمض النووي القياسية (qPCR) لتحديد أي الحيوانات مصابة ويجب إزالتها من القطيع. لكن SRLVs تتحور وتعيد التركيب بسرعة، مكونة العديد من المتغيرات الفيروسية المتقاربة. بعض المتغيرات لا تتعرف عليها اختبارات الأجسام المضادة بشكل جيد، وبعض الأغنام المصابة لا تطور استجابة مضادية قوية على الإطلاق. qPCR، التي تستهدف مقاطع قصيرة ومحددة جداً من DNA الفيروس، قد تفشل أيضاً إذا تغيرت مناطق الهدف تلك. نتيجة لذلك، تختبر العديد من الحيوانات المصابة فعلاً على أنها سلبية وتبقى في القطيع، ناشرة الفيروس بهدوء.
استخدام قراءة DNA في الوقت الحقيقي لاكتشاف الفيروس
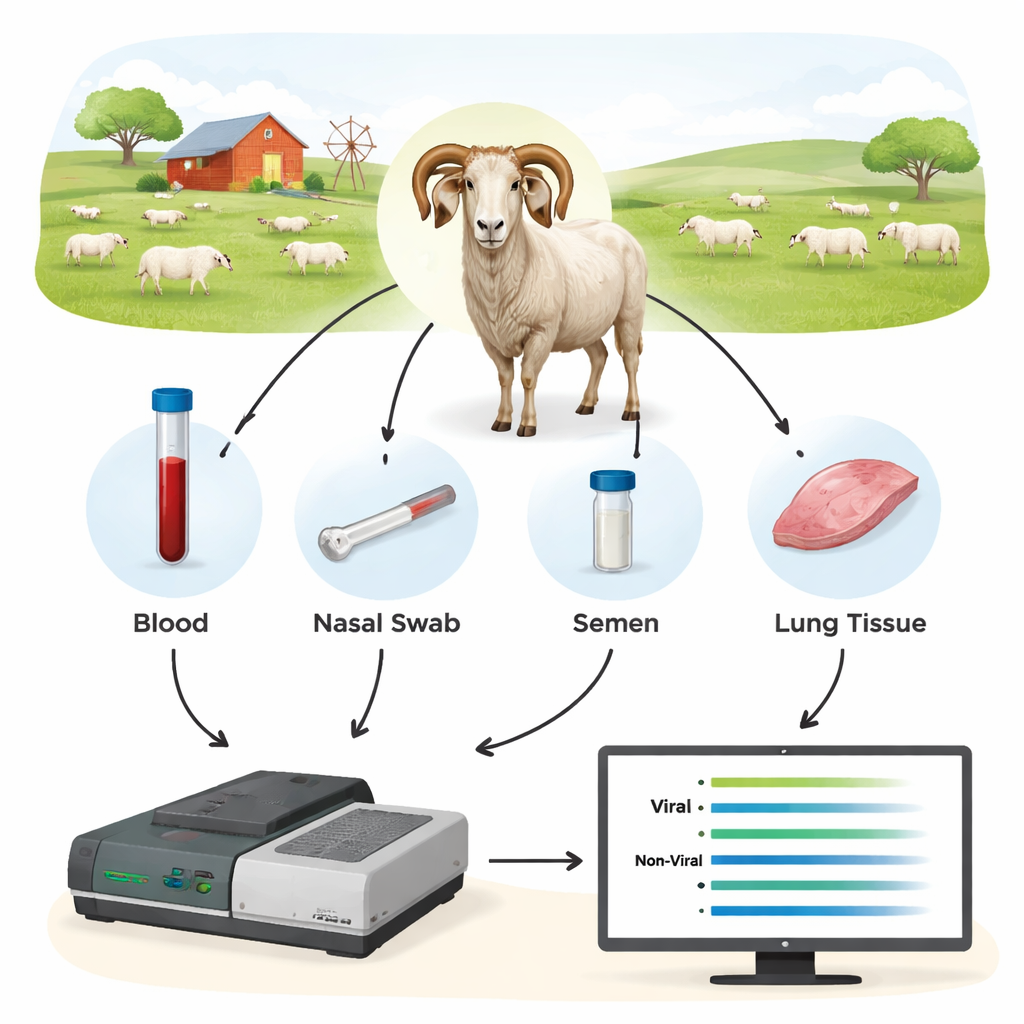
اختبر الباحثون طريقة من الجيل الثالث تسمى تسلسل أوكسفورد نانوبور كأداة تشخيصية جديدة. بدلاً من البحث عن قطعة صغيرة واحدة من DNA الفيروس، قاموا أولاً بتضخيم مقاطع أطول من جينات فيروسية رئيسية من عينات الحيوانات ثم تسلسلوا تلك المقاطع في الوقت الحقيقي على جهاز نانوبور. جمعوا دماء ومسحات أنفية، وسائل منوية، وخلايا من الدم والرئتين من 44 كبشاً وأغنام إضافية، العديد منها سبق اختباره بالطرق التقليدية. من خلال التركيز على مناطق فيروسية محافظة نسبياً لكنها طويلة بما يكفي لكشف السلالة الدقيقة، تمكن الفريق من اكتشاف العدوى وتحديد أنواع الفيروسات الموجودة.
الدم هو الأنسب — ويكشف ما تفوته الاختبارات الأخرى
أظهر التسلسل أن DNA من الدم الكامل كان المادة الأكثر موثوقية لاكتشاف SRLV، رغم أن الفيروس يعيش أساساً في فئة صغيرة من خلايا الدم البيضاء. أعطت أنسجة الرئة من الحيوانات المصابة بشدة كميات عالية جداً من DNA الفيروس، لكن مثل هذه العينات متاحة فقط بعد الذبح. بالمقابل، قدمت المسحات الأنفية، والسائل المنوي، والخلايا البيضاء المصفاة مادة فيروسية قليلة جداً للتشخيص المتسق. عندما قارن العلماء نتائج نانوبور مع اختبارات ELISA وqPCR التقليدية، كانت الفوارق لافتة: أكدت تسلسلات نانوبور العدوى في جميع الكباش الإيجابية بـELISA لكنها كشفت أيضاً أن العديد من الحيوانات السلبية بـELISA كانت في الواقع مصابة. عبر قطعان مختلفة، تبين أن نحو 40–45% من الحيوانات المصنفة «سلبية» بواسطة ELISA كانت حاملة للفيروس، وقد فشل qPCR في اكتشاف جزء أكبر حتى. كما كشفت بيانات التسلسل عن عدوى مشتركة بأنواع SRLV مختلفة في بعض الكباش، وهي معلومة لا توفرها الاختبارات التقليدية بسهولة.
من إجابة بنعم/لا إلى رؤى أعمق
بما أن نانوبور يقرأ تسلسلات الفيروس الفعلية، فهو يستطيع أن يتجاوز التشخيص البسيط بنعم أو لا. استخدم الفريق البيانات لمقارنة السلالات الفيروسية، وبناء أشجار نسب للفيروسات المتداولة في قطعانهم، ودراسة اختلافات طفيفة في البروتينات الفيروسية التي قد تفسر سبب هروب بعض الحيوانات من كشف مجموعات ELISA القياسية. أظهروا أن نسخاً معينة من بروتين فيروسي أساسي، تستهدفها اختبارات الأجسام المضادة التجارية، تختلف بشكل ملحوظ بين الحيوانات الإيجابية والسلبية بالأجسام المضادة. مع مرور الوقت، يمكن أن تساعد مثل هذه المعلومات في تحسين كل من الاختبارات المصلية وبرامج التربية الهادفة لاختيار حيوانات أكثر مقاومة طبيعياً للعدوى.
ما معنى ذلك للمزارعين وصحة الحيوان
بالنسبة لغير المتخصصين، الرسالة الأساسية بسيطة: بقراءة مقاطع أطول من DNA الفيروس مباشرةً، يمكن لتسلسل نانوبور كشف المزيد من الأغنام المصابة، في وقت أبكر وبدرجة دقة أعلى، مقارنة بالاختبارات الروتينية الحالية. كما يحدد بالضبط أي سلالات فيروسية موجودة في القطيع. رغم أن هذا النهج لا يزال أكثر تعقيداً وتكلفة من اختبار دم واحد، فإن التكنولوجيا تصبح أسرع وأرخص وأكثر قابلية للحمل. إذا تم دمجها في برامج السيطرة، فقد تقلل بشدة من عدد الحاملين «الخفاء»، وتحسّن تصميم اللقاحات والاختبارات، وتدعم تربية حيوانات أكثر مقاومة — مما يجعل تربية الأغنام أكثر استدامة وإنسانية.
الاستشهاد: Serrano, M., González, C., Roy, R. et al. Amplicon sequencing with Oxford nanopore technologies as a diagnostic alternative for small ruminant lentiviruses in sheep. Sci Rep 16, 6212 (2026). https://doi.org/10.1038/s41598-026-36989-y
الكلمات المفتاحية: صحة الأغنام, لنتيفيروس, تسلسل نانوبور, تشخيص بيطري, ميدي-فيزنا