Clear Sky Science · ar
التحليل البروتيومي الكمي للمصل بعد التكييف الإقفاري البعيد في السكتة الإقفارية الحادة
لماذا قد يساعد عصر الذراع على حماية الدماغ
عندما يحدث سكتة نتيجة انسداد وعاء دموي، كل دقيقة من انخفاض تدفق الدم تهدد خلايا الدماغ. تهدف العلاجات القياسية إلى إعادة فتح الشريان المسدود، لكن العديد من المرضى يصلون بعد فوات الأوان أو لا يكونون مؤهلين للعلاج. يستكشف الباحثون علاجًا مساعدًا بسيطًا بشكل مدهش: قطع تدفق الدم مؤقتًا إلى ذراع أو ساق بواسطة كفة ضغط دم، وهي استراتيجية تُسمى التكييف الإقفاري البعيد (RIC). يطرح هذا البحث سؤالًا أساسيًا لتحويل الفكرة إلى علاج فعلي: ما الذي يغيره RIC بالضبط في دم مرضى السكتة، وهل يمكن أن تشير هذه التغييرات إلى من قد يستفيد أكثر؟
إشارة توتّر لطيفة تُرسل من الطرف إلى الدماغ
يعمل RIC عن طريق نفخ كفة حول طرف الجسم لعدة دقائق بشكل متكرر ثم تفريغها، محدثًا نوبات قصيرة وغير ضارة من انخفاض تدفق الدم. تشير تجارب حيوانية وتجارب سريرية مبكرة إلى أن هذا "التوتر المتحكم فيه" يمكن أن يرسل إشارات إلى أعضاء بعيدة، بما في ذلك الدماغ، لتشغيل برامج حماية. في تجربة سريرية كبيرة اسمها RICAMIS، تحسّن أداء المرضى ذوي السكتة الإقفارية المتوسطة الذين تلقوا RIC بالإضافة إلى الرعاية المعتادة بعد 90 يومًا مقارنة بمن تلقوا الرعاية المعتادة وحدها. ومع ذلك، لم تَرَ تجربة أخرى (RESIST) مثل هذا الفائدة، مما ترك الأطباء في حيرة حول متى ولمن يعمل RIC فعلاً. يَغوص الدراسة الحالية في دم المرضى للبحث عن دلائل جزيئية—بروتينات قابلة للقياس، أو مؤشرات حيوية، تتغير مع مرور الوقت مع تطبيق RIC.
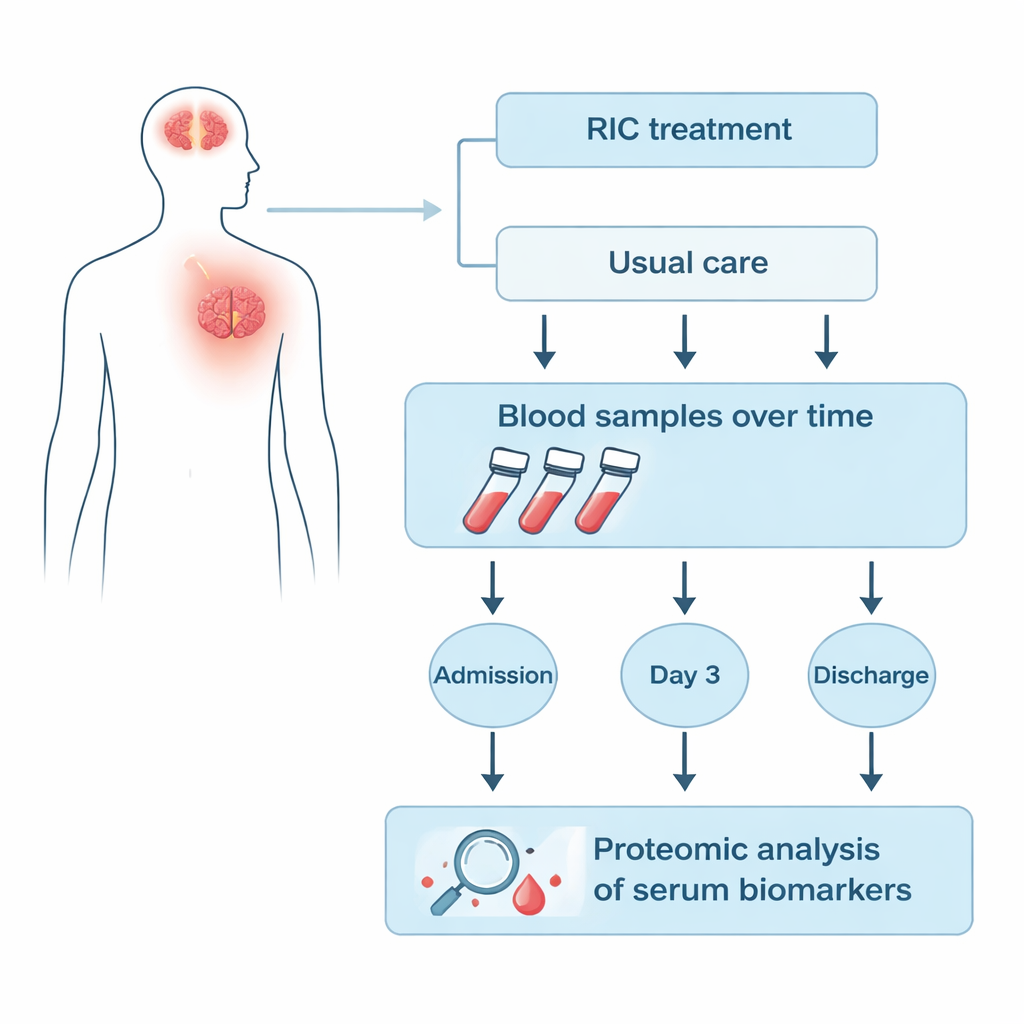
متابعة دم المرضى خلال إقامتهم في المستشفى
ركز الباحثون على 25 مريضًا من تجربة RICAMIS التي أُخذت منهم عينات دم في ثلاث نقاط: عند الدخول، وبعد ثلاثة أيام من تخصيص العلاج، وعند خروج المستشفى. تسعة مرضى تلقوا RIC بالإضافة إلى الرعاية المعتادة، في حين تلقى ستة عشر رعاية معتادة فقط. باستخدام تقنية تسمى البروتيوميات الكمية، قاس الفريق مئات البروتينات في جزء المصل من الدم دفعة واحدة، بدلًا من فحص عدد قليل من العلامات المختارة مسبقًا. ثم قارنوا كيف ارتفعت أو انخفضت مستويات كل بروتين مع مرور الوقت في مجموعة RIC مقابل مجموعة التحكم للعثور على بصمات مرتبطة بشكل فريد بـ RIC.
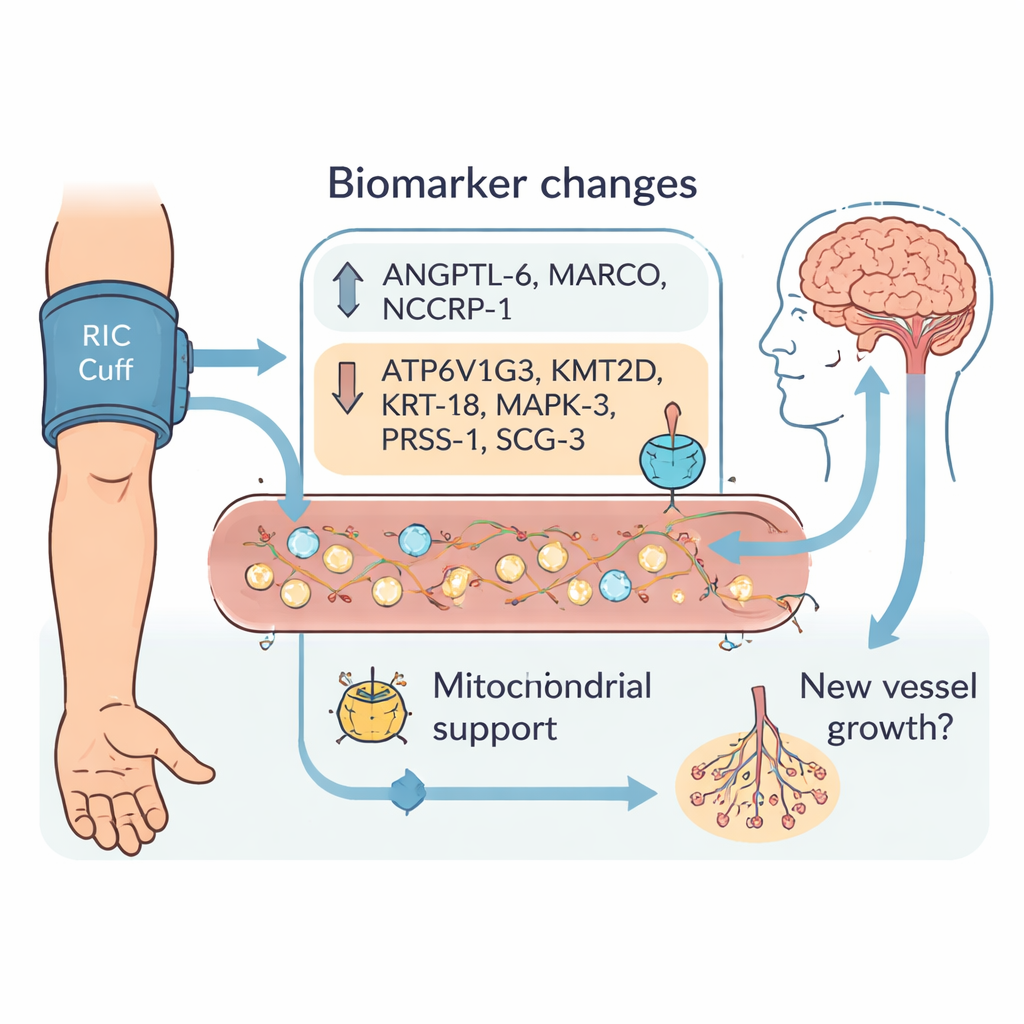
تسعة إشارات بارزة في مجرى الدم
طوال فترة الإقامة في المستشفى، تغيّرت عشرات البروتينات بشكل مختلف بين المجموعتين. بعد ترشيح دقيق، أبرز الفريق تسعة مؤشرات حيوية تغيرت من الدخول إلى اليوم الثالث وإلى وقت الخروج بطرق فصلت بوضوح بين المرضى المعالجين بـ RIC ومثيلاتهم في الضبط. ارتفعت ثلاثة بروتينات—ANGPTL‑6 وMARCO وNCCRP‑1—بمعدل أكبر مع RIC. أما ستة أخرى—ATP6V1G3 وKMT2D وKRT‑18 وMAPK‑3 وPRSS‑1 وSCG‑3—فأظهرت ميلًا للنقصان. يشارك العديد من هذه الجزيئات في كيفية إدارة الخلايا للطاقة في مصانعها الصغيرة (الميتوكوندريا)، أو في كيفية نمو الأوعية الدموية وإعادة تشكيلها. يتسق هذا مع الفكرة أن RIC لا يقتصر على حماية الخلايا العصبية من الضرر، بل قد يساعد مناطق الدماغ المصابة على إعادة التنظيم، وإصلاح الإمداد الدموي، واستعادة الوظيفة على مدى أيام إلى أسابيع.
مؤشرات حول استخدام الطاقة ونمو الأوعية الجديدة
لفهم أفضل لما قد تفعله هذه البروتينات التسعة، ربط المؤلفون بينها وبين مسارات بيولوجية معروفة. يرتبط اثنان منهما، KMT2D وMAPK‑3، بكيفية تغليف الحمض النووي وكيفية تشغيل أو إطفاء الجينات، خاصة في برامج مرتبطة بنمو الأوعية. أما أخرى، مثل ATP6V1G3 وKRT‑18، فقد رُبطت في أعمال سابقة بالمحافظة على صحة الميتوكوندريا وحماية نسيج القلب بعد الإصابة. مجتمعة، تشير هذه الأنماط إلى أن RIC قد يدفع الجسم نحو استخدام أكثر كفاءة للطاقة ويشجّع نمو الأوعية أو إعادة تشكيلها—مما قد يحسّن التدفق الدموي حول المنطقة المتضررة من السكتة. وفي الوقت نفسه، قد تعكس بعض المؤشرات، مثل NCCRP‑1 وMARCO، استجابة الجسم للضغط الحاد والاستجابة المناعية لإجراء نفخ الكفة نفسه، مما يؤكد أن RIC يثير رد فعل معقدًا على مستوى الجسم ككل.
ماذا يعني هذا لرعاية السكتة في المستقبل
لا تستطيع هذه الدراسة الاستكشافية الصغيرة إثبات بالضبط كيف يحمي RIC الدماغ، وقد شملت فقط 25 مريضًا من بلد واحد، لذا يجب تأكيد النتائج في مجموعات أكبر وأكثر تنوعًا. ومع ذلك، يمثل تحديد قائمة قصيرة من تسعة بروتينات تتحرك باستمرار في اتجاهين متعاكسين مع وبدون RIC خطوة مهمة. في المستقبل، قد تساعد مثل هذه المؤشرات الأطباء على معرفة ما إذا كان RIC "مفعّلا" بسرعة لدى مريض معين، وتوجيه قرار من ينبغي أن يتلقاه، أو حتى إلهام علاجات دوائية تحاكي تأثيراته المفيدة دون الحاجة للكفة. في الوقت الراهن، يعزز هذا العمل فكرة بسيطة لكنها قوية: عبر إجهاد جزء من الجسم بأمان، قد نتمكن من دفع الدماغ إلى حالة أكثر مرونة وقابلية للشفاء بعد السكتة.
الاستشهاد: Cui, Y., Liu, F., Cai, JR. et al. Quantitative proteomic analysis of plasma after remote ischemic conditioning in acute ischemic stroke. Sci Rep 16, 6106 (2026). https://doi.org/10.1038/s41598-026-36968-3
الكلمات المفتاحية: السكتة الإقفارية الحادة, التكييف الإقفاري البعيد, مؤشرات حيوية في المصل, التحليل البروتيومي, الحماية العصبية