Clear Sky Science · ar
تُسهم فئة مُعدية من العدلات في إصابة الأمعاء بنقص التروية وإعادة التروية عبر مسار إجهاد الشبكة الباطنية المُدار بواسطة ATF4
عندما يؤذي تدفّق الدم الأمعاء
لطالما حيّر الجراحون وأطباء العناية المركزة مفارقة خطيرة: عند انقطاع إمداد الدم للأمعاء ثم استعادته، يمكن أن يؤدي فعل استعادة التدفق نفسه إلى إتلاف شديد لبطانة الأمعاء. تُعرف هذه العملية باسم إصابة الأمعاء بنقص التروية–إعادة التروية، وقد تؤدي إلى مضاعفات مهددة للحياة مثل الإنتان وفشل العديد من الأعضاء. تكشف الدراسة الملخصة هنا أن ليس كل الخلايا المناعية المتسارعة إلى الموقع متساوية—فأحد الفئات الشديدة العدوانية من خلايا الدم البيضاء يلعب دور البطولة في تحويل استجابة تُنقذ الحياة إلى استجابة ضارة.
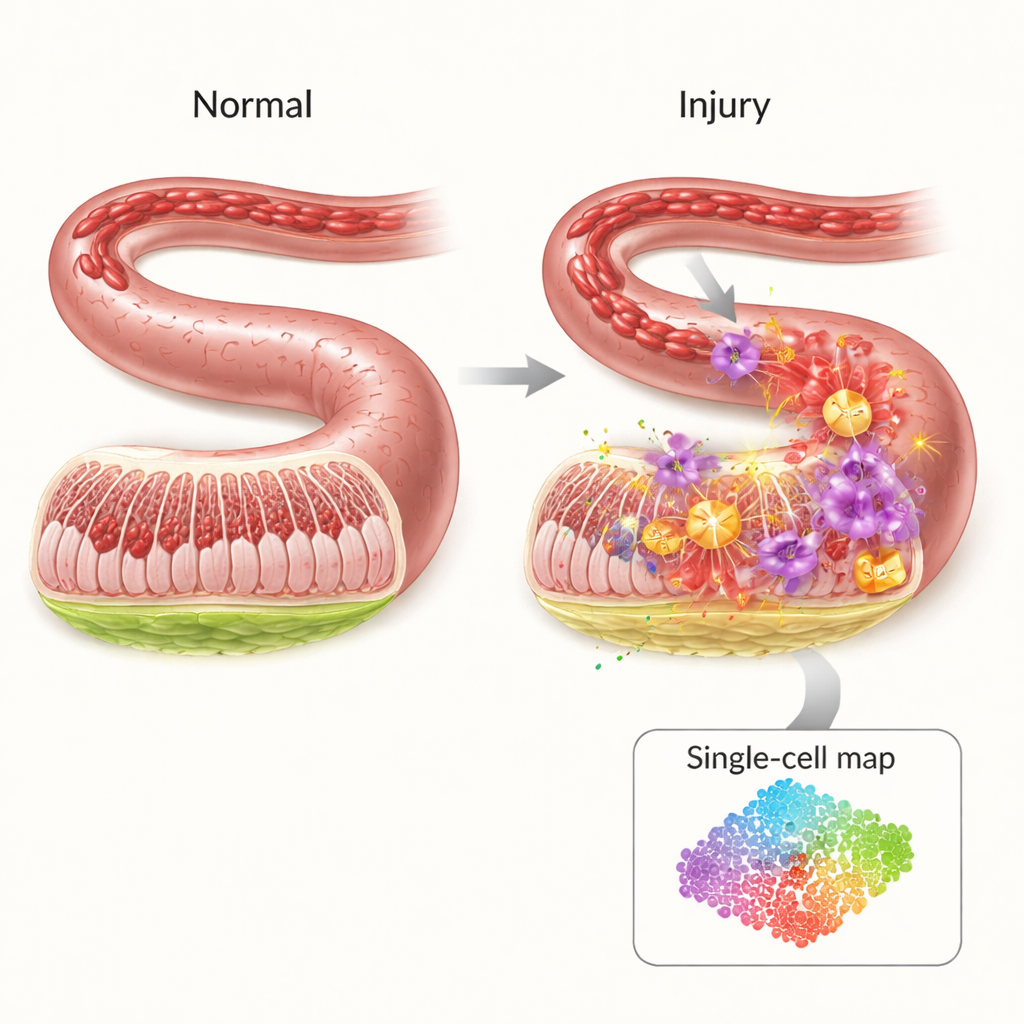
الجدار الواقي الهش للأمعاء
يُبطّن داخل الأمعاء حاجز رقيق لكنه منظم للغاية يحجز البكتيريا والسموم داخل القناة المعوية بينما يسمح بمرور المغذيات. عندما يتوقف تدفّق الدم—مثلما يحدث خلال الصدمة أو العمليات الجراحية الكبرى أو الإصابات الشديدة—يفتقر هذا الحاجز إلى الأكسجين. من المدهش أن معظم الضرر لا يحدث أثناء انقطاع التروية ذاته بل عند عودة الدورة الدموية. الانفجار المفاجئ للأكسجين والخلايا المناعية يطلق عاصفة من الإشارات الالتهابية والجزيئات التفاعلية التي يمكن أن تفتح ثقوباً في جدار الأمعاء، ما يسمح بدخول الجراثيم إلى مجرى الدم. على الرغم من أهميتها السريرية، فإن الأطباء يفتقرون اليوم إلى علاجات موجهة فعالة لمنع هذا التسلسل.
التقريب إلى مستوى الخلايا المفردة
لكشف من يقوم بماذا خلال هذه الأزمة، استخدم الباحثون تقنية تسلسل الرنا المفرد الخلوي، وهي تقنية تقرأ أي الجينات نشطة في آلاف الخلايا الفردية دفعة واحدة. في نموذج فأري لإصابة الأمعاء بنقص التروية–إعادة التروية، قارنوا الأمعاء المصابة بالأمعاء السليمة ورسموا خريطة تضم 19 نوع خَلَوي رئيسي. وجدوا أن خلايا مناعية معينة—وخاصة العدلات والوحيدات الالتهابية—توسعت بشكل كبير بعد الإصابة، بينما انخفضت الخلايا الوقائية مثل الخلايا التائية والخلايا البائية والخلايا القاتلة الطبيعية. تغيّرت أيضاً شبكات التواصل بين أنواع الخلايا، فبرزت العدلات كمحاور مركزية تبعث وتتلقى العديد من الإشارات الالتهابية، مما يشير إلى دورها المحوري في إحداث الضرر.
فئة ضارة من الخلايا المستجيبة الأولى
تعد العدلات من أسرع الخلايا المستجيبة في الجسم، تسارع عبر مجرى الدم لمواجهة العدوى وإزالة الحطام. لكن تُظهر هذه الدراسة أنه داخل مجتمع العدلات توجد فئة أكثر عدوانية مسؤولة عن قدر كبير من الضرر الجانبي في الأمعاء. عندما قلّص العلماء العدلات في الفئران قبل إحداث نقص التروية–إعادة التروية، أظهرت الحيوانات قِصَرَاً أقل في طول الأمعاء، وانخفاض مستويات مؤشرات الإصابة في الدم، ومظهر نسيجي أفضل تحت المجهر، وبروتينات ربط في البطانة المعوية أكثر إحكاماً. في تجارب التعايش الخلوي، أضرت العدلات المأخوذة من فئران مصابة مباشرة بالخلايا المعوية، فقلّلت من بقائها، وزادت موت الخلايا، وأعاقت بروتينات «السحّاب» الأساسية التي تحافظ على سلامة الحاجز المعوي.
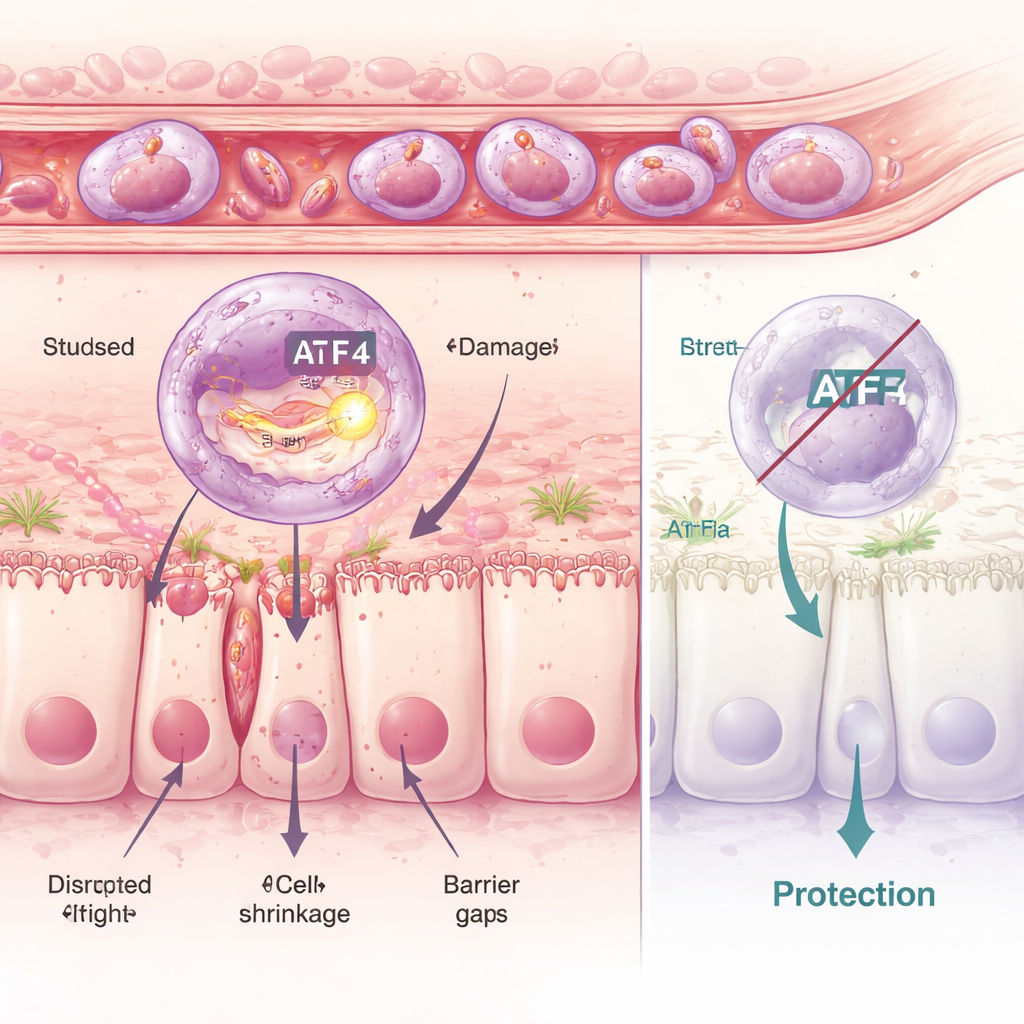
الإجهاد داخل الخلايا: عندما يفشل ضبط الجودة
بتعمق أكبر، فحص الباحثون العدلات خلية بخلية وحدّدوا ست فئات مميزة. برزت واحدة، سُميت مجموعة C5، بملف التهابي قوي وبنشاط برنامج جزيئي للإجهاد داخل بنية تُدعى الشبكة الباطنية، وهي ورشة طي البروتين داخل الخلية. من الضوابط الرئيسية لهذا البرنامج بروتين يُدعى ATF4. في خلايا C5 الضارة كان ATF4 وجينات هدفه نشطين بدرجة عالية. من خلال استعمال أدوية تُعزّز أو تكبّح هذه الاستجابة الداخلية للإجهاد، أظهر الفريق أن زيادة الإجهاد تعني ضرراً معوياً أكبر، بينما كبحه يحافظ على الحاجز المعوي. كانت الفئران المُهندسة وراثياً لعدم وجود ATF4 محمية إلى حد كبير: حتى عند إعطاء أدوية محرضة للإجهاد، لم تعد عدلاتها قادرة على تنفيذ برنامجها الضار بالكامل، وبقيت بطانة الأمعاء أكثر سلامة بكثير.
ماذا يعني هذا للعلاجات المستقبلية
معاً ترسم هذه النتائج صورة واضحة لغير المتخصصين: من بين سيل الخلايا المناعية التي تغمر الأمعاء عند عودة تدفّق الدم، هناك فئة محددة من العدلات المهيأة بالإجهاد تعمل كطاقم تنظيف مفرط الحماس يهدّم المبنى مع الحطام. تعتمد قوتهم التدميرية على مسار إجهاد داخلي يتحكم به ATF4 داخل الخلايا. خفض فعالية هذا المسار—دون القضاء على كل العدلات—قد يوفر وسيلة لحماية الأمعاء خلال أحداث عالية الخطورة مثل الجراحة الكبرى أو العدوى الشديدة أو الإصابات. ومع أن ثمة حاجة لمزيد من العمل لتأكيد هذه النتائج في البشر وللعثور على أدوية آمنة ومحددة، تفتح الدراسة طريقاً واعداً نحو علاجات تحافظ على سلامة الحاجز المعوي عندما يكون المرضى في أمس الحاجة إليها.
الاستشهاد: Yang, Y., Zhou, Q., Liu, S. et al. A pro-inflammatory neutrophil subpopulation drives intestinal ischemia–reperfusion injury via the ATF4-mediated endoplasmic reticulum stress pathway. Sci Rep 16, 6117 (2026). https://doi.org/10.1038/s41598-026-36938-9
الكلمات المفتاحية: الحاجز المعوي, نقص تروية وإعادة تروية, العدلات, إجهاد الشبكة الباطنية, ATF4