Clear Sky Science · ar
يكشف التمثيل الميتا-ديناميكي تثبيتًا تَبْيُنيًا بوساطة اللوتيولين ضد مقاومة أفابريتينيب لطفرة PDGFRα D842V/G680R في أورام GIST
لماذا هذا مهم لعلاج السرطان
يمكن أن تعمل الأدوية المستهدفة بشكل مذهل — حتى تطوّر الأورام وسائل للهروب منها. تستكشف هذه المقالة كيف قد يساعد مركب نباتي شائع، اللوتيولين، في استعادة فعالية دواء مهم يُستخدم ضد أنواع معينة من أورام اللحمة المعوية (GIST)، وهو نوع من السرطان في الجهاز الهضمي. باستخدام محاكاة حاسوبية متقدمة، يبيّن الباحثون كيف يمكن للوتيولين أن يثبّت بروتينًا مشوّهًا في خلايا السرطان بحيث يستطيع الدواء الحالي الارتباط به مجددًا، مما يشير إلى طريق جديد لمكافحة مقاومة الأدوية دون إعادة اختراع العلاج من الأساس. 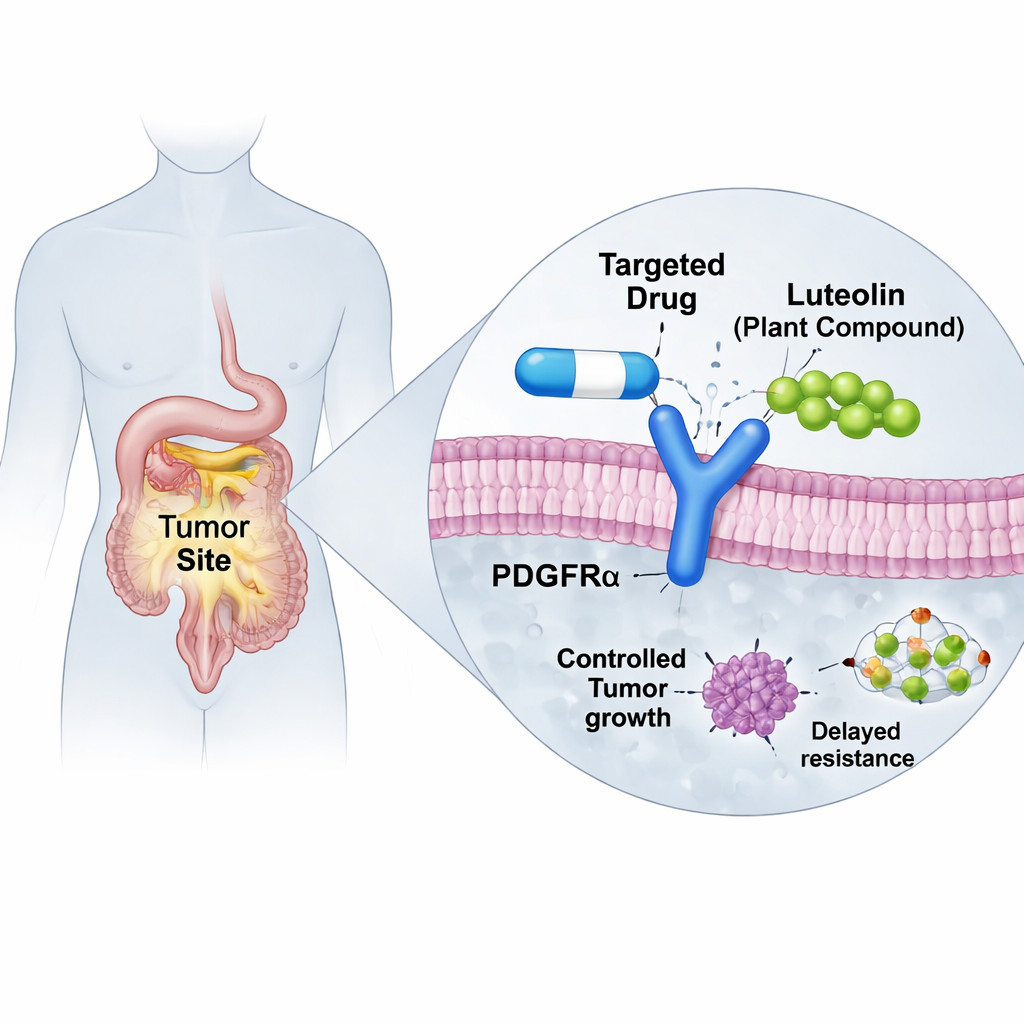
مشكلة الأورام التي تتعلّم التفادِي
تنمو أورام GIST غالبًا بسبب خلل في «مفاتيح التشغيل» الموجودة على سطح الخلايا والمعروفة باسم KIT أو PDGFRα، والتي تطلق إشارات نمو مستمرة. صُمِّمت الأدوية الحديثة المسماة مثبطات التايروسين كيناز لإيقاف هذه المفاتيح وقد غيّرت نتائج الكثير من المرضى. لكن طفرة شائعة في PDGFRα تسمى D842V تجعل الدواء القديم إيماتينيب غير فعال إلى حد كبير. صُمّم دواء أحدث، أفابريتينيب، خصيصًا للتعامل مع هذا الطفرة العنيدة وأظهر نجاحًا لافتًا في التجارب السريرية. ومع ذلك، يمكن للأورام أن تتكيف مجددًا. يطوّر بعض المرضى تغيرات إضافية في PDGFRα، مثل طفرة ثانوية G680R، التي تحجب فعليًا مقعد ارتباط أفابريتينيب فتدفعه للخروج ويزداد مستوى المقاومة.
جزيء نباتي ذو شكل مثير للاهتمام
المواد الطبيعية مصدر غني لأفكار دوائية، والمعادن الفلافونويدية — مركبات ملونة موجودة في العديد من الفواكه والخضراوات والنباتات الطبية — معروفة بتفاعلها مع بروتينات التحكم بالنمو داخل الخلايا. اللوتيولين، أحد هذه الفلافونويدات الموجود في شجيرة متوسِّطية تُدعى Retama monosperma، دُرِس بالفعل لخصائصه المضادة للسرطان والمضادة للالتهاب ويبدو آمنًا عند مستويات يمكن تحقيقها عن طريق المكملات الفموية. استنادًا إلى أعمال غربلة سابقة، اشتبه المؤلفون أن اللوتيولين قد يلتصق بـ PDGFRα في موضع قريب لكن لا يتداخل مع موضع ارتباط الدواء المعتاد. وإذا كان ذلك صحيحًا، فقد يسمح اللوتيولين بالعمل كدعامة دقيقة، تدفع البروتين إلى شكل يرحب مرة أخرى بأفابريتينيب.
محاكاة شراكة جزيئية
لاختبار هذه الفكرة حاسوبيًا، بنى الفريق نماذج ثلاثية الأبعاد مفصّلة للبروتين المقاوم PDGFRα الحامل لكل من الطفرتين D842V وG680R. حاكوا سلوك أفابريتينيب بمفرده وكيف تصرّف عندما وُجد اللوتيولين قريبًا، متتبعين حركات الذرات عبر مئات النانوسواندات — أي مليارات الأجزاء من الثانية في الزمن الحقيقي. عندما كان أفابريتينيب مرتبطًا بمفرده، انجرف الدواء تدريجيًا خارج جيبه بسبب دفع التغير الكبير G680R له، وانتهى به المطاف منفصلًا تمامًا عن البروتين. بالمقابل، عندما كان اللوتيولين مرتبطًا أيضًا في موضع «كلوستيري» منفصل بجانب حلزون رئيسي، بقي أفابريتينيب إلى حد كبير في مكانه. تقلّصت مرونة البروتين ككل، وحافظت المقاطع البنائية الرئيسية على شكلها، واستمرّت الاتصالات المهمة بين الدواء والبروتين لفترة أطول بكثير. 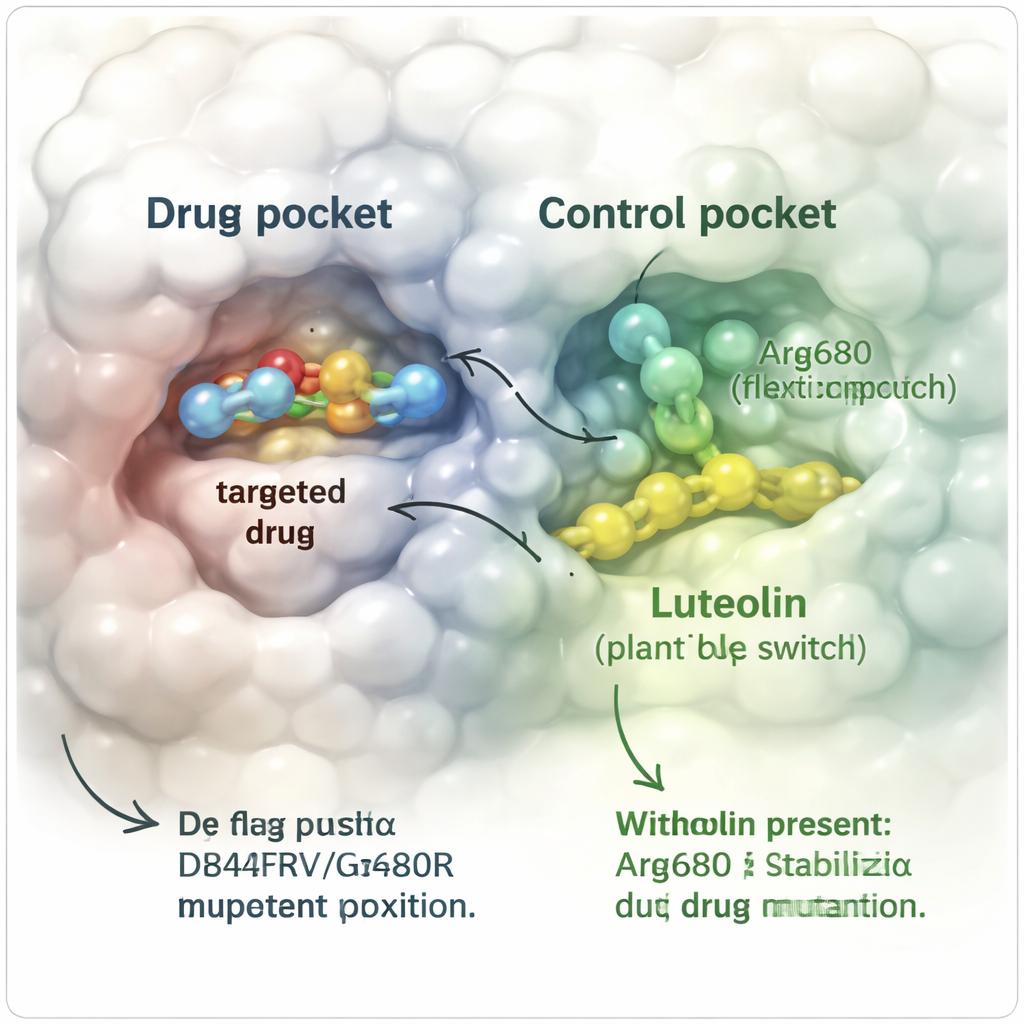
تثبيت مفتاح جزيئي هارب
لا تلتقط المحاكاة القياسية دائمًا التغيرات النادرة لكنها المهمة في الشكل، لذا لجأ الباحثون إلى نهج معزز يُدعى الميتا-ديناميكس لاستكشاف كيف قد يلتف البروتين وينثني بشكل أكثر شمولًا. ركّزوا على سلوك الحمض الأميني المعدّل أرجينين 680 (Arg680)، الذي يتصرف كذراع صغيرة مرنة بالقرب من جيب الدواء. بدون اللوتيولين، جال هذا الذراع في مواضع متعددة وانزلق الدواء بسهولة بعيدًا، مع حواجز طاقة منخفضة نسبيًا للهروب. مع وجود اللوتيولين في مكانه، احتُفظ بـ Arg680 في اتجاه محدد لم يعد يتصادم مع الدواء. تغيّر مشهد الطاقة: أصبح النظام يفضّل تراكيب تبقى فيها أفابريتينيب مرتبطًا، وارتفع "التل" الطاقي الذي ينبغي على الدواء تسلُّقه للانفصال بعدة كيلو كالوريات، ما جعل التفتت أقل احتمالًا بكثير.
ما الذي قد يعنيه هذا للمرضى
بعبارات بسيطة، تشير الدراسة إلى أن اللوتيولين قد يعمل كجبيرة جزيئية، يثبّت بروتين السرطان المشوّه بحيث يتمكن قرص مستهدف قائم من إمساكه مجددًا. بدل تصميم دواء جديد تمامًا لكل طفرة مقاومة، قد يعيد اقتران الدواء الحالي مع مركب مساعد مختار بعناية فعاليته. العمل يعتمد على طرق حاسوبية قوية لكنها بحتة، لذا لا بد من دراسات مخبرية وحيوانية للتأكد مما إذا كان اللوتيولين، أو جزيء ذو صلة معدّل لخصائص دوائية أفضل، يعزّز فعليًا أفابريتينيب في أنظمة حية. ومع ذلك، قد يفتح مفهوم استخدام مساعدين كلوسيتريين صغار لإعادة استقرار الأهداف المقاومة للسرطان مسارًا جديدًا لإطالة عمر علاجات الدقة الحالية.
الاستشهاد: El Khattabi, K., Akachar, J., Lemriss, S. et al. Metadynamics reveals luteolin-mediated conformational stabilization against avapritinib-resistant PDGFRα D842V/G680R GIST. Sci Rep 16, 6534 (2026). https://doi.org/10.1038/s41598-026-36898-0
الكلمات المفتاحية: مقاومة الأدوية, ورم اللحمة المعوي, مثبطات تايروسين كيناز, لوتيولين, تعديل كلوسيتري