Clear Sky Science · ar
تقييم تجريبي ونظري لتحمُّل الدوكسوروبيسين على جسيمات أكسيد السيريوم اعتمادًا على الشكل عبر نمذجة قوى فان دير فال
لماذا يهم شكل حوامل الأدوية الصغيرة
أدوية السرطان مثل الدوكسوروبيسين قوية لكنها قد تضر الأنسجة السليمة. إحدى الاستراتيجيات لجعلها أكثر أمانًا هي ربطها بجسيمات نانوية تنقل الدواء مباشرة إلى الأورام. تطرح هذه الدراسة سؤالًا بسيطًا لكن ذي نتائج بعيدة المدى: هل يغيّر شكل الجسيم النانوي—سواء كان كرويًا أو عصويًا أو صفائحيًا—كمية الدواء التي يمكنه حملها ومدى فعاليته؟
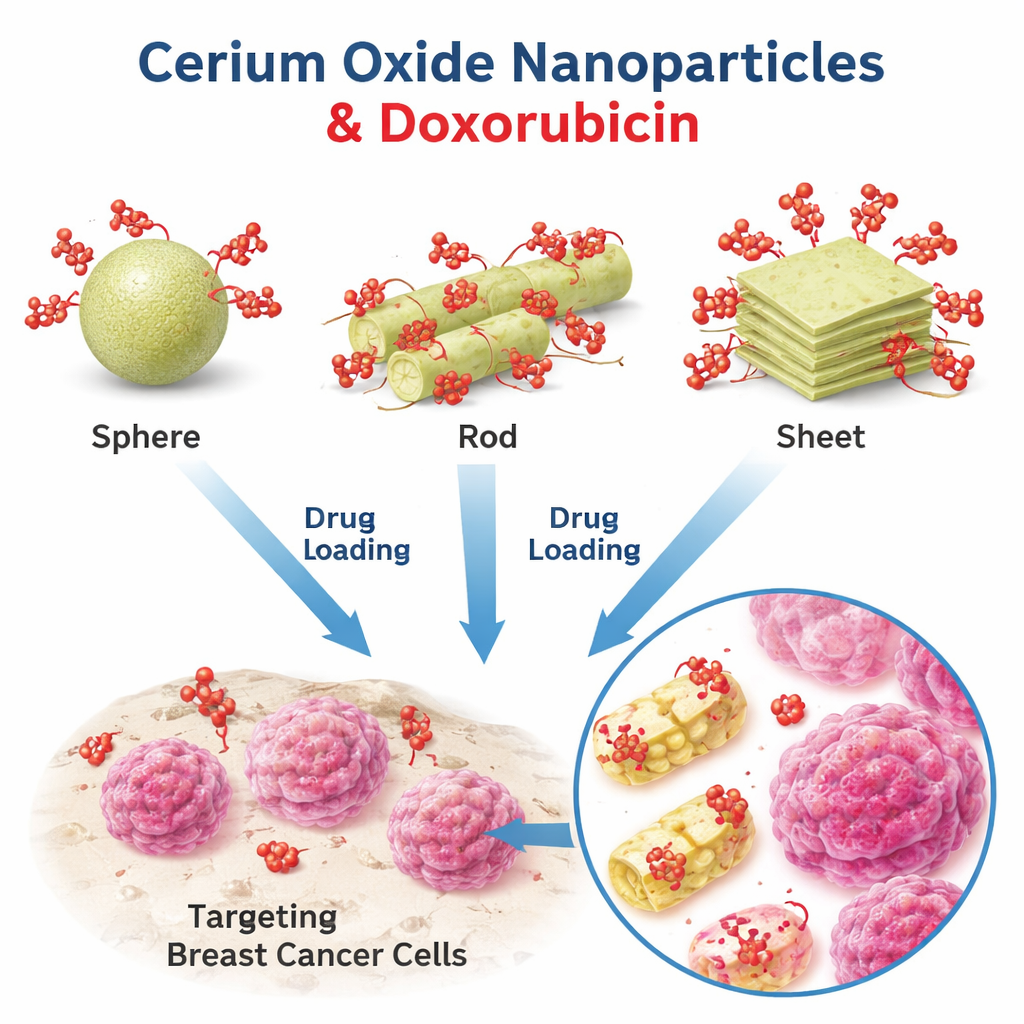
ثلاثة أشكال صغيرة ودواء واحد للسرطان
ركز الباحثون على جسيمات نانوية من أكسيد السيريوم، مادة معروفة بالفعل بخصائصها المضادة للأكسدة والمضادة للبكتيريا والمساهمة في التئام الجروح، واستكشفوا إمكانيتها كحامل للدوكسوروبيسين، وهو دواء كيميائي مستخدم على نطاق واسع. حضّروا ثلاثة أشكال مميزة من أكسيد السيريوم: كرات تقريبًا متقاربة الشكل، أسطوانات عصوية، وصفائح رقيقة شبيهة بالرقائق. باستخدام مجاهر إلكترونية وقياسات تشتت الضوء، أكدوا أحجام وشكل الجسيمات، حيث شكلت الكرات خرزات مدمجة، وظهرت الأسطوانات كعصي نحيلة، وكانت الصفائح طبقات عريضة ومسطحة. سمح لهم هذا الطقم المسيطر عليه من الأشكال بالتحقق من تأثير الهندسة وحدها على سلوك الدواء مع إبقاء المادة نفسها ثابتة.
قياس مقدار الدواء الذي تحمله كل شكل
لمعرفة مدى فعالية كل شكل في حمل الدوكسوروبيسين، خلط الفريق الجسيمات النانوية مع محلول الدواء ثم قاسوا كمية الدواء المتبقية في السائل بعد ذلك. كلما قلّ الدواء المتبقي، زاد ما تم تحميله على الجسيمات. باستخدام طرق ضوئية دقيقة (مطيافية فوق بنفسجية–مرئية والفلورية)، وجدوا أن الجسيمات الكروية امتصت أكبر كمية من الدوكسوروبيسين، حيث انتهى المطاف بحوالي 86% من الدواء على أو داخل الكرات. تلتها الأسطوانات بنحو 79%، والصفائح بحوالي 67%. عند اختبار هذه الجسيمات المحمّلة بالدواء ضد سلالة خلوية عدوانية من سرطان الثدي، كانت التركيبة القائمة على الكرات هي الأكثر فعالية في قتل الخلايا السرطانية، تلتها الأسطوانات ثم الصفائح. ومن المثير للاهتمام أن الكرات أظهرت أيضًا إطلاقًا أبطأ للدواء مع مرور الوقت، مما يوحي بأن التحميل العالي مع إطلاق بطيء قد يعزز تأثير الدواء داخل الخلايا.
تطبيق الرياضيات على العالم النانوي
بالتوازي مع العمل المختبري، بنى الباحثون نموذجًا تحليليًا—نوع من المجهر الرياضي المبسّط—لحساب مدى التصاق جزيء دوكسوروبيسين مفرد تقريبًا كروي الشكل بكل شكل من أشكال الجسيمات. ركزوا على قوى فان دير فال، وهي التجاذبات الضعيفة الشائعة التي تساعد الجزيئات على الالتصاق ببعضها. من خلال معاملة الدواء ككرة صغيرة قريبة من سطح أكسيد سيريوم كروي أو أسطواني أو صفائحي، اشتقّوا صيَغا دقيقة لطاقة التفاعل أثناء اقتراب الدواء أو ابتعاده. سمحت لهم هذه الحسابات بالتنبؤ بالشكل الذي ينبغي أن يمنح الربط الأكثر استقرارًا، سواء عندما يكون الدواء مدفونًا داخل الجسيم أو عندما يكون جالسًا على السطح، دون الحاجة لتشغيل محاكيات حاسوبية ضخمة.
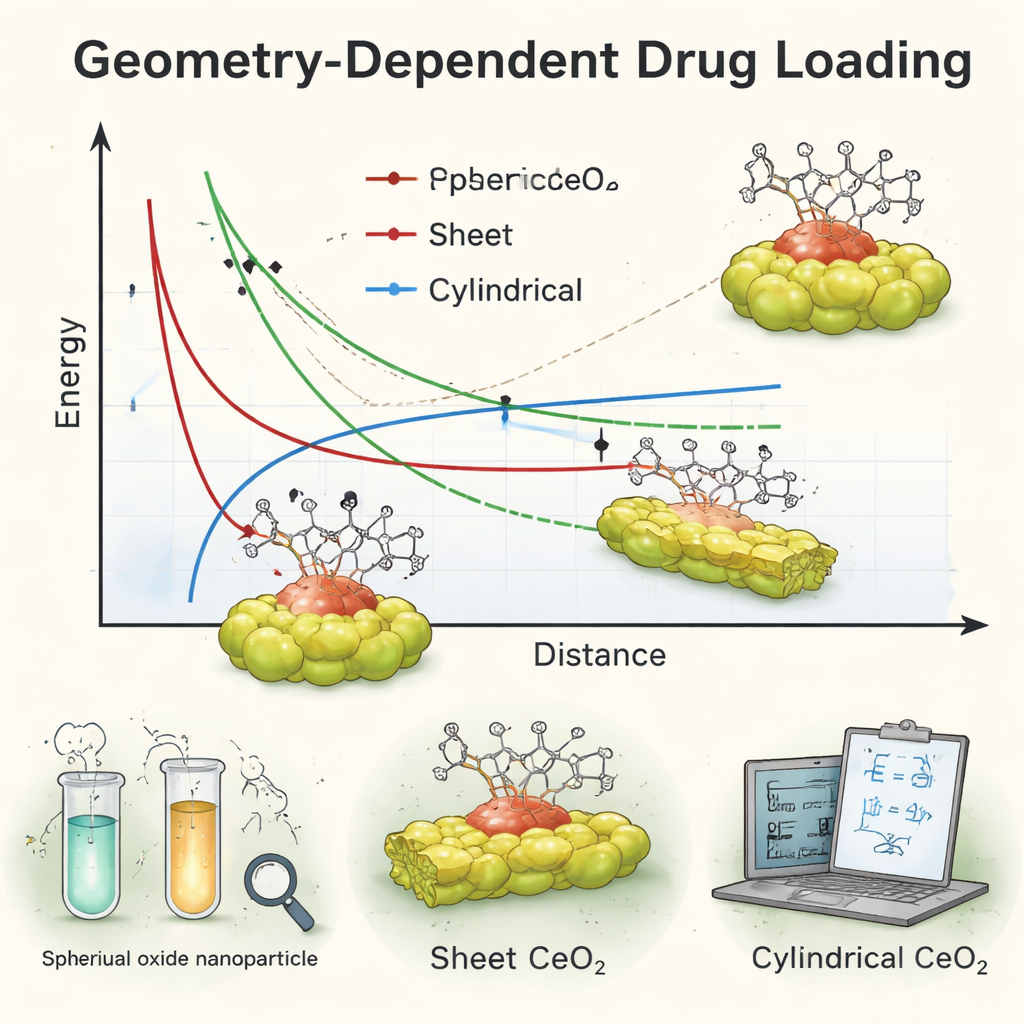
أين تتفق النظرية—وأين تنهار
عندما قارن الفريق معادلاتهم بالبيانات التجريبية، وجدوا تطابقًا جزئيًا ملحوظًا. أشارت الرياضيات إلى أن الجسيمات الكروية والصفائحية ينبغي أن تحتفظ بالدوكسوروبيسين بقوى ربط متشابهة جدًا، وهو ما تناسب مع التحميل العالي الذي لوحظ عمومًا لهاتين الحالتين. علاوة على ذلك، حين افترضوا أن الدواء محبوس داخل الجسيمات، خرجت الكرات كأكثر استقرارًا قليلًا من الأشكال الأخرى، مما ينعكس في الأداء القوي لحوامل الكرات في المختبر. لكن كانت هناك مفاجأة: تنبأ النموذج بوجود ربط أضعف نسبيًا للأسطوانات، بينما أظهرت التجارب أن الجسيمات ذات الشكل العصوي لا تزال تحمل الدواء بكفاءة كبيرة—قريبة تقريبًا من الكرات. هذا التباين، لا سيما بالنسبة للشكل الأسطواني، كشف أن نموذجًا بسيطًا يعامل الوسط المحيط كفضاء فارغًا ويعمم تفاصيل السطح لا يمكنه أن يلتقط سلوك أنظمة الدواء–الجسيم النانوي في الواقع، حيث تكون هذه الأنظمة في محاليل وتتعامل مع خلايا حية.
ماذا يعني هذا لعلاجات السرطان المستقبلية
لغير المتخصصين، الرسالة ذات شقين. أولًا، شكل الجسيم النانوي ليس تفصيلًا تجميليًا؛ فهو يؤثر مباشرةً في كمية الدواء السرطاني التي يمكنه حملها، ومعدل إطلاقه، وقوة تأثيره على الخلايا الورمية. برزت جسيمات أكسيد السيريوم الكروية في هذه الدراسة كحاملات واعدة للدوكسوروبيسين، مدمجةً تحميلًا عاليًا، وقتلًا قويًا للخلايا السرطانية، وتسربًا بطيئًا للدواء. ثانيًا، تظهر الدراسة حدود النماذج الرياضية حتى عندما تكون أنيقة، إذا ما بالغت في تبسيط الواقع الفوضوي للبيولوجيا. لصياغة أدوية نانوية موثوقة حقًا، سيحتاج العمل المستقبلي إلى مزج تجارب مفصلة مع نظريات أكثر تطورًا تشمل الوسط المائي وواجهات جزيئية معقدة وتجمعات الجسيمات. معًا، قد تؤدي هذه التقدّمات إلى تصميمات جسيمات نانوية أذكى توصل أدوية قوية بأمان وفعالية أكبر.
الاستشهاد: Sripaturad, P., Keo, S., Wongpan, A. et al. Experimental and theoretical evaluation of geometry-dependent doxorubicin loading onto cerium oxide nanoparticles via van der Waals interaction modeling. Sci Rep 16, 6169 (2026). https://doi.org/10.1038/s41598-026-36893-5
الكلمات المفتاحية: الطب النانوي, جسيمات أكسيد السيريوم النانوية, توصيل الدوكسوروبيسين, هندسة الجسيمات النانوية, علاج سرطان الثدي