Clear Sky Science · ar
يعدّل YTHDC1 الطراز الخبيث لسرطان الشبكية عبر التحلّل الذاتي المتوسط بواسطة SQSTM1
لماذا يهم هذا سرطان عيون الأطفال
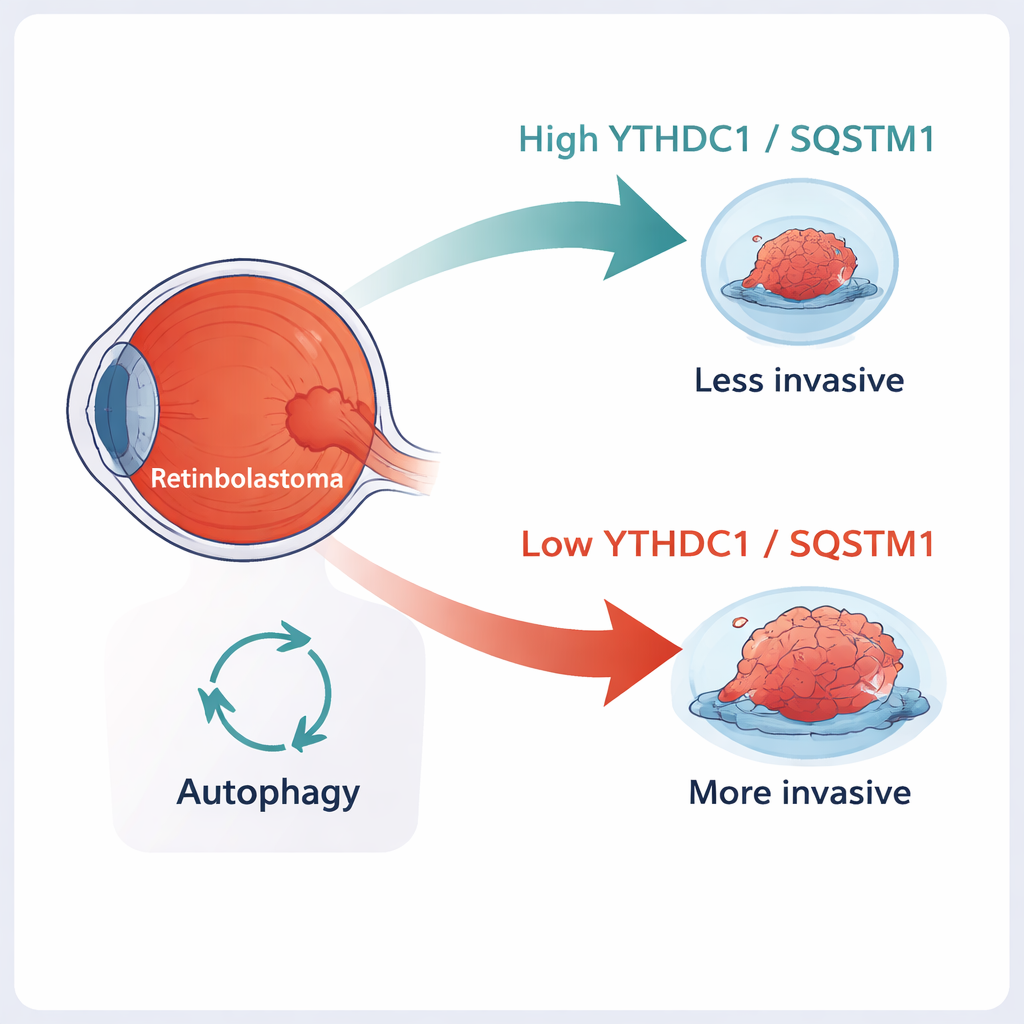
سرطان الشبكية هو أكثر أنواع سرطانات العين شيوعاً لدى الأطفال الصغار. في كثير من الحالات يمكن للأطباء علاجه إذا تم اكتشافه مبكراً، لكن عندما يبدأ الورم في غزو الأنسجة المحيطة بالعين أو الانتشار باتجاه الدماغ، يصبح إنقاذ حياة الطفل ورؤيته أصعب بكثير. تستكشف هذه الدراسة «مكبحاً» جزيئياً داخل خلايا الورم — جزيئان يسميان YTHDC1 وSQSTM1 — يبدو أنهما يساعدان على إبقاء سرطان الشبكية أقل عدوانية. فهم كيفية عمل هذا المكبح قد يفتح طرقاً جديدة لعلاجات أكثر استهدافاً وأقل قسوة.
نظرة أقرب على أورام عيون الأطفال
ينشأ سرطان الشبكية من طبقة شبكية العين الحاسة للضوء، وعادةً ما يحدث لدى الأطفال دون سن الخامسة. تقليدياً، تبدأ الحالة عندما تُفقد النسختان من جين الحراسة RB1. لكن فقدان RB1 وحده لا يفسر تماماً لماذا تبقى بعض الأورام محصورة داخل العين بينما يحفر البعض الآخر في الأنسجة المجاورة أو ينتشر على طول العصب البصري. أدرك الباحثون بشكل متزايد أن العلامات الكيميائية المضافة إلى الرنا (الرسائل المؤقتة التي تخبر الخلية أي بروتينات تصنع) يمكن أن تؤثر بشدة في سلوك السرطان. إحدى أكثر هذه العلامات شيوعاً تُسمى m6A، ويمكنها تغيير مدى استقرار هذه الرسائل ومدة بقائها داخل الخلية.
اكتشاف مكبح جزيئي مفقود
بدأ المؤلفون بمقارنة النشاط الجيني في الأورام التي بقيت داخل العين مع تلك التي أصبحت غازية بالفعل. باستخدام مجموعة بيانات تسلسل رنا عامة من عينات سرطان الشبكية، حددوا آلاف الجينات التي اختلف نشاطها بين المجموعتين ثم ركزوا على «منظمي» m6A الرئيسيين. يشمل هؤلاء إنزيمات تضيف أو تزيل m6A وبروتينات «قارئة» تفسر العلامة. من بين عشرة منظمين رئيسيين، وجدوا أن قارئاً واحداً، YTHDC1، كان أقل باستمرار في الأورام الغازية. عندما فحصوا عينات من 50 طفلًا وأجروا اختبارات مخبرية على نسيج الورم، أكدوا أن مستويات YTHDC1 — سواء على مستوى الرنا أو البروتين — كانت منخفضة في السرطانات الأكثر عدوانية.
اختبار دور YTHDC1
للتحقق مما يفعله YTHDC1 فعلياً، تلاعب الفريق بمستوياته في سطرين خلويين بشريين لسرطان الشبكية. عندما خفضوا YTHDC1 باستخدام أدوات جينية، تكاثرت الخلايا بسرعة أكبر وأصبحت أكثر قدرة على المرور عبر أغشية صناعية تحاكي الحواجز النسيجية — وهي علامات على ورم أكثر غزوًا. في الفئران، شكلت الخلايا التي تفتقر إلى YTHDC1 أوراماً أكبر وأثقل. والعكس صحيح أيضاً: إجبار الخلايا على إنتاج YTHDC1 إضافي أبطأ نموها وقلل من قدرتها على الهجرة والغزو. تشير هذه التجارب إلى أن YTHDC1 يعمل كمثبط للورم، يساعد في كبح أشرس سلوكيات سرطان الشبكية.
كيف يسيطر YTHDC1 على نظام إعادة التدوير الخلوي
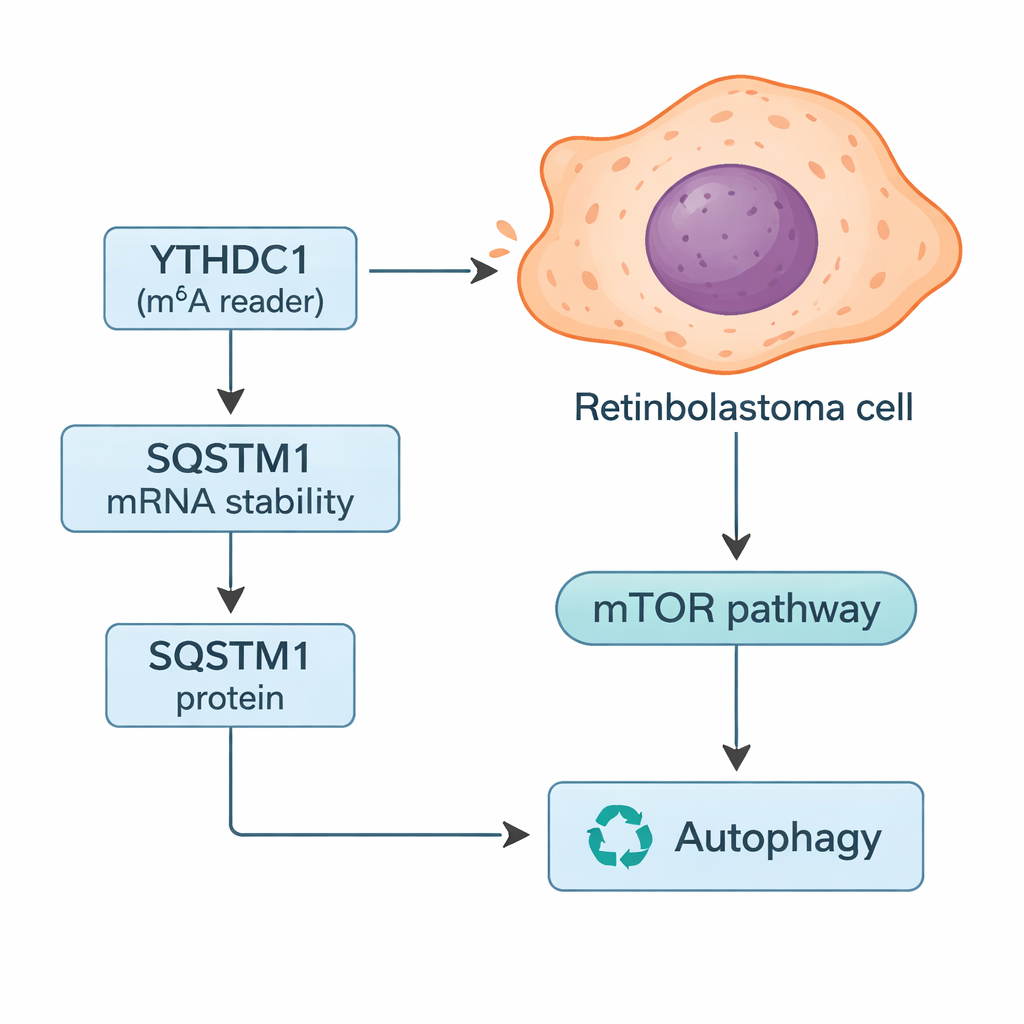
بتعمق أكثر، بحث الباحثون عن جينات محددة قد تُسيطر رسائلها بواسطة YTHDC1. من خلال دمج عمليات بحث في قواعد البيانات مع بياناتهم الطلبية، ركزوا على SQSTM1، وهو بروتين يُعرف أيضاً باسم p62. يساعد SQSTM1 في تنظيم التحلل الذاتي، نظام إعادة التدوير الخلوي الذي يكسر المكونات التالفة ويمكن أن يوفر وقوداً عندما تكون الموارد نادرة. أظهرت الدراسة أن YTHDC1 يرتبط فعلياً برنا SQSTM1 ويثبّته، مما يسمح بإنتاج كمية أكبر من بروتين SQSTM1. عندما انخفض YTHDC1، انخفضت مستويات SQSTM1 وتلاشى رناها أسرع. أدى إسكات SQSTM1 بمفرده إلى جعل خلايا سرطان الشبكية تنمو وتغزو أكثر، وطمس جزئياً التأثيرات الوقائية التي شوهدت عند إفراط إنتاج YTHDC1، مما يضع SQSTM1 كوسيط رئيسي في هذا المسار.
التحلل الذاتي، الطاقة، وعدوانية الورم
لأن SQSTM1 مركزي في التحلل الذاتي، اختبر الفريق كيف غيّر تعديل YTHDC1 وSQSTM1 هذا العملية. باستخدام مزيج من العلامات الفلورية وقياسات البروتين، وجدوا أن خفض أي من YTHDC1 أو SQSTM1 عزز «تيار» التحلل الذاتي — أي أن مزيداً من المواد الخلوية تُنقل إلى نظام إعادة التدوير وتُعالج خلاله. ولاحظوا أيضاً تغييرات في مسار mTOR، المفتاح الحساس للمغذيات الذي يثبّت عادةً التحلل الذاتي. مع انخفاض SQSTM1، انخفض نشاط mTOR، وهو ما يتوافق مع زيادة التحلل الذاتي. يقترح المؤلفون أنه في سرطان الشبكية الغازي يؤدي انخفاض YTHDC1 إلى إشارات SQSTM1 أضعف، ونشاط mTOR مخفّض، وتحلل ذاتي مرتفع يساعد خلايا الورم على تحمل الضغوط والانتشار.
ماذا يعني هذا للعلاجات المستقبلية
لغير المتخصصين، الخلاصة أن هذه الدراسة تحدد سلسلة من الأحداث داخل خلايا سرطان الشبكية — YTHDC1 الذي يتحكم في SQSTM1، والذي بدوره يشكل آلية إعادة التدوير الخلوية — تؤثر في مدى عدوانية السرطان. عندما تضعف هذه السلسلة، تنمو الأورام أسرع وتغزو أكثر. رغم أن هناك عملاً كثيراً قبل أن تصل هذه النتائج إلى العيادة، يقدم هذا المسار أفكاراً علاجية جديدة: استعادة وظيفة YTHDC1، تدعيم استقرار SQSTM1، أو تعديل التحلل الذاتي ونشاط mTOR قد يكمل يوماً ما العلاجات الكيميائية الحالية. للأطفال المصابين بهذا السرطان العيني قد تساعد مثل هذه الاستراتيجيات الموجّهة في الحد من انتشار الورم مع الحفاظ على رؤية أكبر وتقليل آثار العلاج الجانبية.
الاستشهاد: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
الكلمات المفتاحية: سرطان الشبكية, YTHDC1, SQSTM1, التحلل الذاتي, مسار mTOR