Clear Sky Science · ar
الإيريسين ينظم أيض الدهون والموت بالخرف (فرفوبتوز) في خلايا سرطان المبيض عبر تعديل محور ALOX5-5-HETE-PD-L1
لماذا تهم هذه الجزيئة النباتية في سرطان المبيض
يُعد سرطان المبيض من أشد الأورام فتكًا لدى النساء لأنه يُشخّص غالبًا في مراحل متأخرة ويعود في كثير من الحالات بعد العلاج. تستكشف هذه الدراسة ما إذا كان مركب طبيعي يُدعى تيكتوريجينين، الموجود في نبات Belamcanda chinensis، قادرًا على إبطاء سرطان المبيض عن طريق حرمان الخلايا الورمية من أنواع معينة من الدهون وإخضاعها لنوع خاص من الموت الخلوي المعتمد على الحديد. كما تفحص كيف قد يُضعف هذا المركب «عباءة الاختفاء» التي تستخدمها الأورام للاختباء من الجهاز المناعي.
مورد خفي للوقود داخل الخلايا الورمية
مثل كثير من السرطانات، تعيد أورام المبيض برمجة تعاملها مع الدهون. فبدلًا من استخدام الدهون للطاقة فقط، تخزنها الخلايا السرطانية كعناصر لبناء الأغشية الجديدة وكعوازل ضد التلف. في خلايا سرطان المبيض المزروعة مخبريًا، أدى إضافة أحماض دهنية أحادية غير مشبعة إلى تراكم الأحماض الدهنية الحرة والدهون الثلاثية والكوليسترول — وهي أشكال رئيسية من الدهون المخزنة. جعلت هذه الفائضة الدهنية الخلايا تنمو وتغزو بسهولة أكبر وساعدتها على مقاومة عملية هدّامة تُسمى الفرفوبتوز (الموت بالخرف)، حيث يتفاعل الحديد مع الدهون المؤكسدة لتمزيق أغشية الخلايا. بكلمات أخرى، منح الاختلال في أيض الدهون السرطان ميزة نمو ودروعًا للبقاء.
دفع الخلايا السرطانية نحو التدمير الذاتي
اختبر الباحثون بعد ذلك التيكتوريجينين على خلايا مبيض طبيعية وعلى عدة خطوط خلايا سرطان مبيض. عند جرعات تصل إلى 200 ميكروغرام لكل لتر، لم يضر المركب بالخلايا الطبيعية لكنه أبطأ نمو الخلايا السرطانية بوضوح، وخفض قدرتها على الغزو عبر غشاء، وزاد من معدل موتها المبرمج. عندما عُولجت الخلايا السرطانية مسبقًا بدواء يثبط الفرفوبتوز، أصبحت أكثر عدوانية. وأدى إضافة التيكتوريجينين إلى عكس هذه التأثيرات: انخفضت مخزونات الدهون، وارتفعت مؤشرات التلف المرتبطة بالحديد والأكسدة، وماتت خلايا أكثر. في نماذج فأرية تحمل أورامًا بشرية للمبيض، قلّصت حقن التيكتوريجينين أحجام الأورام، وخفّضت محتوى الدهون في أنسجة الورم، وعزّزت العلامات الكيميائية للفرفوبتوز، مما يشير مجددًا إلى أن المركب يدفع الخلايا السرطانية نحو هذا المسار الموتي المعتمد على الحديد.
مفتاح جزيئي يربط الدهون والهروب المناعي
لكشف كيفية عمل التيكتوريجينين على المستوى الجزيئي، جمع الفريق بين تنقيب البيانات واسع النطاق ونمذجة الحزم الدوائية لبروتينات الهدف. ركزوا على إنزيم يُدعى ALOX5، الذي يحول حمضًا دهنيًا شائعًا إلى جزيء إشاري يُدعى 5‑HETE. كانت مستويات ALOX5 في خلايا سرطان المبيض وعينات الأورام أعلى بكثير منها في الأنسجة الطبيعية. أظهرت محاكاة الاقتران الجزيئي والديناميكيات الجزيئية أن التيكتوريجينين يمكنه الارتباط بثبات بـ ALOX5، ليعمل كمكبح داخلي. عندما زاد الباحثون ALOX5 اصطناعيًا داخل الخلايا السرطانية، ارتفعت مخزونات الدهون، وانخفضت علامات الفرفوبتوز، وأصبحت الخلايا أكثر غزوًا. ألغت معالجة التيكتوريجينين هذه التغيرات. وكان تثبيط ALOX5 له التأثير المعاكس — دهون أقل، فرفوبتوز أكثر، ونمو أضعف — ما يضع هذا الإنزيم في مركز عمل المركب.
كيف تفقد الأورام درعها ضد الجهاز المناعي
ربطت الدراسة أيضًا هذا المسار الدهني بجزيء نقطة تفتيش مناعي مهم يُدعى PD‑L1، الذي تستخدمه الأورام لإيقاف خلايا الجهاز المناعي المهاجمة. عزّزَ ناتج ALOX5، 5‑HETE، مستويات PD‑L1، مما قوّى هذا الدرع. عندما تم كبت ALOX5، انخفض كل من 5‑HETE وPD‑L1؛ وعند إعادة إدخال 5‑HETE، ارتفعت مستويات PD‑L1 مجددًا واستعادت الخلايا بعض حمايتها من الفرفوبتوز. خفّض التيكتوريجينين ALOX5، وقلّل 5‑HETE، وبالتالي خفّض PD‑L1 في المزارع الخلوية وفي أورام الفئران. وتشير هذه النتائج إلى أنه باستهداف إنزيم أيضي واحد، يمكن للمركب أن يزعزع دفاعات السرطان المعتمدة على الدهون ويضعف أيضًا قدرته على الاختباء من الهجوم المناعي.
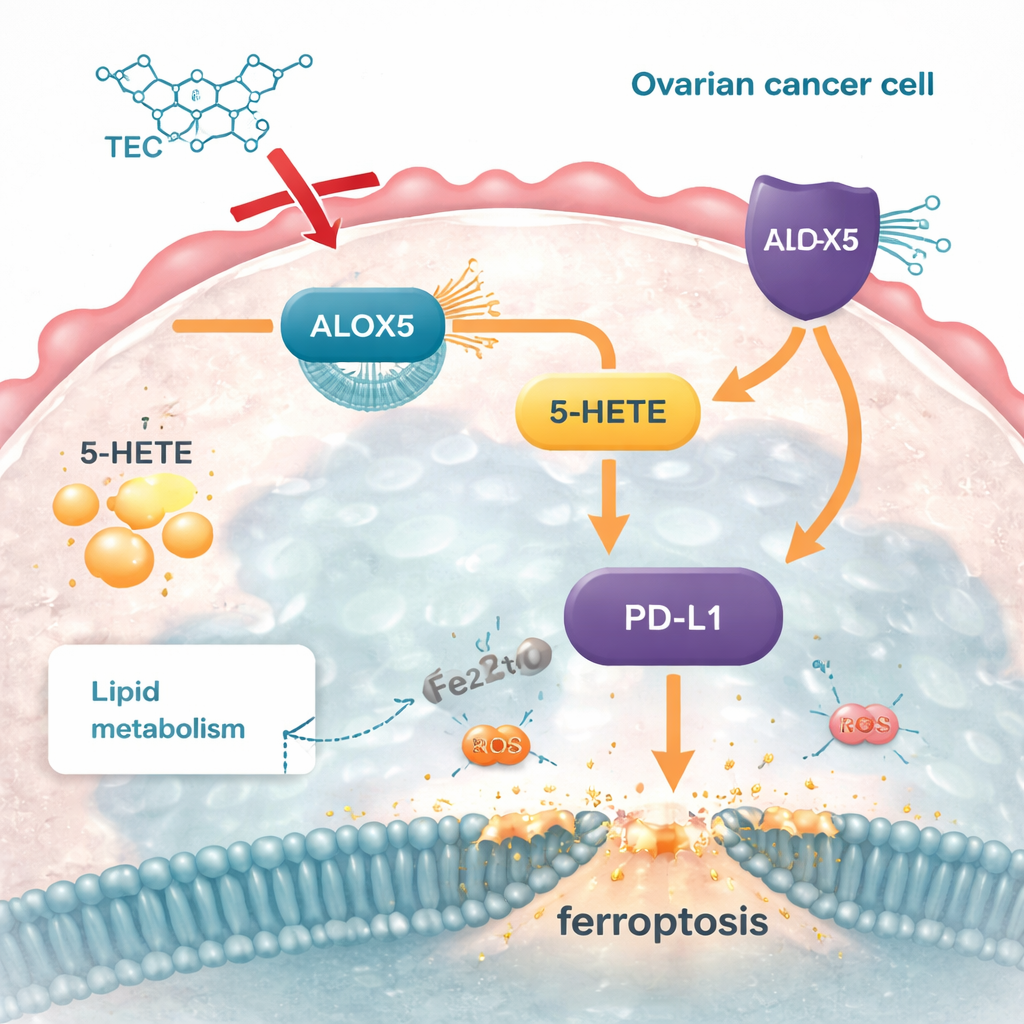
ما الذي قد يعنيه هذا للعلاجات المستقبلية
ببساطة، تُظهر هذه الدراسة أن التيكتوريجينين يعمل كأداة دقيقة تعطل آلية معالجة الدهون في الخلية السرطانية. عبر حجب ALOX5، يقطع إنتاج 5‑HETE، ويقلص مخزونات الدهون الزائدة، ويجعل الخلايا عرضة للتلف المعتمد على الحديد، ويكشف جزءًا من تمويهها المناعي. رغم أن هذه النتائج مستمدة من دراسات خلوية وفأرية — ولا يزال هناك الكثير لاختباره في البشر — فإنها تشير إلى استراتيجية واعدة: استهداف محور ALOX5–5‑HETE–PD‑L1 لتجويع أورام المبيض ولجعلها أكثر عرضة للقضاء عليها بواسطة دفاعات الجسم أو عبر علاجات مناعية مستقبلية.
الاستشهاد: Cai, H., Huang, C. & Zhang, Z. Irisin regulates lipid metabolism and ferroptosis in ovarian cancer cells by modulating the ALOX5-5-HETE-PD-L1 axis. Sci Rep 16, 7223 (2026). https://doi.org/10.1038/s41598-026-36816-4
الكلمات المفتاحية: سرطان المبيض, أيض الدهون, الموت بالخرف (فرفوبتوز), ALOX5, العلاج بالمركبات الطبيعية