Clear Sky Science · ar
الاستجابة الحرارية المحسّنة لإطارات نانوية من الذهب في نافذة NIR-II: دراسة عددية
حرارة لطيفة كأداة لمحاربة السرطان
يتجه الأطباء بشكل متزايد إلى استخدام جسيمات ذهبية دقيقة لمحاربة السرطان عن طريق تسخين الأورام من الداخل. التحدي يكمن في تسخين خلايا السرطان بدرجة تكفي لإضلالها دون إحراق الأنسجة السليمة المحيطة أو تدمير الجسيمات نفسها. تستخدم هذه الدراسة محاكاة حاسوبية متقدمة لتصميم نوع جديد من الجسيمات الذهبية المجوفة، يُسمّى الإطار النانوي المزدوج الطور، قادرًا على تسخين الأورام بعمق داخل الجسم بكفاءة وأمان باستخدام نوع خاص من الضوء غير المرئي.
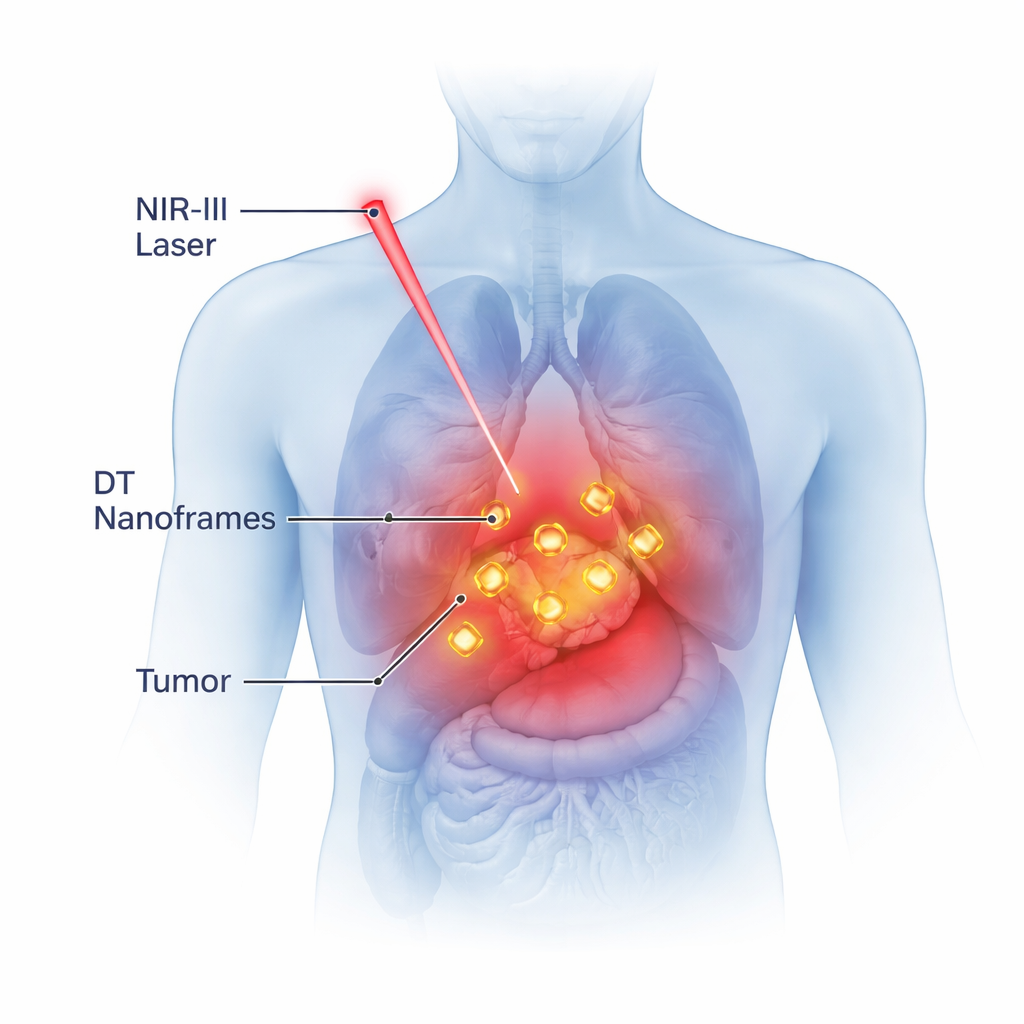
لماذا يهم الضوء غير المرئي
يمتص جسدنا أو يبعثر معظم الضوء المرئي، مما يحد من مدى اختراق الضوء للأنسجة. ومع ذلك، هناك «منطقة مثالية» في طيف الأشعة تحت الحمراء القريبة، تُعرف بنافذة NIR-II (1000–1400 نانومتر)، حيث يمكن للضوء أن يخترق الجسم لمسافات بوصات سنتيمترية مع تشتت وأضرار أقل. يمكن تعديل خصائص جسيمات الذهب بحيث تهتز إلكتروناتها بقوة عند أطوال موجية محددة من الضوء، وهي ظاهرة تُسمى الرنين. عندما يحدث ذلك داخل نافذة NIR-II، يمكن للجسيمات امتصاص ضوء الليزر بكفاءة وتحويله إلى حرارة بدقة في مكان الحاجة، داخل الورم بعمق.
حدود جسيمات الذهب الحالية
تم تجربة العديد من أشكال الذهب للتسخين العلاجي: كرات صلبة، ومكعبات، وقضبان، وهياكل حلقيّة، وقشور رفيعة على شكل «إطار». لكل شكل عيوبه. غالبًا ما لا يمكن تعديل الجسيمات الصلبة للوصول بعيدا بما يكفي داخل نافذة NIR-II. تسخن قضبان الذهب النانوية بكفاءة عالية، لكنها قد تسخن بشكل مفرط وتتشوه لتصبح كراتًا وتفقد سلوكها البصري الخاص. يمكن لإطارات الذهب المكعبة والكروية أن تُركّز الحرارة على زوايا حادة، وهو أمر مفيد، لكن نفس الحواف الحادة تجعلها عرضة للتقوّس وتغيير الشكل عند التعرض لتسخين قوي. يمكن ضبط النانوتوريس (الحلقات) على الطول الموجي المناسب لكنها تمتص حرارة أقل وتعتمد فعاليتها بشدة على اتجاهها نسبة إلى شعاع الليزر، ما يشكل مشكلة للجسيمات الطافية بحرية في الدم.
إطار ذهبي مزدوج الحلقات جديد
لتجاوز هذه المشاكل، اقترح الباحثون تصميمًا جديدًا: إطار نانوي مزدوج الطور مكوّن من حلقتين ذهبيتين مجوفتين مرتبتين متعامدتين، مثل شكل ثمانية ثلاثي الأبعاد. بالمحاكاة الحاسوبية قارنوا هذا التصميم مع قضبان نانوية قياسية، وإطارات مكعبة وكروية، ونانوطور مفردة. تم ضبط جميع الجسيمات بحيث يقع طولها الموجي الرنيني ضمن نافذة NIR-II. ثم، باستخدام مزيج من محاكاة البصريات وانتقال الحرارة، تتبّعوا مقدار الحرارة التي يولدها كل جسيم مع مرور الزمن، وكيف يتغير هذا التسخين عندما تكون الجسيمات موجهة عشوائيًا في الماء، كما ستكون في مجرى الدم.
موازنة الحرارة والاستقرار والحجم
ركزت الدراسة على تحقيق نطاق درجة حرارة محدد: حوالي 40–49 °م، حار بما يكفي لإجهاد أو قتل خلايا السرطان (فرط الحرارة) لكن ليس بحيث يحترق النسيج أو تذوب الجسيمات أو تتشوه. أظهرت المحاكاة أن بعض الأشكال، مثل الإطارات المكعبة والقضبان النانوية، يمكنها التسخين بسرعة كبيرة لكنها معرضة لتجاوز هذا النطاق الآمن أو تغيير الشكل تحت تسخين مطوّل. من ناحية أخرى، غالبًا ما فشلت النانوتوريات المفردة في الوصول إلى درجات الحرارة العلاجية، خاصة عندما كان اتجاهها بالنسبة لليزر غير ملائم. كما تبين أن الإطارات الكروية والمكعبة حساسة للغاية للتغيرات الصغيرة في سمكها أو مساميتها، وهو أمر قد يحدث بسهولة أثناء التصنيع أو تحت الحرارة، مما يحرف سلوكها خارج النطاق المطلوب.
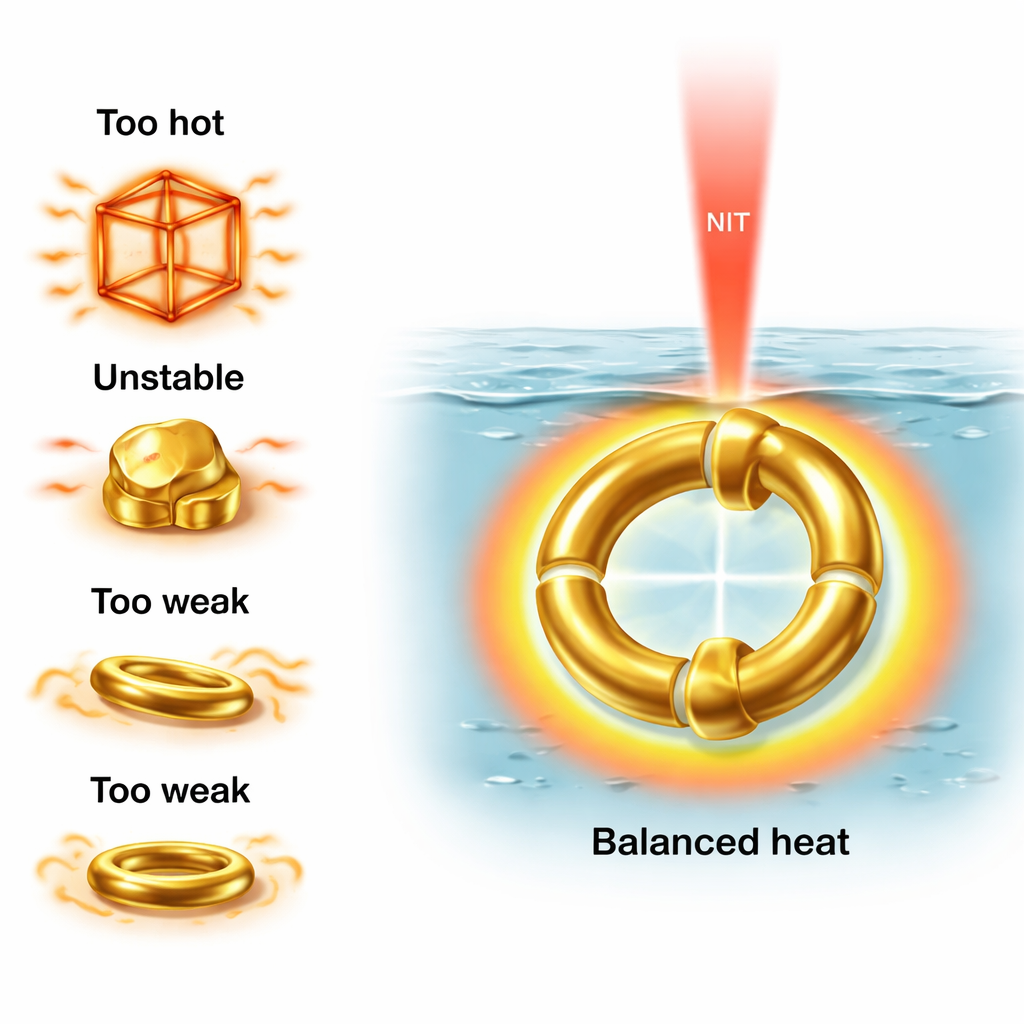
لماذا يبرز الإطار المزدوج الطور
يجمع تصميم الإطار المزدوج الطور بين عدة مزايا. تناظره العالي يجعله يمتص الضوء ويولد الحرارة بشكل مستقر حتى عند التوجيه العشوائي؛ فهو لا يعتمد على الاصطفاف مع استقطاب الليزر. شكله المنحني والمدوَّر يمنحه مقاومة أكبر للتشوّه الناتج عن الحرارة مقارنةً بالإطارات ذات الحواف الحادة. وبما أنه يحتوي على ذهب أكثر من طور واحد مفرد، فإنه يمكنه توليد حرارة كافية مع البقاء ضمن نافذة فرط الحرارة الآمنة عبر نطاق واسع من الأحجام والحجوم. كما أن زيادة حجم المعدن هذه تجعله واعدًا لأدوار مزدوجة: ليس فقط لتسخين الأورام، بل أيضًا لنثر الضوء بقوة كافية للمساعدة في التصوير واستشعار درجة الحرارة المحلية.
تبعات لعلاجات السرطان المستقبلية
لغير المتخصصين، الخلاصة الأساسية هي أن الشكل الدقيق للجسيم الذهبي يمكن أن يحدد نجاحه كأداة لتسخين السرطان. تشير هذه الدراسة إلى أن إطارات النانو المزدوجة الطور توفر توازنًا جيدًا بين التسخين القوي والقابل للتحكم والاستقرار البنيوي في ظروف واقعية. وبينما لا تزال هناك تحديات في تصنيع مثل هذه الإطارات الذهبية الملساء والمنحنية بشكل موثوق، تشير المحاكاة إلى أنها مخطط واعد لجيل مستقبلي من الجسيمات النانوية القادرة على تدفئة الأورام بدقة في أعماق الجسم، مما يحسّن سلامة وفعالية العلاجات الضوئية للسرطان.
الاستشهاد: Alali, F.A. Optimized thermal response of Au nanoframes in NIR-II window: a numerical study. Sci Rep 16, 5658 (2026). https://doi.org/10.1038/s41598-026-36727-4
الكلمات المفتاحية: جسيمات الذهب النانوية, العلاج الحراري الضوئي, علاج السرطان, الضوء القريب من تحت الحمراء, الطب النانوي