Clear Sky Science · ar
تطبيق بروتين شبيه بالكولاجين 1 المعبر عنه من المكورات العقدية من المجموعة A في Lactococcus كعلاج مناعي مبتكر ضد سرطان قناة البنكرياس الغدي
تحويل البكتيريا الصديقة إلى مقاتلة للسرطان
يعد سرطان البنكرياس من أكثر أنواع السرطان فتكا، ويرجع ذلك جزئياً إلى أنه يختبئ خلف دفاعات قوية تكبح جهاز المناعة في الجسم. تستكشف هذه الدراسة حليفاً غير متوقع في مكافحة هذا المرض: بكتيريا "جيدة" شائعة من عالم الألبان، أعيد هندستها لتتوجه نحو أورام البنكرياس وتساعد جهاز المناعة على مهاجمتها بفعالية أكبر. من خلال استعارة بروتين سطحي لزج من جرثوم المكورات العقدية المسبب للمرض، حول الباحثون ميكروباً غير ضار إلى أداة مستهدفة مضادة للسرطان في الفئران.
سرطان عنيد يخدع جهاز المناعة
يعتبر سرطان الغدد القنوية البنكرياسية شديد القتامة، حيث ينجو نحو مريض واحد فقط من بين ثمانية بعد خمس سنوات من التشخيص. سبب رئيسي لذلك هو بيئة الورم الدقيقة: قشرة كثيفة تشبه الندبة مليئة بالخلايا والجزيئات الداعمة التي تضعف الهجمات المناعية وتمنع العديد من الأدوية. من بين المذنبات هناك شبكات العدلات خارج الخلية، أو NETs — وهي شباك من الحمض النووي والبروتينات تطلقها خلايا الدم البيضاء إلى المحيط. في سرطان البنكرياس، تؤدي هذه الشباك اللاصقة ضرراً أكبر من نفعها: فهي تساعد الأورام على النمو، وتبعد الخلايا التائية القاتلة، وترتبط بنتائج أسوأ. أصبح تعطيل NETs، مع تنشيط المناعة المضادة للورم، استراتيجية مغرية.
استعارة بروتين لزج، ولكن من دون الجرثوم الخطير
أظهرت أعمال سابقة أن بروتيناً سطحياً من المكورات العقدية من المجموعة A، يسمى Scl1، يمكنه الالتحام بألياف مرتبطة بالأورام وتقليل تشكل NETs، مما يبطئ نمو أورام البنكرياس في الفئران. لكن المكورات العقدية من المجموعة A هي أيضاً بكتيريا تسبب التهاب الحلق وأمراضاً غازية خطيرة، مما يجعلها غير مناسبة كعلاج حي. للحفاظ على البروتين المفيد دون الجرثوم الضار، قامت الفريق بتعديل Lactococcus lactis — بروبيوتيك مستخدم على نطاق واسع في الغذاء ومعتبر آمناً — لعرض Scl1 على سطحه. تم اختبار السلالة الجديدة، المسماة Lactococcus::620، في فئران تحمل أوراماً بنكرياسية، باستخدام أورام تحت الجلد البسيطة ونماذج أكثر واقعية تنمو داخل البنكرياس نفسه.
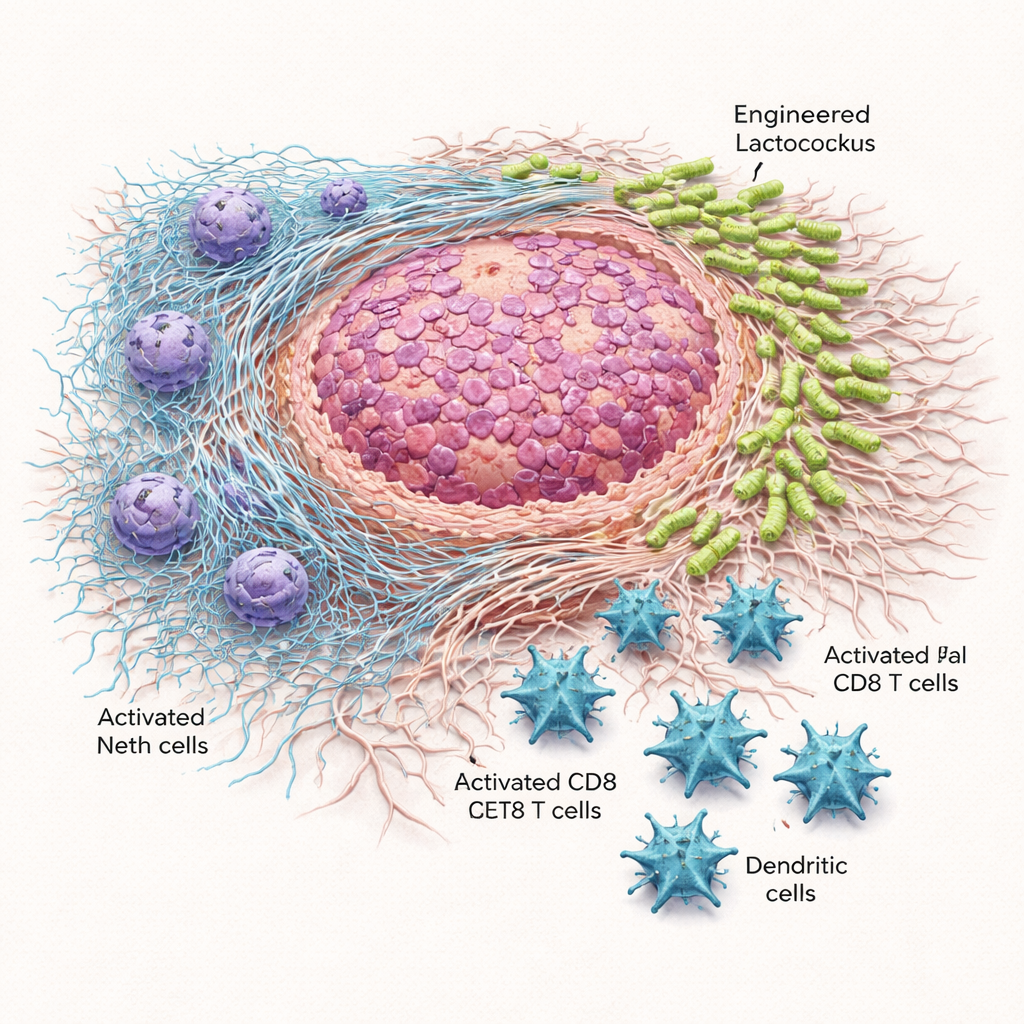
بكتيريا موجهة تقلص نمو الورم وتطيل البقاء
عندما تم حقن جرعة واحدة من البكتيريا المعدلة مباشرة في أورام تحت الجلد، أو إعطاؤها في البطن، نما الورم ببطء وكان وزنه أقل مقارنة بالفئران التي أعطيت Lactococcus العادية أو محلول ملحي كضابطة. في نموذج البنكرياس الأكثر تطلباً، كانت هناك حاجة لجرعات متعددة كل ثلاثة أيام، لكن الفوائد كانت ملحوظة. قلصت Lactococcus::620 الأورام، وخفضت وزنها، وطالت بقاء الحيوانات دون التسبب في وفيات مرتبطة بالعلاج. أظهرت الفحوص الميكروسكوبية وزراعة نسيج الورم أن البكتيريا الحاملة لـ Scl1 تراكمت بشكل موثوق في منطقة الورم، خصوصاً في المصفوفة الليفية التي تفرزها الخلايا الليفية المرتبطة بالسرطان، مع تجنب الطحال إلى حد كبير. في المقابل، انتشرت Lactococcus غير المعدلة في الجسم على نطاق أوسع وكانت أحياناً سامة عند إعطائها جهازياً.
نزع سلاح الشباك الضارة وإتاحة دخول الخلايا المناعية
أعاد التصميم المناعي للبكتيريا تشكيل البيئة المناعية المحيطة بالأورام. احتوت أورام الفئران المعالجة بـ Lactococcus::620 على المزيد من الخلايا التائية CD8 "القاتلة" والخلايا التغصنية — لاعبين أساسيين في التعرف على الخلايا السرطانية وتدميرها — وأظهرت هذه الخلايا التائية علامات استنزاف أقل ومزيداً من الجزيئات المرتبطة بالنشاط. في الوقت نفسه، انخفضت مقاييس نشاط NET. في اختبارات مخبرية، أطلقت العدلات المعرضة لـ Lactococcus::620 كمية أقل من الحمض النووي الحر وأظهرت نشاطاً أقل لإنزيم الميلوبيروكسيداز، وهو إنزيم ضروري لبناء NETs. في الفئران المعالجة، انخفض مستوى الحمض النووي الدوري المرتبط بـ NETs. والأهم من ذلك، عندما أُجريت التجارب نفسها في فئران معيبة وراثياً وغير قادرة على تكوين NETs، لم تعد البكتيريا المعدلة تبطئ نمو الورم. هذا الفقدان للفائدة يشير بقوة إلى أن حجب NETs يمثل جوهر قوة العلاج.
ما الذي قد يعنيه هذا لعلاج السرطان في المستقبل
تلخّص النتائج معاً مفهوماً جديداً: استخدام بكتيريا آمنة ومعتمدة غذائياً كحامل مبرمج لتوصيل بروتين حاجب للـ NET وهادف تجاه الورم إلى داخل البيئة العدائية لسرطان البنكرياس. في الفئران، خفف هذا النهج من عبء الورم، وحسن البقاء، وفتح الباب أمام الخلايا المناعية لأداء وظائفها بفعالية أكبر. بينما لا يزال هناك الكثير من العمل قبل أن يُجرّب مثل هذا الأسلوب في البشر — بما في ذلك الاختبارات في نماذج الأمراض النقيليّة والجمع مع العلاجات المناعية الحديثة — تُظهر الدراسة أن البكتيريا "الجيدة" المهندسة بعناية قد تساعد يوماً في تغيير المعادلة ضد أحد أكثر سرطاناتنا مقاومة.
الاستشهاد: Godfrey, E.A., Choi, S.J., Sestito, M. et al. Application of group A streptococcal collagen-like protein 1-expressing Lactococcus as a novel immunotherapeutic against pancreatic ductal adenocarcinoma. Sci Rep 16, 5911 (2026). https://doi.org/10.1038/s41598-026-36657-1
الكلمات المفتاحية: سرطان البنكرياس, علاج بروبيوتيكي, البيئة الدقيقة للورم, تعديل مناعي, شبكات العدلات خارج الخلية