Clear Sky Science · ar
التحقق السريري من صحة بنى شبكات CNN الخفيفة لتصنيف سرطانات الرئة المتعدد بشكل موثوق باستخدام تقنيات التصوير النسيجي المرضي
لماذا يهم هذا البحث للمرضى والأطباء
يكون سرطان الرئة قاتلاً في كثير من الأحيان لأنه يُكتشف متأخراً أو يُصنَّف بشكل خاطئ، مما قد يؤخر العلاج المناسب. يستكشف هذا البحث مدى قدرة برامج حاسوبية صغيرة وفعالة — بدلاً من نماذج ضخمة تستهلك طاقة كبيرة — على التعرف بثبات على أنماط مختلفة من سرطان الرئة من صور مجهرية لأنسجة مُلوَّنة. إذا نجحت هذه الأدوات الخفيفة، فقد تُستخدم في مستشفيات حول العالم، بما في ذلك تلك التي تفتقر إلى موارد حاسوبية متقدمة، لدعم اختصاصيي الأمراض في اتخاذ تشخيصات أسرع وأكثر اتساقاً.
التدقيق في السرطان باستخدام المجاهر الرقمية
عندما يُستأصل عقيد مشتبه به في الرئة أو يُؤخذ خزعة، يفحص الأطباء الشرائح الرقيقة المصبوغة تحت المجهر لتقرير ما إذا كانت حميدة أم إحدى أنواع السرطان. يركز هذا العمل على ثلاث فئات رئيسية: نسيج رئوي حميد، سرطان غدة الرئة (adenocarcinoma)، وسرطان الخلايا الحرشفية في الرئة (squamous cell carcinoma). تكتسب هذه الأنواع أهمية لأن استجابتها للعلاجات تختلف. يستخدم الفريق لقطات رقمية من هذه الشرائح — صور النسيج المرضي — ويسألون ما إذا كانت الشبكات العصبية المدمجة قادرة على تعلم الأنماط البصرية الدقيقة التي تميز كل فئة، من أشكال الخلايا إلى بنية النسيج، بموثوقية قريبة من النماذج الأكبر حجماً.
بناء مصنفات رقمية أصغر وأكثر ذكاءً
معظم أنظمة التعرف على الصور المتقدمة كبيرة جداً وتتطلب معالجات رسوم مكلفة، مما يصعّب نشرها في العديد من العيادات. بدلاً من ذلك، صمّم الباحثون أربعة نماذج تحليل صور «خفيفة»، سميت Lite-V0 وLite-V1 وLite-V2 وLite-V4، وكل منها نسخة مبسطة من شبكة عصبية التفافية. تتبع النماذج الأربعة نفس الوصفة الأساسية: تستخرج السمات البصرية تدريجياً عبر تكديس كتل بسيطة، ثم تلخّص الصورة وتُنتج واحدة من تسميات الأنسجة الثلاث. ما يتغير بين الإصدارات هو عدد الكتل واتساعها — بمعنى مقدار سعة النموذج لتعلّم الأنماط المعقدة. يتيح هذا التصميم المتحكم فيه للفريق دراسة مقدار التعقيد اللازم فعلاً لتصنيف السرطان بشكل موثوق.
التدريب والاختبار واختيار أنصف النماذج
لتعليم واختبار هذه النماذج، جمع المؤلفون مجموعة متوازنة مكونة من 15000 صورة لأنسجة الرئة، قسّموها بعناية إلى مجموعات تدريب وتحقق واختبار تحتوي على أعداد متساوية من كل فئة. قبل التدريب، تُعاد تحجيم كل صورة وتُطَبَّع وتُعبأ بتعديلات طفيفة مثل الانعكاسات والدورانات الصغيرة والتكبير لتقليد اختلاف مظهر الشرائح تحت ظروف مختلفة. والأهم من ذلك أن الفريق لا يقيم النماذج بناءً على الدقة الخام فقط، لأن هذا المقياس قد يخفي ضعف الأداء في فئة واحدة. بدلاً من ذلك، اعتمدوا مقياس «macro-F1» الذي يُلزم النموذج بأن يحقق أداء جيداً على الثلاث فئات، وليس على الأسهل منها فحسب. تتابع إجراءات تدريب مخصّصة هذا المقياس المتوازن تلقائياً وتوقف التدريب عندما تتوقف التحسينات، مع حفظ أفضل نسخة من كل نموذج للمقارنة. 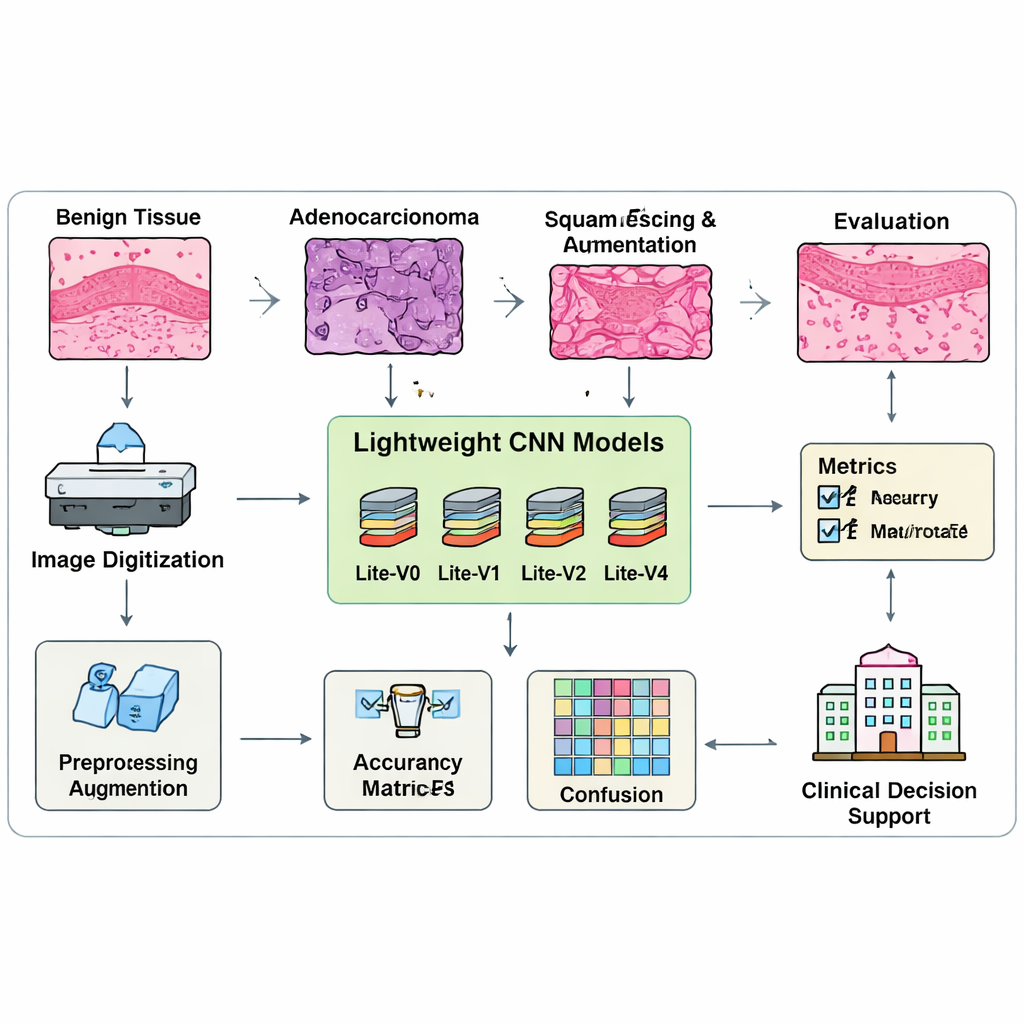
ما الذي يمكن أن يقدمه أفضل نموذج خفيف فعلاً
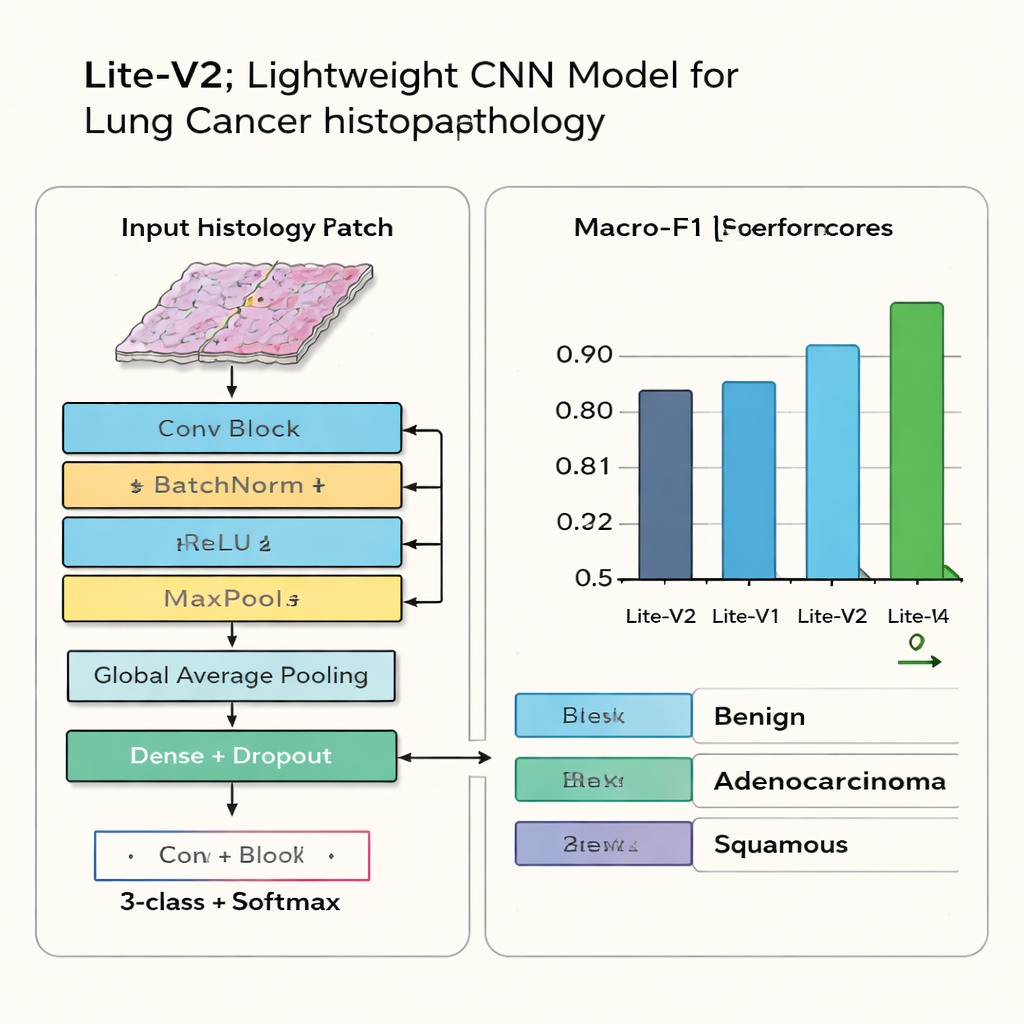
عند انتهاء التجارب، تبرز إحدى النسخ — Lite-V2. ليست الأصغر ولا الأكبر، بل تقع في المنتصف وتحقّق أفضل توازن بين الدقة والكفاءة. على صور الاختبار غير المرئية سابقاً، يصنّف Lite-V2 نسيجاً حميداً وسرطان الغدة وسرطان الخلايا الحرشفية بدقة عالية وموزعة بشكل متساوٍ، محققاً مقياس macro-F1 يقارب 0.96. تُظهر مخططات مصفوفة الالتباس أنه نادراً ما يخلط بين الفئات الثلاث، بينما تبدأ الإصدارات الأعمق في «الانطباع المفرط» (overfitting)، أي حفظ بيانات التدريب على حساب الموثوقية على حالات جديدة. أعاد المؤلفون تشغيل Lite-V2 عدة مرات بنقاط بداية عشوائية مختلفة واستخدموا اختباراً إحصائياً للتأكد من أن تفوقه على المتغيرات الأخرى ليس صدفة.
من كود البحث إلى الدعم في العالم الحقيقي
بعيداً عن أرقام الأداء، يؤكد البحث على إمكانية النشر العملي. نظراً لصغر حجم Lite-V2 وشقيقاته، يمكن تشغيلها على أجهزة مستشفيات متواضعة أو حتى على أجهزة طرفية دون إرسال الصور الحساسة إلى السحابة. نشر المؤلفون إطاراً قابلاً لإعادة الإنتاج يسجل كل تفصيلة تجريبية، من معالجة البيانات إلى منحنيات التدريب وأنماط الأخطاء، لكي يتمكن فرق أخرى من التحقق من النتائج أو توسيع العمل. بالنسبة للمرضى والأطباء، الخلاصة أن تصميمات الذكاء الاصطناعي الخفيفة والمطوّرة بعناية يمكن أن يقرب تصنيف سرطان الرئة الموثوق من ممارسة علم الأمراض اليومية، داعماً قرارات أسرع وأكثر اتساقاً — حتى في العيادات التي تفتقر إلى قدرات حاسوبية متقدمة.
الاستشهاد: Raza, A., Hanif, F. & Mohammed, H.A. Clinical validation of lightweight CNN architectures for reliable multi-class classification of lung cancer using histopathological imaging techniques. Sci Rep 16, 6512 (2026). https://doi.org/10.1038/s41598-026-36652-6
الكلمات المفتاحية: سرطان الرئة, النسيج المرضي, الشبكات العصبية التفافية, الذكاء الاصطناعي في التصوير الطبي, التشخيص بمساعدة الحاسوب