Clear Sky Science · ar
النيكوتيناميد يعاكس ضعف الميتوكوندريا والخلايا العصبية الناجم عن الروتانون في نموذج انتقالي لفترة الحياة المبكرة
لماذا تهم المحركات الخلوية الصغيرة للدماغ النامي
أثناء تطور الدماغ، يجب على مليارات الخلايا العصبية الشابة أن تنمو فروعاً طويلة وتكوّن وصلات دقيقة. تستكشف هذه الدراسة كيف تشكّل "محطات الطاقة" الخلوية — الميتوكوندريا — هذه العملية، وماذا يحدث عندما تُسمم هذه المحطات بشكل طفيف بمركب شبيه بالمبيد. كما يختبر الباحثون ما إذا كان جزيء شائع مرتبط بالفيتامينات، النيكوتيناميد، يمكن أن يساعد في حماية خلايا الدماغ النامية من هذا الضغط الطاقي الخفي، مع دلالات محتملة لحالات مثل الفصام.
من نموذج المبيدات إلى تجربة خلايا الدماغ
بنى الفريق على أعمال سابقة أظهرت أن جرذان رضيعين تعرضت لفترة وجيزة للروتانون، وهو مبيد يحجب خطوة رئيسية في إنتاج الطاقة الميتوكوندرية (المركب الأول)، أظهرت لاحقاً سلوكيات تشبه الفصام. لفهم ما يحدث على مستوى الخلايا العصبية الفردية، عزَلوا خلايا عصبية غير ناضجة من قشرة رحِم الجرذ وعرضوها لتركيز الروتانون نفسه الذي وُجد في أدمغة الحيوانات. سمح لهم هذا النهج "الترجمِي" بطرح سؤال: عند جرعات منخفضة واقعية لا تقتل الخلايا، هل يظل الروتانون يعيق كيفية نمو الخلايا العصبية وتكوّن توصيلاتها؟
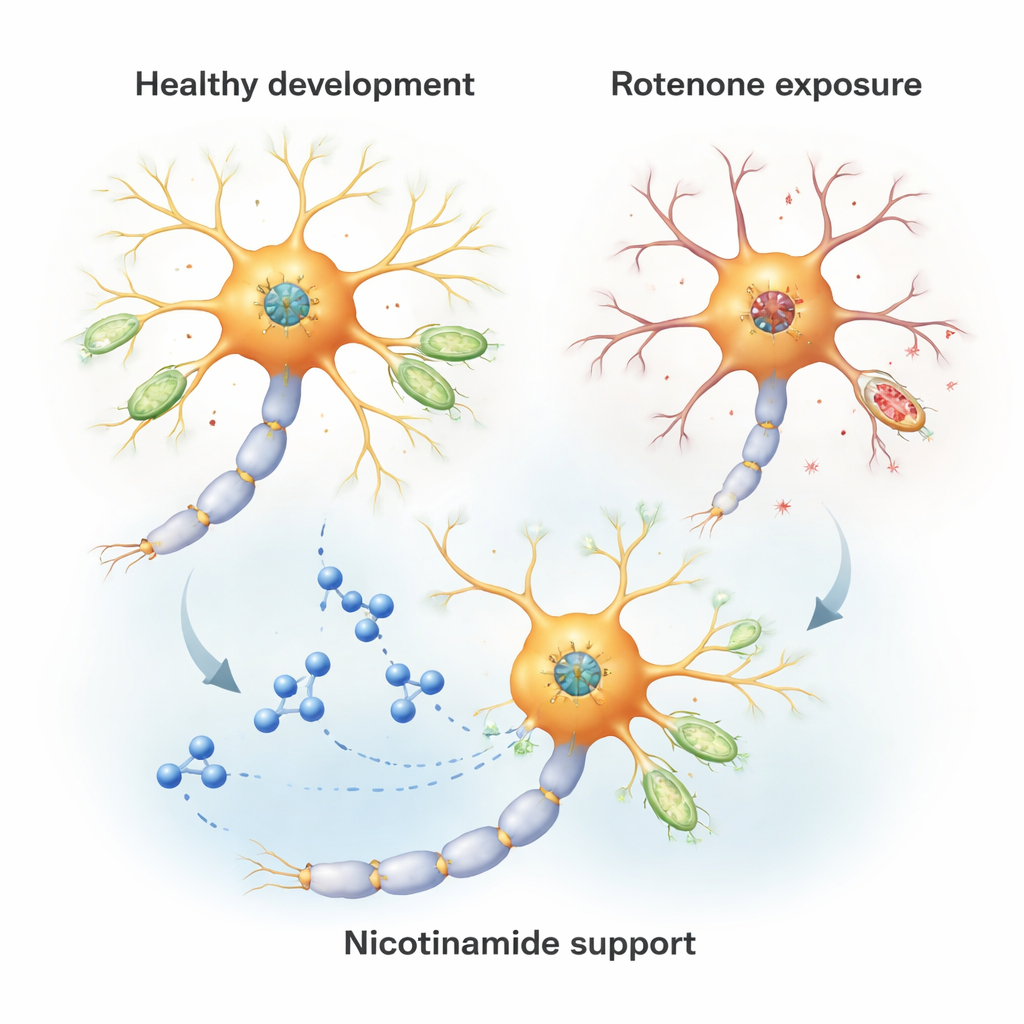
تباطؤ في الطاقة دون موت خلوي صريح
من المدهش أن جرعة الروتانون المنخفضة لم تتسبب في موت الخلايا العصبية أو تعطيل التوازن الأساسي للكالسيوم أو الشحنة الكهربائية عبر أغشية الميتوكوندريا — وهي سمات تُرى غالباً عندما تكون الخلايا في مأزق حاد. بدلاً من ذلك، أحدثت تحولاً أكثر هدوءاً لكنه مهمّاً في الأيض. أنتجت الميتوكوندريا طاقة أقل (ATP) واستهلكت أكسجيناً أقل، وانخفض النشاط العام للمركب الأول. في الوقت نفسه، انخفض إنتاج جزيء تفاعلي معين، الأكسيد الفائق الميتوكوندري، بدلاً من الارتفاع. تتناقض هذه النتيجة مع دراسات الجرعات العالية من الروتانون التي عادة ما تبلّغ عن ارتفاع سام في أنواع الأكسجين التفاعلية. هنا، الصورة توحي بـ"محرك بطيء" بدلاً من محرك يدخن أو يسخن بشدة.
تغيرات في مراقبة الجودة وشكل الخلية
عندما تتدهور أداء الميتوكوندريا، تعيد الخلايا عادة تشكيل هذه العضيات وتدويرها. وجد الباحثون إشارات إلى أن نظام مراقبة الجودة هذا قد تعطّل. تغيّرت البروتينات المشاركة في تقطيع وإعادة تشكيل الميتوكوندريا، وكذلك تلك التي تشير إلى عدد الميتوكوندريا الموجود، بعد التعرض للروتانون. تراكمت أيضاً مكونات مسار التدوير الخلوي (الالتهام الذاتي) بنمط يوحي بأن حزم النفايات كانت تتكوّن لكن لم تُزال بكفاءة. في الوقت نفسه، أصبحت الخلايا العصبية نفسها أبسط هيكلياً: كانت أشجارها الشجيرية (التغصّنات) أقصر وأقل عدداً. وبما أن التغصّنات حاسمة لاستقبال الإشارات، فإن هذا التقليم يوحي بأن حتى الإجهاد الميتوكوندري الطفيف والمزمن يمكن أن يترك آثاراً دائمة في دوائر الدماغ.
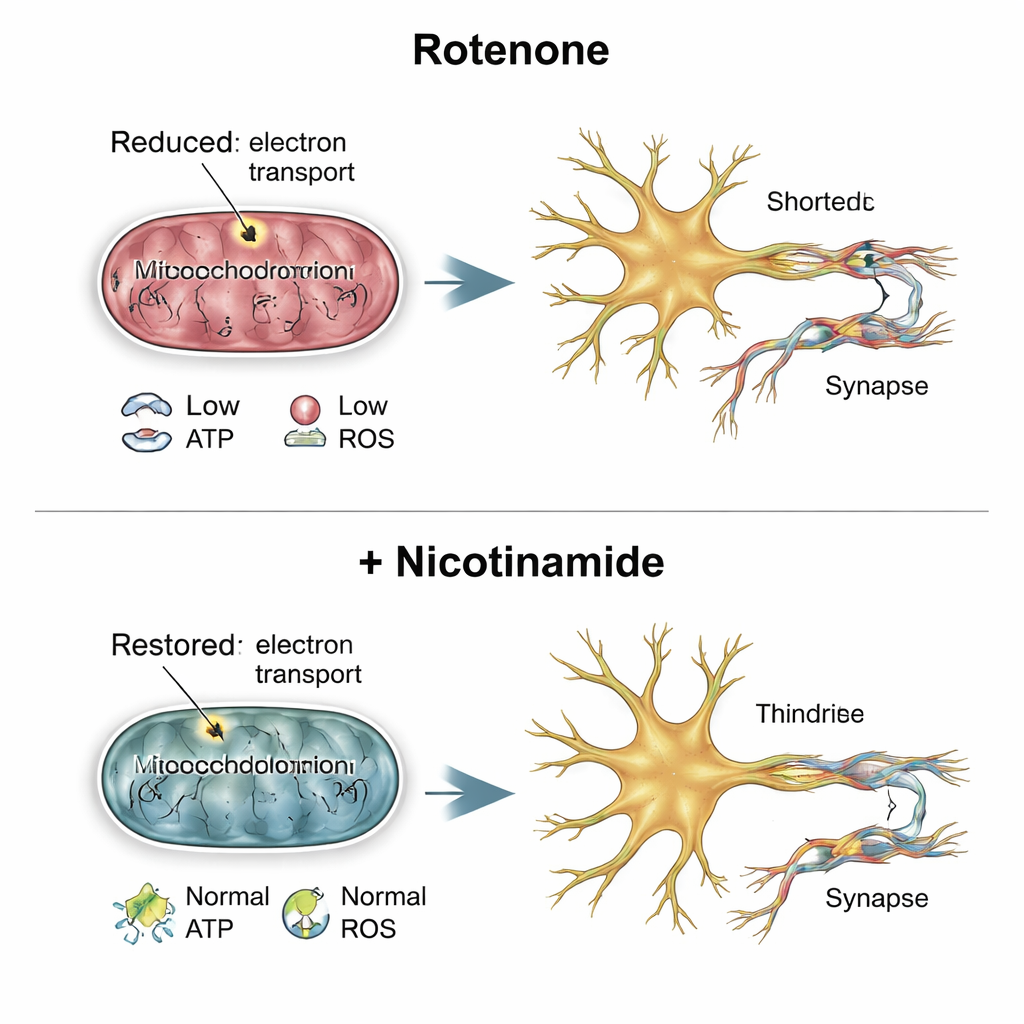
ضعف المشابك وكيف يساعد النيكوتيناميد
ثم تساءل الفريق عما إذا كانت نقاط الاتصال بين الخلايا العصبية — المشابك — قد تأثرت. باستخدام مؤشرات متوهجة لبروتينات ما قبل وما بعد المشبك، رأوا أن الخلايا المعالجة بالروتانون كانت تحتوي على مزيد من مكونات المشبك لكن بمحاذاة أسوأ بينها، ما يشير إلى تراكم الآلات دون تكوين اتصالات وظيفية كاملة. أدى إدخال النيكوتيناميد قبل التعرض للروتانون إلى تغيير هذه الصورة. استعاد النيكوتيناميد، وهو لبنة بناء لجزيء حامل الطاقة NAD، التنفّس الميتوكوندري ومستويات ATP وإنتاج الأكسيد الفائق إلى قيم تقارب الطبيعية. كما أعاد تطبيع مؤشرات التدوير، وخفّض التراكم غير الطبيعي لبروتينات المشبك، وحسّن محاذاتها، وأعاد عدد وطول التغصّنات إلى مستويات مماثلة للخلايا غير المعالجة.
ماذا قد يعني هذا لاضطرابات الدماغ
تلمّ النتائج مجتمعة إلى أن الضربات المتواضعة وغير القاتلة لوظيفة الميتوكوندريا خلال فترة الحياة المبكرة يمكن أن تتسرب لتضعف شكل الخلايا العصبية وتكوين المشابك — عمليات يُعتقد أنها متغيرة في اضطرابات مثل الفصام. لم يعِدِ النيكوتيناميد كل التغيرات الجزيئية بالسحر، لكنه كان كافياً لاستعادة توازن الطاقة، وأنظمة التنظيف، وبنية التغصّنات، وتنظيم المشابك في هذا النموذج الخلوي. للقراء غير المتخصصين، الرسالة الأساسية هي أن الحفاظ على صحة "محطات طاقة" الخلايا أثناء التطور قد يكون محورياً لبناء دوائر دماغية قوية، وأن دعم مسارات وقود الميتوكوندريا بجزيئات مرتبطة بالفيتامين B3 قد يكون وسيلة لمواجهة الإصابات المبكرة الخفية. بينما لا يزال هناك الكثير من العمل قبل أن يُؤخذ أي علاج بعين الاعتبار لدى البشر، تقدم هذه الدراسة جسرًا آلياً بين التعرضات البيئية، والإجهاد الميتوكوندري، والصحة الدماغية على المدى الطويل.
الاستشهاد: Siena, A., Souza e Silva, L.F., Araujo, V.C. et al. Nicotinamide counteracts Rotenone-induced mitochondrial and neuronal dysfunction in a translational early-life model. Sci Rep 16, 7159 (2026). https://doi.org/10.1038/s41598-026-36651-7
الكلمات المفتاحية: الميتوكوندريا, تطور الدماغ, الفصام, النيكوتيناميد, الروتانون