Clear Sky Science · ar
المؤشرات السطحية على السوبرمير تتفوق على الحويصلات الخلوية في تشخيص سرطان القولون والمستقيم
لماذا قد تغير جزيئات الدم الصغيرة فحوصات السرطان
يُعد سرطان القولون والمستقيم واحدًا من أكثر السرطانات شيوعًا عالميًا، ويحتاج الأطباء بشكل عاجل إلى اختبارات دم أفضل تكتشف المرض مبكرًا وتراقب استجابة العلاج. تَفحص هذه الدراسة فئة جديدة معروفة مؤخرًا من الجسيمات فائقة الصغر في الدم تُسمى «السوبرمير»، وتُظهر أنها قد تحمل إشارات سرطانية أوضح من الجسيمات المعروفة أكثر. كما يكشف المؤلفون عن مستشعر سريع قادر على قياس هذه السوبرمير مباشرةً من قطرة دم صغيرة في أقل من نصف ساعة، ما قد يفتح الباب أمام تشخيصات أسرع وأكثر دقة للسرطان.
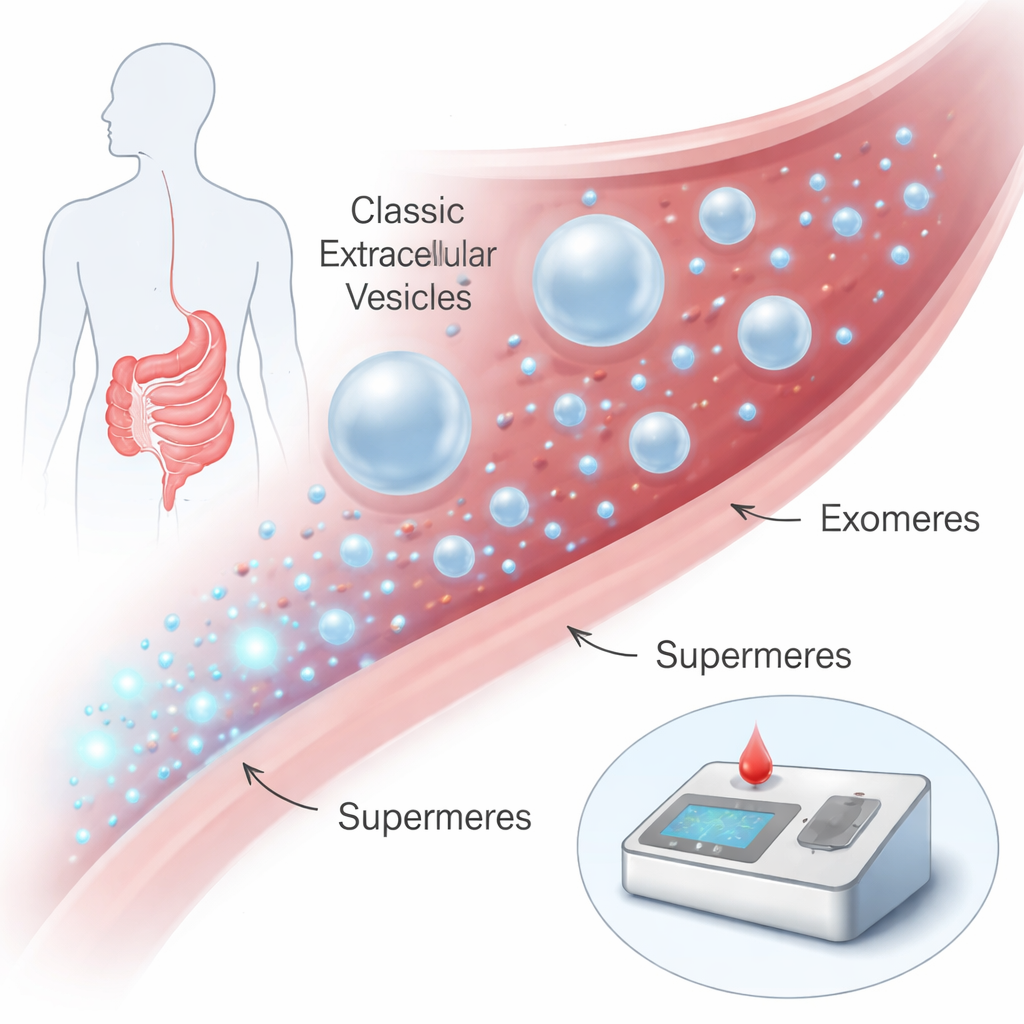
رسل صغيرة في مجرى الدم
تفرز خلايانا باستمرار حزمًا نانوية الحجم في سوائل الجسم مثل الدم. لسنوات، ركزت الاهتمامات على الجسيمات المحاطة بغشاء مثل الإكسوسومات والحويصلات خارج الخلية الأخرى، التي تستطيع نقل البروتينات والمواد الجينية بين الخلايا وقد دُرست كمؤشرات مرضية. ومؤخرًا اكتشف الباحثون جسيمات أصغر خالية من الغشاء تُدعى الإكسومير، ثم أصغر منها السوبرمير. يبلغ قطر السوبرمير نحو 15–25 نانومتر فقط—آلاف منها قد تصطف عبر عرض شعرة الإنسان—ومع ذلك فهي محشوة بجزيئات مرتبطة بالأمراض. أشارت أعمال سابقة إلى أن السوبرمير قد تكون غنية بشكل خاص بإشارات السرطان، لكنها كانت صعبة العزل والدراسة، حيث تتطلب أيامًا من الطرد المركزي فائق السرعة ومعدات متخصصة.
ما الذي يميز السوبرمير
قام الفريق بفصل ثلاثة أنواع رئيسية من الجسيمات النانوية من مزروعات خلايا سرطانية ودم بشري: الحويصلات خارج الخلية الصغيرة، الإكسومير، والسوبرمير. أكدوا أن كل مجموعة لها نطاق حجم مميز، مع كون السوبرمير الأصغر. لكن الاختلاف الأساسي كان كهربائيًا. حملت السوبرمير شحنة سطحية سالبة أقوى بكثير من الجسيمات الأخرى—بنحو ضعف المستوى الذي تصبح عنده الحركة الحرارية العشوائية ذات أهمية—ترجع في الأساس إلى خيوط من الحمض النووي الريبوزي (RNA) المتشبثة بسطحها. عندما هضم الباحثون هذه الحمضيات النووية بالإنزيمات، انخفضت الشحنة بشكل حاد، مما أظهر أن RNA السطحي مركزي للتوقيع الكهروستاتيكي للسوبرمير. كشف تخطيط البروتينات أن للسوبرمير أيضًا «بطاقات تعريف» خاصة بها: بروتينات مثل HSPA13 وENO2 وDDR1 كانت غنية جدًا على السوبرمير لكنها غائبة إلى حد كبير عن أنواع الجسيمات الأخرى، تمامًا مثل العلامات التقليدية التي تميز الحويصلات خارج الخلية العادية.
مستشعر سريع يستمع للشحنة
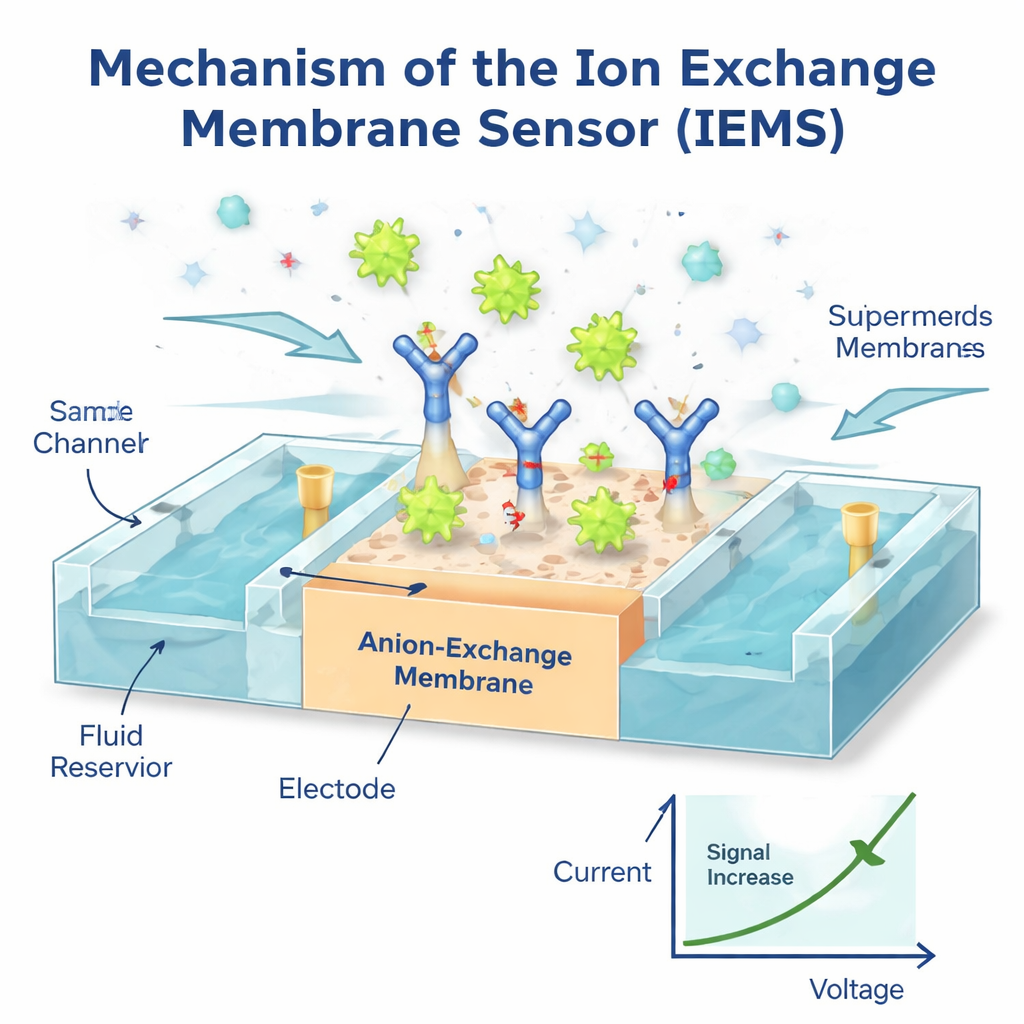
لاستغلال هذه الخصائص الفريدة، بنى المؤلفون مستشعر غشائي لتبادل الأيونات (IEMS)، وهو جهاز صغير يشعر بتغيرات في التيار الكهربائي عندما ترتبط الجسيمات المشحونة بسطحه. طبّقوا غشاءً خاصًا مُغطى بأجسام مضادة تلتقط بروتينًا محددًا، مثل علامة مرتبطة بالسرطان، من عينة دم متدفقة. وبما أن السوبرمير مشحونة بشدة بينما معظم الجسيمات الأخرى والبروتينات الحرة ضعيفة الشحنة، فإن السوبرمير الملتقطة فقط هي التي تغير سلوك الجهد-التيار للغشاء بشكل ملحوظ. النتيجة إشارة كهربائية قوية وانتقائية تعكس عدد السوبرمير الحاملة لتلك العلامة. باستخدام هذا النظام، تمكن الفريق من اكتشاف ما يصل إلى مليون سوبرمير لكل مليلتر عبر مدى تركيز يبلغ ألف ضعف، كل ذلك في نحو 30 دقيقة وباستخدام 50 ميكرولتر فقط من العينة—دون حاجة لتنقية مطولة. أظهرت تجارب اختُبرت فيها كميات معروفة من السوبرمير مضافة إلى بلازما صحية استردادًا شبه كامل، وكانت القياسات متطابقة مع تلك من أجهزة بصرية متقدمة وبطيئة.
تفوق على مؤشرات الجسيمات الحالية
مسلحين بالطرائق التقليدية والسريعة معًا، قارن الباحثون السوبرمير مباشرة بالإكسومير والحويصلات خارج الخلية الصغيرة في دم أشخاص مصابين بسرطان القولون والمستقيم ومتطوعين أصحاء. ركزوا على عدة بروتينات تظهر على الأنواع الثلاثة من الجسيمات، بما في ذلك مؤشرات ورم معروفة مثل CEA وGPC1. بالنسبة لكل بروتين مشترك تقريبًا، كانت الإشارة التي تحملها السوبرمير أفضل أو مساوية في تمييز المرضى المصابين عن الأصحاء، بينما أظهرت الإكسومير غالبًا قيمة تشخيصية ضئيلة. كانت البروتينات الخاصة بالسوبرمير مثل HSPA13 وENO2 وDDR1 مفيدة بشكل خاص: كانت تكاد لا تُكتشف في بلازما الأصحاء لكنها مرتفعة بقوة في سرطان القولون والمستقيم، مما وفر فصلًا ممتازًا بين المجموعتين. بشكل لافت، في مريضين دُرِسا قبل وبعد استئصال الورم، انخفضت مستويات السوبرمير بشكل حاد بعد إزالة الورم، بينما تغيرت الإشارات من الحويصلات التقليدية القليلة جدًا، مما يشير إلى أن السوبرمير تُعكس عبء الورم عن قرب.
ماذا قد يعني هذا لعينات السرطان المستقبلية
لوضع مستشعرهم الجديد على المحك في ظروف واقعية، استخدم الفريق IEMS لقياس السوبرمير الحاملة لعلامات مختلفة في بلازما مرضى بسرطان القولون والمستقيم، وسرطان البنكرياس، والميلانوما الدماغية (الغلوبلاستوما)، ومتبرعين أصحاء. كانت القراءات السريعة والخالية من العزل مطابقة عن قرب لتلك من الطرائق الأبطأ بكثير التي تجمع بين الطرد المركزي فائق السرعة والتحليل البصري، مؤكدة أن السرعة لم تذهب على حساب الدقة. في سرطان القولون والمستقيم، تفوقت قياسات السوبرمير على مستويات الدم الإجمالية لـ CEA، وهو علامة سريرية مستخدمة منذ زمن. تشير النتائج مجتمعة إلى أن السوبرمير ليست مجرد فضول مجهري آخر، بل مصدر قوي ومتاح لمعلومات السرطان. إذا أُكدت هذه النتائج في مجموعات مرضى أكبر وأكثر تنوعًا، فقد تصبح قياسات السوبرمير الحاملة للعلامات باستخدام مستشعرات صغيرة قائمة على الشحنة وسيلة عملية لفحص سرطان القولون والمستقيم، ومراقبة العلاج، وربما تكييف العلاجات بجهد ووقت وعينات أقل وتعقيد أقل مما تتطلبه الطرق الحالية.
الاستشهاد: Kumar, S., Sinclair, J.A., Shi, T. et al. Surface markers on supermeres outperform extracellular vesicles in colorectal cancer diagnosis. Sci Rep 16, 5989 (2026). https://doi.org/10.1038/s41598-026-36626-8
الكلمات المفتاحية: سرطان القولون والمستقيم, مؤشرات الدم الحيوية, الجسيمات النانوية خارج الخلايا, السوبرمير, تقنية المستشعرات الحيوية