Clear Sky Science · ar
تعديلات m6A للمضيف تشكّل الميكروبيوتا التي تحفز الفيروبتوزيس الخلوي كمسار سببي للأمراض التنفسية المزمنة
لماذا تهمك الميكروبات بالنسبة لرئتيك
عادةً ما تُلقى اللائمة على التدخين والتلوث أو الحساسية في مشاكل التنفّس المزمنة مثل الربو ومرض الانسداد الرئوي المزمن (COPD). تقترح هذه الدراسة لاعبًا آخر أقل وضوحًا: التريليونات من الميكروبات التي تعيش في أمعائنا وعلى جلدنا. باستخدام بيانات جينية واسعة النطاق، يبيّن المؤلفون أن بعض الميكروبات قد لا تكون مجرد مرافقات للأمراض الرئوية، بل قد تسهم في حدوثها—من خلال تغييرات كيميائية دقيقة داخل خلايانا وشكل من أشكال الضرر الخلوي المدفوع بالحديد. قد يؤدي فهم هذه الشبكة الخفية في نهاية المطاف إلى طرق جديدة للوقاية أو العلاج عن طريق توجيه ميكروباتنا ومساراتها الجزيئية باتجاهات أكثر صحة.
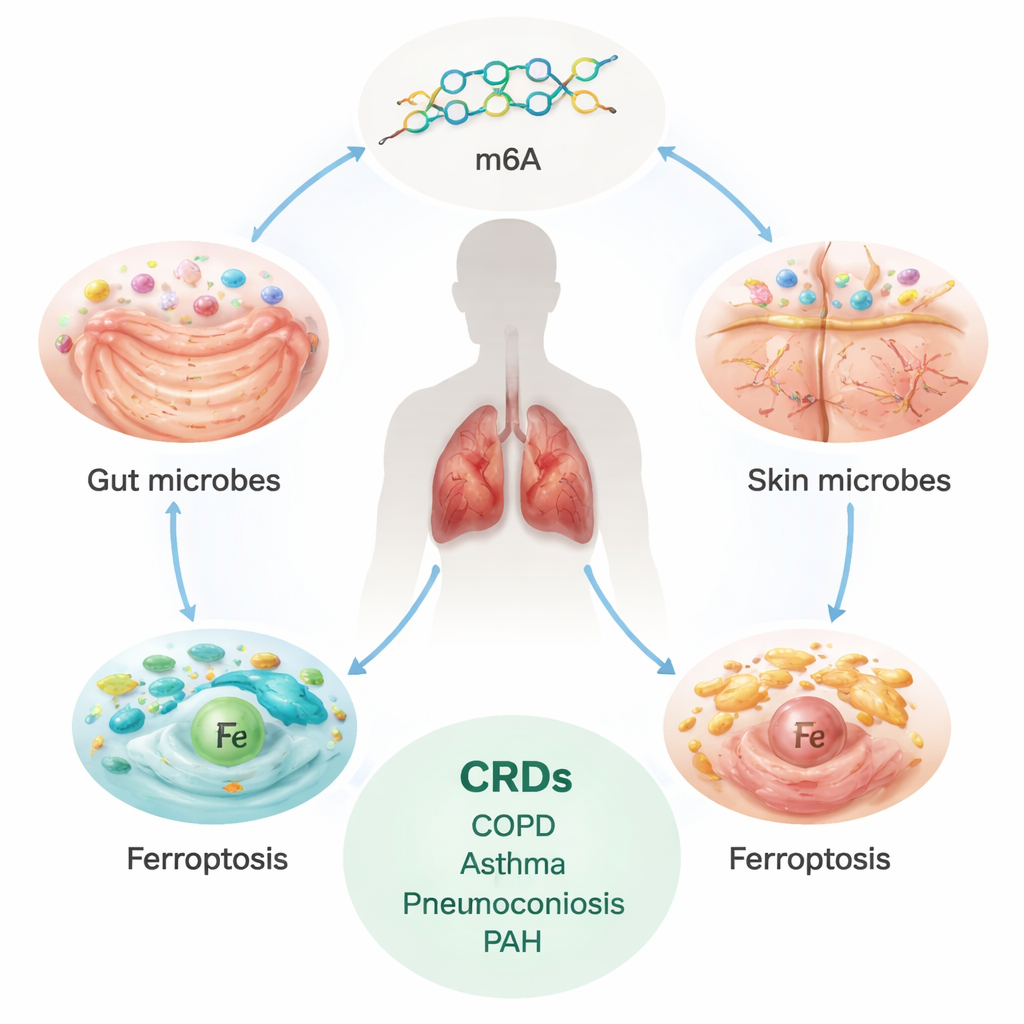
العبء الخفي للأمراض الرئوية المزمنة
تؤثر الأمراض التنفسية المزمنة، بما في ذلك COPD والربو ومرض الرئة الخلالي (ILD) ومرض الرئة الناجم عن استنشاق الغبار (pneumoconiosis) وارتفاع ضغط الشريان الرئوي (PAH)، على مئات الملايين من الناس حول العالم وتسبب ملايين الوفيات سنويًا. غالبًا ما تتقدم هذه الحالات ببطء لكن بثبات، مسببة تندبًا أو إعادة تشكيل للرئتين والأوعية الدموية وتجعل التنفّس صعبًا. تركز العلاجات الحالية في الغالب على إدارة الأعراض؛ فهي لا توقف بالضرورة أو تعكس الضرر الأساسي. دفع ذلك العلماء للبحث عن أسباب أعمق وجذرية، خاصة تلك القابلة للتعديل قبل أن تتطور الحالة إلى مرحلة خطيرة.
الجوار الميكروبي في الأمعاء وعلى الجلد
نعلم الآن أن الأمعاء والجلد موطن لمجتمعات ميكروبية معقدة تساعد على تدريب الجهاز المناعي، وشكل الأيض، والحفاظ على الحواجز الدفاعية. لكن هل هذه الميكروبات تحرك حقًا المرض الرئوي، أم أنها تتغيّر ببساطة عندما يمرض الناس؟ لفك ارتباط السبب بالنتيجة، استخدم الباحثون أسلوبًا يُدعى العشوائية المندلية (Mendelian randomization)، الذي يستفيد من الاختلافات الجينية الطبيعية بين الأشخاص كنوع من "التجربة" مدى الحياة. جمعوا بيانات جينية عن مئات أنواع الميكروبات المعوية والجلدية مع بيانات عن خمسة أمراض رئوية مزمنة رئيسية من دراسات أوروبية واسعة، لاختبار ما إذا كانت الميل الوراثي إلى مستويات أعلى أو أقل من ميكروبات محددة مرتبطًا بخطر كل مرض.
الميكروبات التي تُفيد أو تُضِرّ الرئتين
حددت التحليلات عشرات الميكروبات المعوية التي إما تزيد أو تقلل من مخاطر كل مرض تنفسي، غالبًا بنمط خاص بكل مرض. على سبيل المثال، بدا أن بعض البكتيريا المعوية تحمي من COPD أو الربو أو PAH، بينما زادت أخرى من احتمال الإصابة بـILD أو COPD. أظهرت ميكروبات الجلد روابط أقل قوة لكنها قابلة للكشف، مع ارتباط بعض الأنواع بمخاطر أعلى وأنواع أخرى بمخاطر أقل عبر حالات مختلفة. كما أعاد الفريق توجيه التحليل في الاتجاه المعاكس، فوجدوا أن المخاطر الجينية لـCOPD والربو وأمراض رئوية أخرى تنبأت بدورها بتغيرات في الميكروبيوتا المعوية والجلدية. يشير هذا التبادل ذهابًا وإيابًا إلى حلقة تغذية مرتدة: يمكن للميكروبات أن تشكل المرض الرئوي، ويمكن للمرض الرئوي أن يعيد تشكيل النظم الميكروبية لدينا.
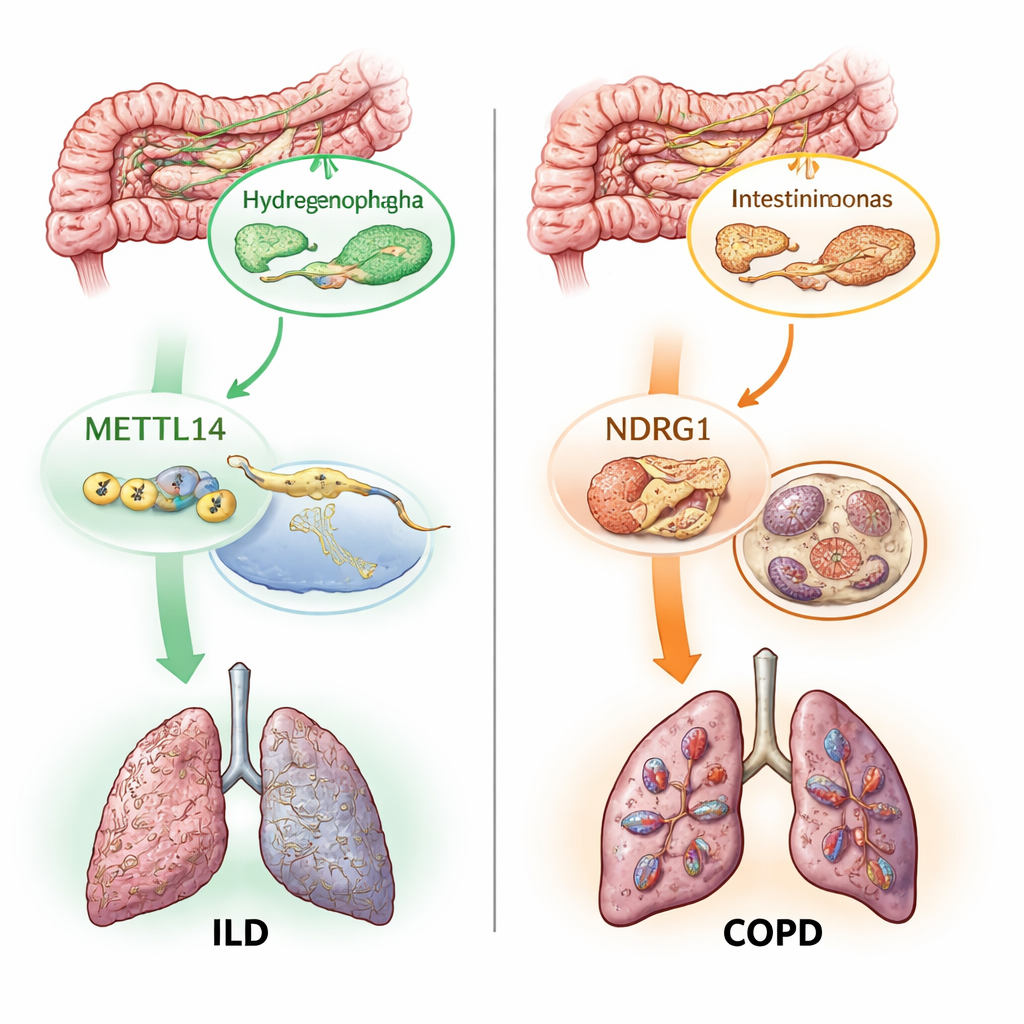
مفتاحان جزيئان: علامات RNA والموت الخلوي المعتمد على الحديد
بعيدًا عن رسم خريطة الميكروبات المهمة، سأل المؤلفون كيف قد تؤثر هذه الشركاء المجهرية على أنسجة الرئة. ركّزوا على مسارين جزيئيين يُشتبه بالفعل في إحداث ضرر رئوي. الأول، المسمّى تعديل m6A، هو شِرْط كيميائي صغير يُضاف إلى الـRNA ويحسب كيفية تشغيل الجينات وإيقافها. الثاني، الفيروبتوزيس (ferroptosis)، هو شكل من أشكال موت الخلايا المعتمد على الحديد والذي يقوده أكسدة مفرطة للدهون في أغشية الخلايا. باستخدام بدائل جينية لـ19 جينًا مرتبطًا بـm6A ومئات الجينات المرتبطة بالفيروبتوزيس، اختبروا ما إذا كانت التغيرات في هذه المسارات ترتبط سببيًا بأمراض الرئة. وجدوا أن جينًا واحدًا من كتّاب m6A، METTL14، ارتبط بانخفاض مخاطر ILD، وأن عدة جينات في مسار الفيروبتوزيس، بما في ذلك NDRG1، ارتبطت بزيادة مخاطر COPD وILD والربو.
ربط النقاط: من الميكروبات إلى الخلايا إلى المرض
أبرز أجزاء العمل كان تتبُّع كيفية ارتباط هذه المكوّنات كسلاسل سبب ونتيجة. أشارت تحليلات الوساطة الإحصائية إلى أن بعض التأثير الوقائي لـMETTL14 على ILD يمر جزئيًا عبر تغيّرات يسببها في ميكروب معوي معين يُدعى Hydrogenophaga. في مسار آخر، بدا أن بكتيريا معوية محددة، Intestinimonas massiliensis، تؤثر على خطر COPD جزئيًا عن طريق تفعيل NDRG1 وبرنامج موت الخلايا الفيروبتوزي. ثم تحقق الفريق من بيانات أنسجة الرئة البشرية وأكدوا أن كلًا من METTL14 وNDRG1 يُعبَّران عنهما بشكل مختلف في عينات المرضى مقارنةً بالعينات السليمة. أخيرًا، باستخدام خرائط جينية خلوية مفردة للخلايا المناعية، حددوا أن التأثير الضار لـNDRG1 على COPD يتركز في مجموعة فرعية من الخلايا المناعية، نوع من الخلايا الوحيدة (monocytes)، مما يوحي أن الأدوية المستقبلية التي تستهدف هذا الجين قد تحتاج أن تعمل بشكل محدد على خلايا معينة.
ماذا يعني هذا للعلاجات المستقبلية
للجمهور غير المتخصص، الرسالة الأساسية أن صحة الرئة ليست مسألة ما نتنفسه فقط، بل تتعلق أيضًا بالميكروبات التي تعيش فينا وعلى أجسادنا وبالمفاتيح الجزيئية التي تُشغّلها داخل خلايانا. لا تستطيع هذه الدراسة إثبات كل خطوة تجريبيًا، وهي محدودة أساسًا بأشخاص من أصل أوروبي، لكنها تقدم دلائل جينية قوية على أن الميكروبات المعوية وعلامات RNA مثل m6A والموت الخلوي المعتمد على الحديد تشكّل مسارًا مترابطًا يؤدي إلى تلف رئوي مزمن. على المدى الطويل، قد تُلهم هذه السلسلة البحثية استراتيجيات جديدة تجمع بين علاجات مستندة إلى الميكروبيوم وأدوية تستهدف METTL14 أو NDRG1 أو الفيروبتوزيس، بهدف ليس فقط تخفيف الأعراض بل تعطيل الدارات البيولوجية التي تدفع تقدم الأمراض التنفسية المزمنة.
الاستشهاد: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
الكلمات المفتاحية: الميكروبيوم المعوي, أمراض الرئة المزمنة, الربو وCOPD, ابيجينتيك الـRNA, مسارات موت الخلايا