Clear Sky Science · ar
ATF4 ينظّم خلل الميتوكوندريا والميتوفاجي، مساهماً في استماتة بطانة القرنية
لماذا قد يتغيّم نافذة العين
تبقى قرنياتنا — النوافذ الشفافة الأمامية للعين — صافية بفضل طبقة رقيقة ومواظبة من الخلايا على السطح الداخلي. في اعتلال بطانة القرنية فوكس (FECD)، يفقد ملايين الأشخاص هذه الخلايا تدريجياً، مما يؤدي إلى وذمة وتشوش الرؤية وغالباً زراعة قرنية. تطرح هذه الدراسة سؤالاً أساسياً لكنه حاسم: ما الذي يدفع هذه الخلايا إلى اتخاذ قرار الموت، وهل يمكن إيقاف «مفتاح» جزيئي واحد لحمايتها؟
طبقة خلوية هشة تحافظ على وضوح الرؤية
بطانة القرنية طبقة مفردة من خلايا مسدسة السداسيات تضخ السوائل باستمرار خارج القرنية للحفاظ على صفائها. في FECD، تتعرض هذه الخلايا للإجهاد وتختفي تدريجياً، بينما تتراكم نتوءات من مادة غير طبيعية تعرف بالغوتا على الغشاء القاعدي. ونظراً لعدم وجود أدوية معتمدة لـ FECD واعتماد العلاج على زرع القرنية بشكل رئيسي، يحاول الباحثون فهم كيفية دفع الإجهاد داخل هذه الخلايا إليها نحو الموت. أشارت أعمال سابقة بشكل منفصل إلى وجود ضغوط في مقصورتين خلويتين رئيسيتين — الشبكة الإندوبلازمية (مصنع طي البروتين في الخلية) والميتوكوندريا (محطات طاقة الخلية) — لكن كانت العلاقة بين استجابات هذين النوعين من الإجهاد غير واضحة.
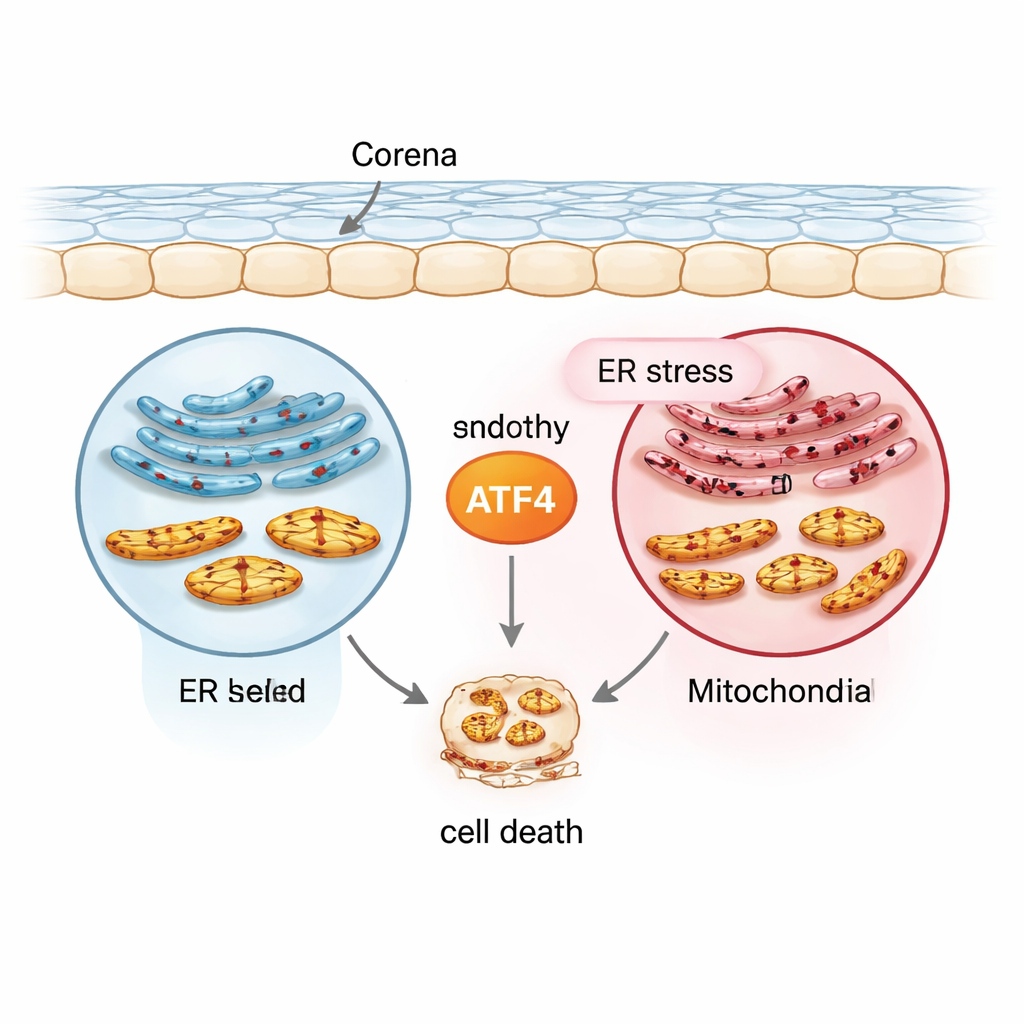
مراسل الإجهاد في المحور: ATF4
ركز الفريق على بروتين اسمه ATF4، وهو عامل نسخ يبدّل تشغيل العديد من جينات الاستجابة للإجهاد. باستخدام خط خلوي طبيعي من خلايا بطانة القرنية البشرية (21T)، وخط خلوي يشبه FECD يحمل تمدد التكرار المرتبط بالمرض في TCF4 (F35T)، وخلايا بطانة قرنية بشرية أولية، ونماذج فأرية معرضة لأشعة UVA، أنشأوا مجموعة من الظروف التي تحاكي الإجهاد المزمن. استحثوا إجهاد الشبكة الإندوبلازمية بدواء يسمى تويناكاميسين ثم قاسوا ATF4 وعلامات أخرى. بالمقارنة مع الخلايا الطبيعية، بدأت الخلايا المشابهة لـ FECD بمستويات أعلى من ATF4 والبروتينات المرتبطة بالإجهاد، وازداد ATF4 أكثر تحت الإجهاد المزمن في كل من الخلايا المزروعة وأنسجة القرنية البشرية. وضع هذا النمط ATF4 عند مفترق طرق بين الاستجابات الوقائية المبكرة والإشارات الهادفة للتدمير الذاتي لاحقاً.
من فشل في الطاقة إلى موت مبرمج
بعد ذلك، نظر الباحثون في كيفية تأثير هذا الإجهاد على الميتوكوندريا. في الخلايا الشبيهة بـ FECD، أنتجت الميتوكوندريا طاقة ATP أقل، فقدت جهد الغشاء الكهربائي، وتحولت من أشكال طويلة وشبكية إلى شظايا صغيرة متعددة. تفاقمت هذه التغيرات عندما طال إجهاد الشبكة الإندوبلازمية. في الوقت نفسه، ازداد وجود بروتينات الموت الخلوية المعروفة — مثل الكاسبيزات النشطة وبروتين إصلاح الحمض النووي PARP في شكله المقطوع المرتبط بالموت — بينما انخفضت البروتينات الواقية مثل Bcl‑2. تشير هذه التغيرات مجتمعة إلى أن خلايا بطانة القرنية المتعرضة للإجهاد في FECD تتجه نحو استماتة مدفوعة بالميتوكوندريا، وهي شكل مرتب لكن نهائي من الانتحار الخلوي المبرمج.
توقف نظام التنظيف تحت الإجهاد المزمن
عادةً تُزال الميتوكوندريا المتضررة بشدة عبر عملية التدوير الذاتية تسمى الميتوفاجي، حيث تُعلَّم وتُحاط في حويصلات صغيرة للتخلص منها. وجد الفريق أن جزيئات بدء الميتوفاجي المبكرة (Parkin وLC3) تنشط في كل من الخلايا الطبيعية والشبيهة بـ FECD، لا سيما بعد التعرض للإجهاد. لكن البروتينات الداعمة الأساسية كانت منخفضة، وأظهرت الميكروسكوب الإلكتروني تراكم ميتوكوندريا مهضومة جزئياً محبوسة في الحويصلات. يشير ذلك إلى أنه بينما تبدأ عملية التنظيف، فإنها تفشل في الاكتمال، تاركة الخلايا مليئة بمحطات طاقة معطوبة تزيد الإجهاد والميل إلى الموت بدلاً من التعافي.
إيقاف ATF4 لإنقاذ الخلايا
لاختبار ما إذا كان ATF4 يقود هذه الدوامة، استخدم الباحثون حمض ريبونوكلييك صغير معرقل (siRNA) لكتم ATF4 جزئياً في خلايا بطانة القرنية المزروعة. تحت نفس الإجهاد المزمن، أظهرت الخلايا ذات ATF4 المخفض مستويات أدنى من بروتينات تعزيز الموت، وجهد غشاء ميتوكوندريا أكثر صحة، وتفتتاً أقل، وبقائية أفضل في اختبارات الصلاحية. والأهم أن عدد هياكل الميتوفاجي المتوقفة انخفض، ما يوحي بأن خفض ATF4 ساعد في استعادة توازن أكثر فاعلية بين التلف والتنظيف. في الفئران المهندسة لتحمل نسخة واحدة عاملة فقط من جين ATF4، أدى التعرض لأشعة UVA إلى تنشيط أقل لبروتين الشريك المعزز للموت CHOP، وحافظ على خلايا بطانة بشكل أكثر طبيعية مقارنة بالفئران التي تملك ATF4 بكامل وظائفه.
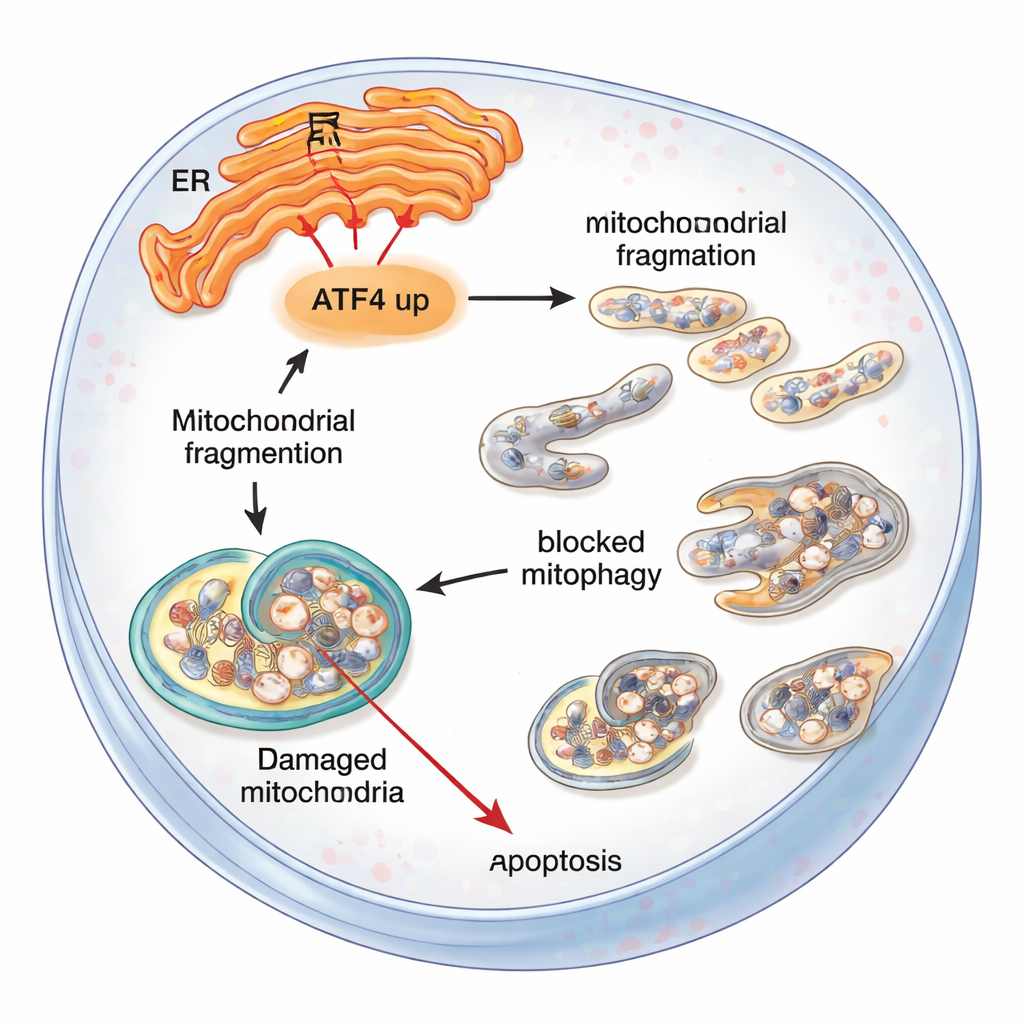
ماذا يعني هذا للأشخاص المصابين بـ FECD
لغير المتخصصين، الرسالة أن مراسل إجهاد واحد، ATF4، قادر على أن يقلب خلايا بطانة القرنية من حالة التكيّف إلى الانهيار. عندما يستمر إجهاد الشبكة الإندوبلازمية لفترة طويلة، يساهم ATF4 في تعطيل الميتوكوندريا، ويعطل آلة تنظيف الخلايا، وفي النهاية يحفز هذه الخلايا الحيوية على الانتحار المبرمج. إن تقليل نشاط ATF4 — سواء جينياً في الفئران أو بأدوات جزيئية مستهدفة في الخلايا — يحمي الميتوكوندريا، ويحسن إزالة النفايات، ويُبقي مزيداً من الخلايا على قيد الحياة. وبينما لا تزال هذه النتائج في مرحلة المختبر والحيوانات، فإنها تبرز ATF4 ومسارات الإجهاد المرتبطة به كأهداف دوائية واعدة قد تبطئ أو تمنع تقدّم اعتلال فوكس وتخفّض حاجة زرع القرنية في المستقبل.
الاستشهاد: Qureshi, S., Kim, S.Y., Lee, S. et al. ATF4 regulates mitochondrial dysfunction and mitophagy, contributing to corneal endothelial apoptosis. Sci Rep 16, 5960 (2026). https://doi.org/10.1038/s41598-026-36453-x
الكلمات المفتاحية: اعتلال بطانة القرنية فوكس, بطانة القرنية, إجهاد الميتوكوندريا, الميتوفاجي, ATF4