Clear Sky Science · ar
حمض بيسودولاريك B يعزز الفيروفتوزيس في خلايا سرطان الرئة اعتمادًا على تنظيم صاعد للبقاء عبر JNK/ERK
مركب نباتي يستهدف أورام الرئة
لا يزال سرطان الرئة واحدًا من أخطر السرطانات عالميًا، ويعجز الكثير من المرضى عن الاستجابة للأدوية الحديثة أو يتعرضون لآثار جانبية خطيرة. تستكشف هذه الدراسة مادة طبيعية تسمى حمض بيسودولاريك B المستخلص من لحاء شجرة طبية صينية تقليدية لمعرفة ما إذا كانت قادرة على قتل خلايا سرطان الرئة بشكل انتقائي مع الحفاظ على أنسجة الرئة السليمة. يكشف الباحثون عن طريقة غير متوقعة يدمر بها هذا المركب الخلايا الورمية عبر تحفيز شكل خاص من موت الخلايا يعتمد على الحديد وتلف الدهون داخل الخلايا.
لماذا يهم مركب من لحاء شجرة
يحتاج الأطباء بشكل عاجل إلى علاجات جديدة قادرة على هزم الأورام المقاومة للأدوية دون إلحاق الضرر بالخلايا الطبيعية. قدمت الأدوية المستمدة من النباتات لنا بالفعل علاجات سرطانية مهمة مثل باكليتاكسيل وفينكريستين. أظهر حمض بيسودولاريك B تأثيرات مضادة للسرطان في عدة أنواع من الأورام، لكن آليته في سرطان الرئة كانت غير واضحة وأحيانًا متضاربة. هنا اختبر العلماء حمض بيسودولاريك B على خلايا سرطان الرئة البشرية والخلايا الشعب الهوائية الطبيعية في المختبر، ثم في فئران تحمل أورام رئوية بشرية، لرسم خريطة دقيقة لكيفية عمل هذا المركب الطبيعي.
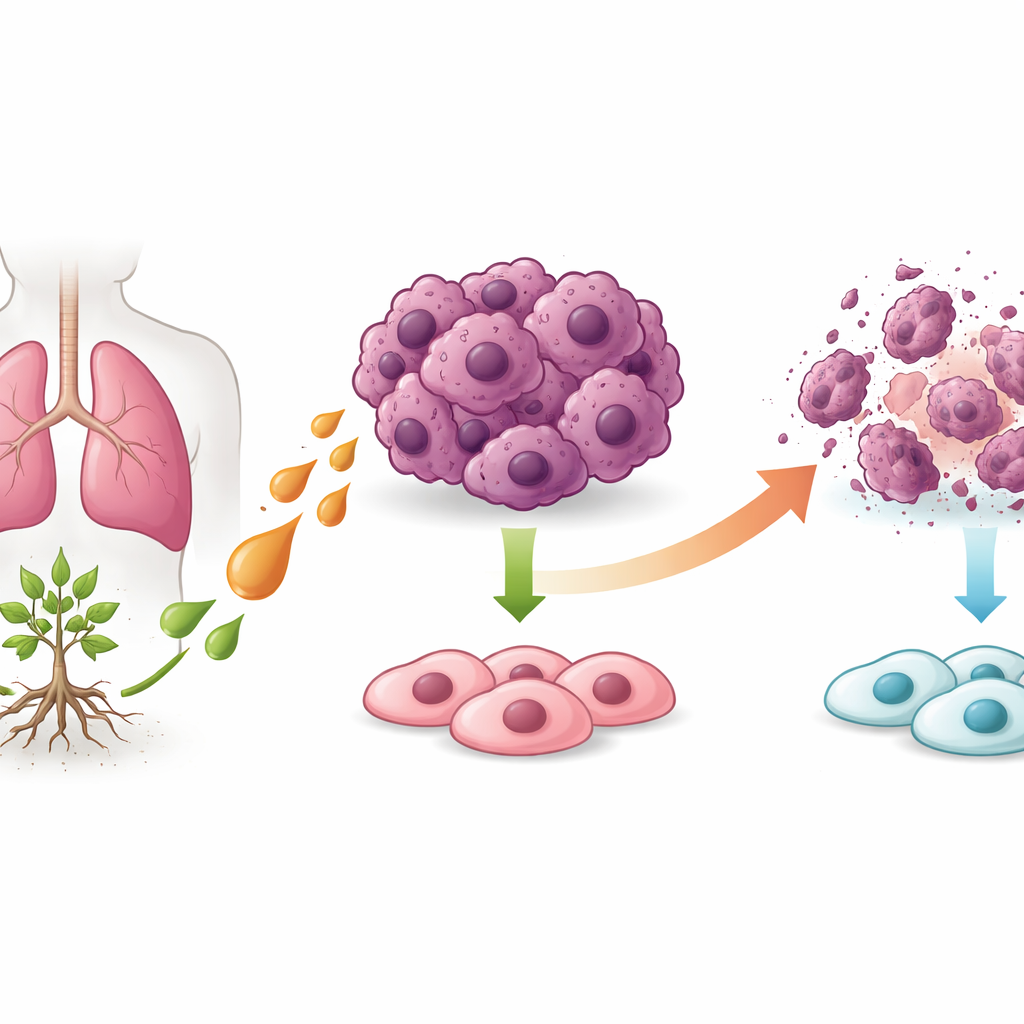
هجوم انتقائي على الخلايا السرطانية
في الزراعة الخلوية، أبطأ حمض بيسودولاريك B بقوة نمو خطيْن مختلفيْن من خلايا سرطان الرئة لكنه لم يؤثر كثيرًا على الخلايا الشعب الهوائية الطبيعية. توقفت الخلايا السرطانية المعالجة عن التكاثر، وفقدت قدرتها على تكوين مستعمرات كثيفة، وأظهرت علامات واضحة للتلف. ومن المثير للاهتمام أن شكلًا كلاسيكيًا من الانتحار الخلوي يسمى الاستماتة لعب دورًا ثانويًا فقط: لم تنقذ حجب إنزيمات الوفاة الرئيسية أو إيقاف عملية الاستحداث الذاتي (الأتوفاجي) الخلايا. في الوقت نفسه، انخفضت البروتينات المعروفة باسم «مثبطات الاستماتة» التي عادة ما تساعد الخلايا السرطانية على البقاء، مما يقترح أن الدواء كان يدفع الخلايا نحو مسار وفاة مختلف.
موت خلوي مدفوع بالحديد داخل الأورام
من خلال تحليل نشاط الجينات عبر الجينوم بأكمله، وجد الفريق أن العديد من الجينات المتأثرة تشير إلى الفيروفتوزيس، وهو نوع من موت الخلايا المنظم يقوده الحديد وتفكك دهون غشاء الخلية. ثم نظروا داخل الخلايا ورأوا علامات مميزة للفيروفتوزيس: ميتوكوندريا منكمشة ومُتلفة؛ مستويات عالية من أنواع الأكسجين التفاعلية؛ زيادة في الحديد الثنائي؛ ومزيد من الدهون المؤكسدة في أغشية الخلايا. كانت البروتينات الواقية الرئيسية التي تحرس عادةً ضد الفيروفتوزيس، مثل SLC7A11 وGPX4، منخفضة على مستوى البروتين والـRNA. عندما أضاف الباحثون دواءً مُخلِّبًا للحديد يعيق الفيروفتوزيس، انعكس موت الخلايا وتراكم الحديد وتلف الدهون بشكل قوي، مما يؤكد أن حمض بيسودولاريك B يقتل خلايا سرطان الرئة أساسًا عبر الفيروفتوزيس.
مساعد غير متوقع: سيرفايفين وإشارات خلوية
كانت إحدى المفاجآت سلوك بروتين يسمى سيرفايفين، من عائلة مثبطات الاستماتة نفسها. بينما انخفضت معظم بروتينات البقاء هذه بعلاج الدواء، ارتفعت مستويات سيرفايفين بشكل حاد على مستوى البروتين، رغم أن مستوى RNA الخاص به لم يتغير. عندما حجب العلماء سيرفايفين باستخدام مثبط جزيئي صغير أو RNA يقصّر التعبير الجيني، فقد حمض بيسودولاريك B كثيرًا من قوته القاتلة: نَجت خلايا سرطان الرئة بشكل أفضل، وانخفضت مستويات الحديد وتلف الدهون، وعادت البروتينات الواقية من الفيروفتوزيس. كشف تحليل المسارات أيضًا أن مسارين إشاريين داخل الخلايا، يعرفان باسم JNK وERK، أصبحا أكثر نشاطًا بعد العلاج. قلل تثبيط هذه الإشارات من الفيروفتوزيس، واستعاد بروتينات البقاء، وخفض مستويات سيرفايفين، مما يبيّن أن حمض بيسودولاريك B يحفز الفيروفتوزيس عبر محور JNK/ERK–سيرفايفين.
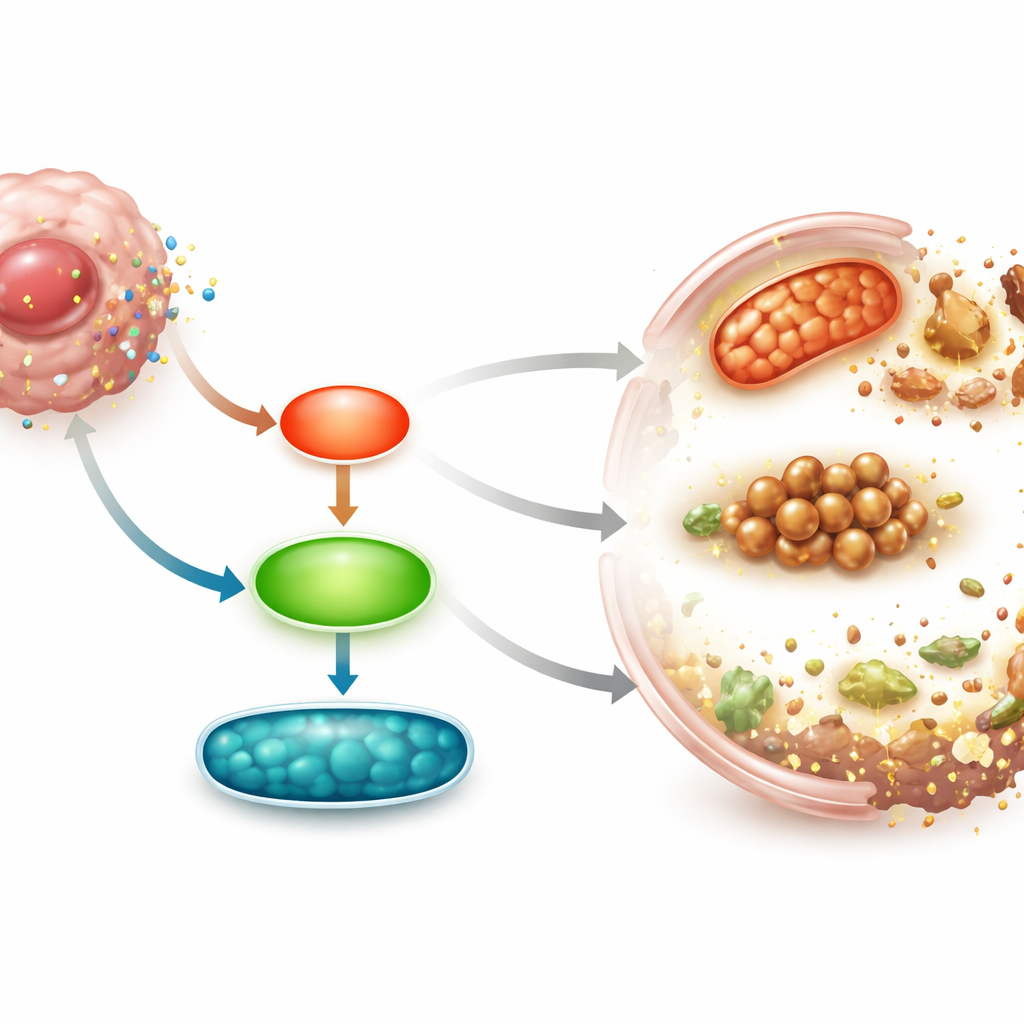
من الأطباق إلى الأورام الحية
لاختبار ما إذا كانت هذه التأثيرات تنطبق في كائن حي، زرع الفريق خلايا سرطان رئة بشرية في فئران لنمو أورام صغيرة. أبطأ العلاج اليومي بحمض بيسودولاريك B نمو الأورام بشكل كبير دون أن يسبب فقدان وزن واضحًا أو علامات سمية أخرى. حملت عينات الأورام من الحيوانات المعالجة مستويات عالية من علامة تلف الدهون، وزيادة في سيرفايفين، وانخفاضًا في الخلايا المنقسمة، وجميعها متسقة مع حدوث الفيروفتوزيس المستمر وتراجع نشاط الورم. تطابقت هذه النتائج داخل الجسم مع تجارب المختبر ودعمت فكرة أن المركب النباتي يمكن أن يحد من نمو الورم عن طريق دفع موت الخلايا المعتمد على الحديد.
ما الذي يعنيه هذا لعلاجات المستقبل
بشكل عام، تظهر الدراسة أن حمض بيسودولاريك B يمكنه قتل خلايا سرطان الرئة انتقائيًا عن طريق دفعها نحو الفيروفتوزيس، شكل من أشكال موت الخلايا يغذِّيه الحديد وتلف الأغشية، بدلاً من الاعتماد بشكل رئيسي على الاستماتة التقليدية. يعتمد هذا التأثير على سلسلة إشارات تشمل بروتينات JNK وERK وارتفاع غير متوقع في بروتين البقاء سيرفايفين، الذي يصبح في هذا السياق أساسيًا لسير الفيروفتوزيس. وبينما تبقى كثير من الأعمال قبل أن يُختبر هذا المركب على المرضى، تشير هذه النتائج إلى أن استغلال الفيروفتوزيس بعناية، وربما باستخدام جزيئات مستمدة من النباتات، يمكن أن يفتح مسارات جديدة لعلاج سرطانات الرئة العنيدة.
الاستشهاد: Li, Y., Yu, C., Yang, S. et al. Pseudolaric acid B promotes lung cancer cells ferroptosis depending on JNK/ERK-mediated upregulation of survivin. Sci Rep 16, 8294 (2026). https://doi.org/10.1038/s41598-026-36423-3
الكلمات المفتاحية: سرطان الرئة, حمض بيسودولاريك B, الانتحار الخلوي الفيروفتوزي, سيرفايفين, إشارات MAPK