Clear Sky Science · ar
من النمذجة الحاسوبية QSAR إلى اختبار MTT المختبري: التحقق التجريبي من قادة جزيئات جديدة تستهدف uPAR لسرطان الثدي ثلاثي السلبي والسرطانات الجلدية
لماذا يهم هذا البحث
تُعرف سرطانات مثل سرطاني الثدي ثلاثي السلبي وبعض سرطانات الجلد بصعوبتها في المعالجة لأنها تنتشر بسرعة وغالبًا ما تقاوم العلاجات القياسية. يستكشف هذا البحث هدفًا واعدًا جديدًا على سطح الخلايا السرطانية — يُسمى uPAR — ويُظهر كيف يمكن أن يكشف الجمع بين تصميم الأدوية الحاسوبي والتجارب المخبرية عن مرشحين دوائيين جدد قد يبطئون أو يوقفون انتشار هذه الأورام العدوانية.
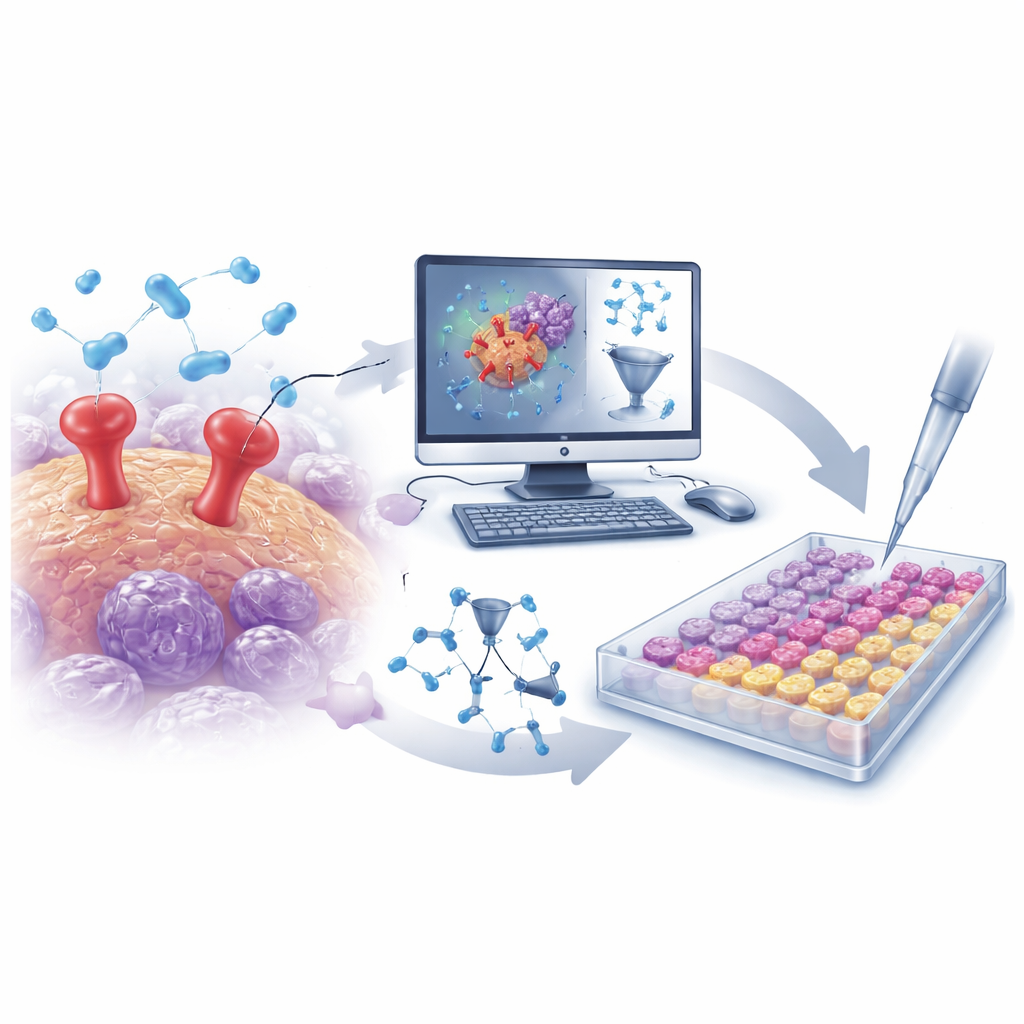
مدخل يساعد السرطان على الانتشار
لكي يصبح الورم مميتًا، يجب على خلاياه أن تنفصل عن موضعها الأصلي، وتقوّي النسيج المحيط، وتدخل مجرى الدم، وتستعمر أعضاء بعيدة. يلعب uPAR دورًا مساعدًا رئيسيًا في هذه العملية. يجلس على سطح الخلية السرطانية ويتعاون مع بروتينات شريكة لتنشيط إنزيمات تذيب البنية الداعمة المحيطة، مما يسهل تحرك الخلايا وغزوها. يوجد uPAR بمستويات مرتفعة بشكل خاص في خلايا سرطان الثدي ثلاثي السلبي وبعض خلايا سرطان الجلد، وترتبط كثافته بنمو أسرع وغزو أكبر ونتائج أسوأ للمرضى. وبسبب ذلك، يُعتبر uPAR هدفًا جذابًا — وإن كان حتى الآن غير مستغَل بالكامل — للأدوية المضادة للسرطان.
التنقيب في بيانات كيميائية كبيرة باستخدام خوارزميات ذكية
بدأ الباحثون بجمع مجموعة كبيرة تضم أكثر من 500 جزيء معروف يعيق uPAR من قاعدة بيانات عامة. تُرجمت بنية كل جزيء إلى آلاف الوصفات الرقمية التي تلتقط خصائص مثل الحجم والشكل وتوزيع الشحنة والمرونة. باستخدام هذه البيانات، بنا الفريق نموذج علاقة كمية بين البنية والنشاط (QSAR) — وهو أداة رياضية تتعلم أي الخصائص البنيوية تجعل الجزيء مثبطًا أقوى لـ uPAR. بعد التحقق الدقيق لتجنب الملاءمة المفرطة، أظهر النموذج قدرة تنبؤية عالية على المركبات غير المرئية سابقًا، مُبرزًا عدة ميزات رئيسية إما تقوّي أو تضعف قدرة إيقاف uPAR. وقد وجهت هذه الرؤى البحث عن جزيئات جديدة مصممة بشكل أفضل.
من الفحوصات الافتراضية إلى الاختبارات الحقيقية
مسلحًا بنموذج QSAR المدرب، فحص الفريق افتراضيًا مكتبة مركزة تضم نحو 30,000 جزيء يهاجم البروتيازات. سرّع النموذج تضييق هذه المجموعة الضخمة إلى مجموعة صغيرة من المثبطات المحتملة لـ uPAR. بالتوازي، استُخدمت محاكاة التراصف الحاسوبي لمعرفة مدى ملاءمة كل مرشح لموقع الارتباط في uPAR، واختبرت محاكيات الديناميكا الجزيئية ما إذا كانت هذه المجمعات المرتبطة ستبقى مستقرة مع مرور الزمن. من هذه الحملة الافتراضية المشتركة، برزت جزيئتان مميزتان: D685‑0061، الذي حدده نموذج QSAR كجزيء شديد الفعالية، وC878‑1660، الذي برز في التراصف والمحاكاة لتكوينه تفاعلات مستقرة بشكل خاص مع uPAR.
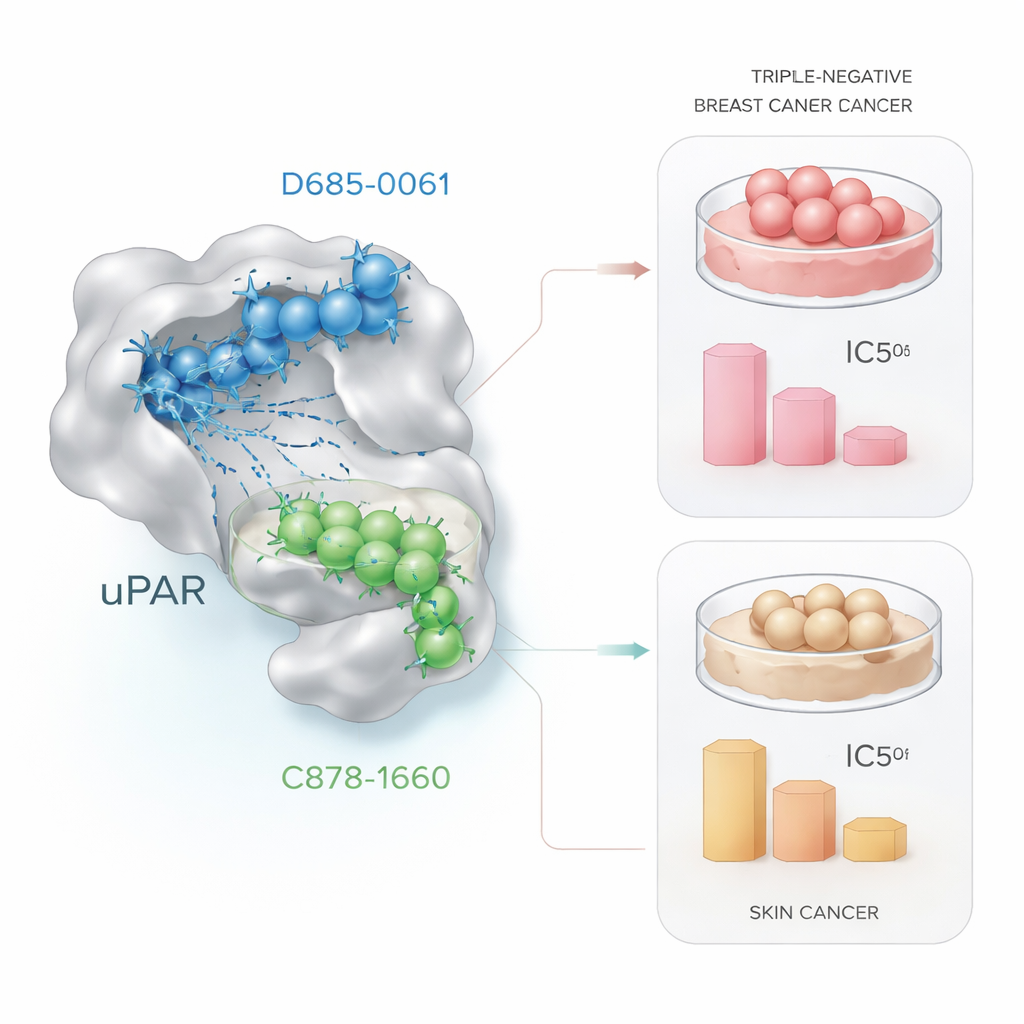
اختبار المرشحين في خلايا سرطانية
الوعد الحاسوبي لا يكتسب معنى إلا إذا ترجَم إلى تأثيرات بيولوجية حقيقية. لاختبار ذلك، عرّض الباحثون خلايا سرطانية حية لجرعات متزايدة من الجزيئين الرائدين وقاسوا بقاء الخلايا باستخدام طريقة مخبرية معيارية تُسمى اختبار MTT. في خلايا سرطان الثدي ثلاثي السلبي (MDA‑MB‑231)، قضى D685‑0061 على الخلايا بكفاءة أكبر، فخفض قابلية البقاء إلى النصف عند نحو 21 ميكرومول، في حين تطلَّب C878‑1660 كمية تقارب أربعة أضعاف ذلك. وتحت المجهر، أظهرت الخلايا المعالجة بـ D685‑0061 علامات واضحة للموت المبرمج، مثل الالتفاف، والانفصال عن السطح، والتحلل إلى شظايا. بالمقابل، في خلايا سرطان الجلد (A431)، كان C878‑1660 القاتل الأقوى، محققًا 50% موتًا للخلايا عند نحو 19 ميكرومول مقارنةً بحوالي 28 ميكرومول لـ D685‑0061، ومع ضرر مرئي يعتمد على الجرعة.
ماذا يعني هذا لعلاجات السرطان المستقبلية
لا يقدم هذا العمل دواءً جديدًا فوريًا، لكنه يقدم نقطتي انطلاق واعدتين، وبنفس الأهمية، مخططًا قويًا للعثور على المزيد. بربط نمذجة البيانات الكبيرة، والمحاكاة ثلاثية الأبعاد، والتجارب الخلوية الدقيقة، تُظهر الدراسة أن uPAR يمكن استهدافه انتقائيًا بجزيئات صغيرة تضر خلايا سرطان الثدي والجلد العدوانية. تعمل D685‑0061 وC878‑1660 الآن كمركبات رائدة يمكن للكيميائيين تنقيحها لزيادة الفعالية، وتحسين السلامة، وتعزيز خواصها الحركية في الجسم. على المدى الأطول، قد تساعد أدوية مبنية على هذا النهج على حجب انتشار السرطانات المدفوعة بـ uPAR، مما يجعل بعض الأورام الأكثر خطورة اليوم أمراضًا أكثر قابلية للإدارة.
الاستشهاد: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
الكلمات المفتاحية: مثبطات uPAR, سرطان الثدي ثلاثي السلبي, سرطان الجلد, تصميم الأدوية بمساعدة الحاسوب, اختبار قابلية بقاء الخلايا MTT