Clear Sky Science · ar
دراسة في نظرية الدالة الكثافية لامتصاص السيكلوفوسفاميد والبيرينيثول على إطار ثلاثي آزيني تساهمي (CTF-2) لتطبيقات توصيل الأدوية
لماذا يهم تطوير العلاج الكيميائي بذكاء
أدوية العلاج الكيميائي تنقذ الأرواح، لكنها غالبًا ما تعمل كمصباح كاشف بدلاً من أن تكون بقعة مضيئة—تهاجم الخلايا السليمة جنبًا إلى جنب مع الخلايا السرطانية. يمكن أن يؤدي ذلك إلى آثار جانبية خطيرة، من التعب والالتهابات إلى تلف الأعضاء. تستكشف الدراسة المعروضة هنا مادة فائقة الرقة وعالية المسامية تُسمى إطار ثلاثي آزيني تساهمي (CTF-2) كـ «إسفنجة ذكية» يمكنها حمل عقاريْن مضادين للسرطان مستخدمين منذ وقت طويل—السيكلوفوسفاميد والبيرينيثول—بشكل أكثر أمانًا وكفاءة إلى المواقع المطلوبة، ثم إطلاقهما في ظل ظروف تشبه بيئة الورم.
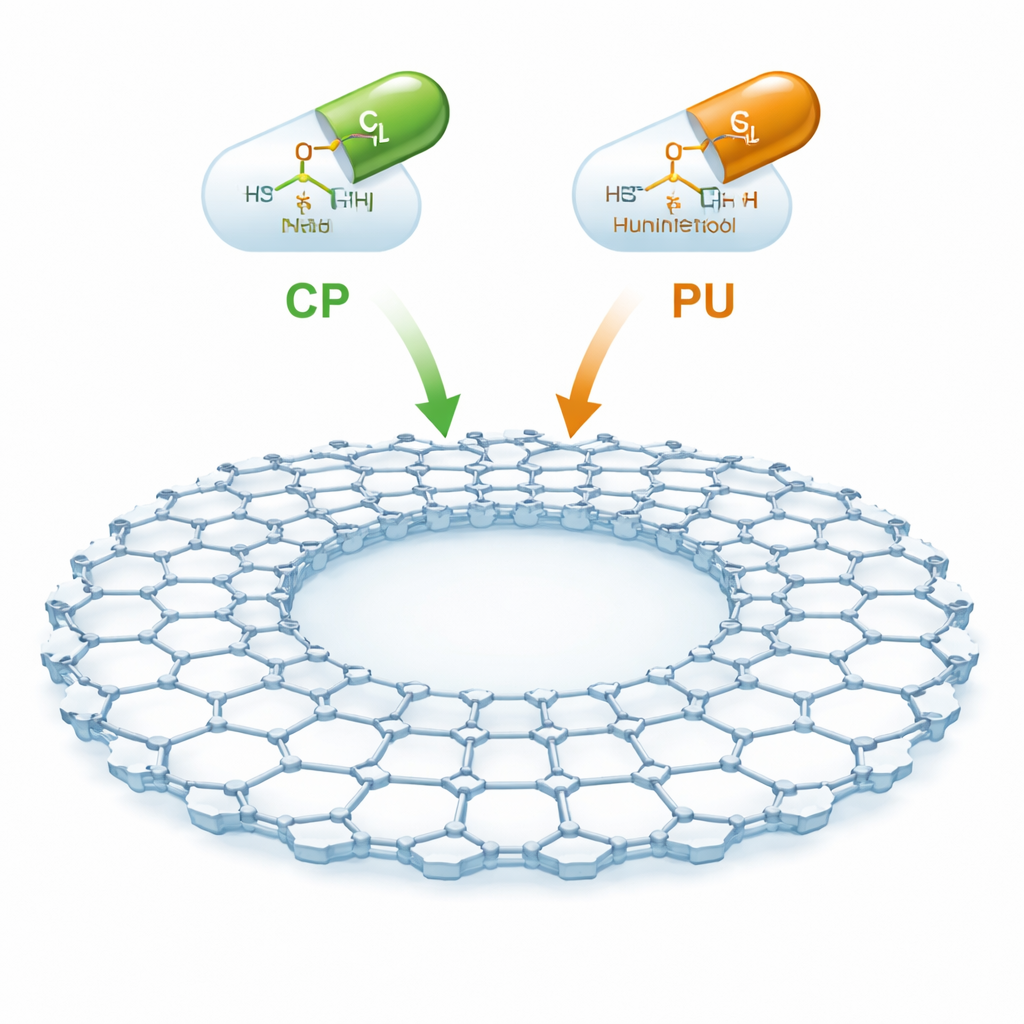
نوع جديد من الإسفنج الجزيئي
CTF-2 مادة صناعية مبنية من حلقات من الكربون والنيتروجين مرتبطة في شبكة مسطحة تشبه الصفائح تحتوي على تجويف مركزي كبير والكثير من الفراغ المفتوح. وبفضل رقتها وثباتها وغناها بالمسام، توفر مساحة سطحية داخلية هائلة لالتقاط جزيئات الدواء. ركز المؤلفون على دوائين سرطانيين مهمين: السيكلوفوسفاميد، المستخدم على نطاق واسع لأورام الدم والأورام الصلبة، والبيرينيثول (المعروف أيضًا بالمركابتوبورين)، المستخدم ضد اللوكيميا وبعض أمراض الأمعاء الالتهابية. الفكرة هي تثبيت هذه الأدوية بلطف على سطح CTF-2 حتى يمكن حملها عبر مجرى الدم وإطلاقها بشكل أكثر انتقائية، مما يقلل الضرر الذي يلحق بالأنسجة السليمة.
استكشاف ما لا يُرى بتجارب حاسوبية
بدلاً من العمل في مختبر رطب، استخدم الفريق حسابات حاسوبية متقدمة على مستوى الكم (نظرية الدالة الكثافية وطرق ذات صلة) لطرح سؤالين رئيسيين: مدى قوة انجذاب كل دواء إلى CTF-2 وما الذي يُثبت هذه المعقدات معًا. قاموا بتحسين أشكال CTF-2 مع كل دواء، وقياس المسافات بين الذرات عند نقاط التلامس، وحساب مقدار الطاقة المكتسبة عند التصاق الدواء بالإطار. بالنسبة للسيكلوفوسفاميد، كانت طاقة الامتصاص المحسوبة نحو −1.04 إلكترون فولط، أقوى قليلًا من −0.82 إلكترون فولط المحسوبة للبيرينيثول. تُشير هذه القيم، التي تبقى ملائمة بوضوح حتى بعد تصحيح الأخطاء التقنية ومحاكاة الماء كمذيب، إلى أن كلا الدوائين يرتبطان بقوة كافية للتحميل لكن ليست بقوة تمنع إطلاقهما لاحقًا.
قوى لطيفة تقوم بعمل مهم
تُظهر الدراسة أن «الغراء» بين الأدوية وCTF-2 ليس رابطًا كيميائيًا صلبًا بل شبكة من قوى غير تساهمية لطيفة. باستخدام تحليلات متخصصة لكثافة الإلكترون—وهي في الأساس خرائط لمواقع الإلكترونات المشتركة—وجد الباحثون أن قوى فان دير فالس الجاذبة (نفس القوى الضعيفة التي تسمح لسحالي الغِيكو بالتسلق) والتفاعلات الكهروستاتيكية الخفيفة هي المسيطرة. تحدث هذه التفاعلات على مسافات قصيرة لكنها غير رابطة بين ذرات الهيدروجين والنيتروجين والأكسجين والكبريت والكربون في الأدوية وعلى الإطار. أكدت حسابات إضافية قسمت الجذب الكلي إلى مكونات مختلفة أن القوى الكهروستاتيكية وقوى التبعثر (فان دير فالس) توفر معظم الجذب المثبت، بينما تمنع القوى التنافرية الدواء من الغوص بعمق شديد أو الارتباط بشكل لا رجعة فيه.
دلالات التحميل المستقر والإطلاق القابل للضبط
كما فحص الفريق كيفية انتقال الإلكترونات عندما تجلس الأدوية على CTF-2، وكيف يغير ذلك الخصائص الكهربائية الأساسية. لوحظت انتقالات شحنات صغيرة لكنها واضحة بين كل دواء والإطار وتضيق طفيف في الفجوة الطاقية التي تفصل الحالات الإلكترونية المملوءة عن الفارغة. وهذا يوحي بأن تفاعلية وموصلية المادة تنضبط بشكل طفيف عند التحميل، وهي سمة مفيدة لأي تطبيق مستقبلي في الاستشعار أو العلاج المشترك والتشخيص. والأهم من ذلك، عندما محاكوا بيئة أكثر حموضة كما هو الحال بالقرب من الأورام بإضافة بروتونات إضافية، ضعُف الارتباط المحسوب وزادت مسافات التماس. بعبارة بسيطة، تقترح المحاكاة أن CTF-2 يمكن أن يحتفظ بالأدوية في ظروف تشبه الدم العادية، لكنه يميل إلى إطلاقها بسهولة أكبر في بيئات حمضية تشبه الورم—وهو السلوك المرغوب لتوصيل مستهدف.
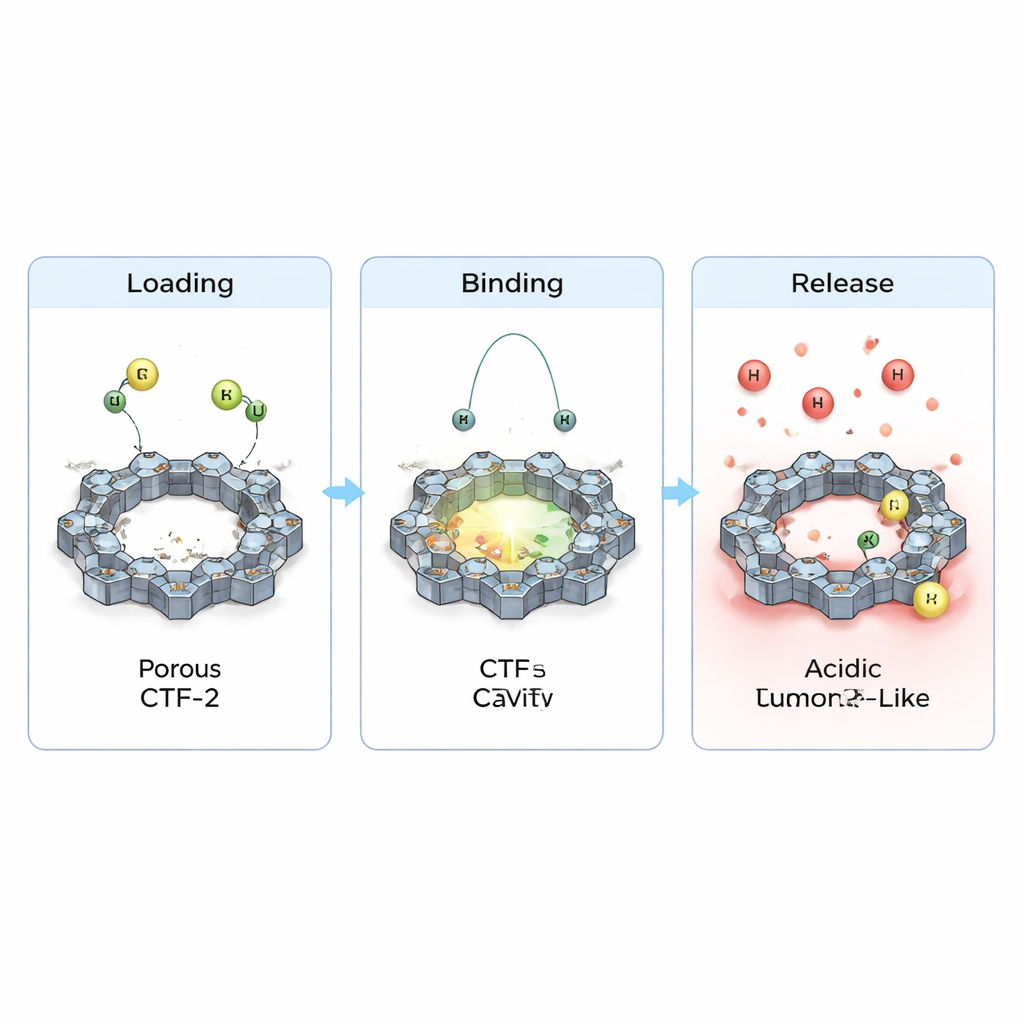
ماذا يعني هذا لعلاجات السرطان المستقبلية
بشكل مجمل، ترسم هذه الحسابات صورة لـ CTF-2 كحامل واعد للسيكلوفوسفاميد والبيرينيثول: يمكنه تعبئتهما على سطحه المسامي بطريقة مستقرة، وحمايتهما أثناء التداول الدموي، ثم إطلاقهما عندما يتغير الكيمياء المحلية حول الورم. وعلى الرغم من أن العمل نظري وسيحتاج إلى تأكيد تجريبي، فإنه يشير إلى أن الأُطر المصممة بعناية والغنية بالنيتروجين مثل CTF-2 قد تساعد في تحويل أدوية كيميائية قديمة لكنها فعالة إلى أدوية أكثر ذكاءً—تسليم جرعات قوية إلى حيث تكون الحاجة أكبر مع تقليل الأضرار الجانبية للخلايا السليمة.
الاستشهاد: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
الكلمات المفتاحية: حامل نانوي, توصيل الأدوية, علاج السرطان الكيميائي, إطار ثلاثي آزيني تساهمي, النمذجة الحاسوبية