Clear Sky Science · ar
إطار تعلم عميق متسلسل تفاعلي مع تحسين خبير لتقسيم مناطق المخيخ الدقيقة بدقة
لماذا يهم رسم خرائط المناطق الدماغية الصغيرة
السترياتوم، تركيب صغير مدفون عميقاً في الدماغ، يلعب دوراً مركزياً في الحركة والتحفيز ويتأثر بشدة في اضطرابات مثل مرض باركنسون. غالباً ما يستخدم الأطباء مسحات PET وMRI لقياس التغيرات الكيميائية في هذه المنطقة، لكن السترياتوم مقسّم إلى العديد من المناطق الفرعية الصغيرة التي يصعب رؤيتها وتحديدها بدقة. تقدم هذه الورقة طريقة جديدة بمساعدة الحاسوب، تسمى StriaSeg‑iARM، تساعد الأخصائيين على رسم هذه الحدود بدقة وكفاءة أكبر، حتى لدى الأشخاص الذين تغيرت أدمغتهم بفعل التقدّم في السن أو المرض.
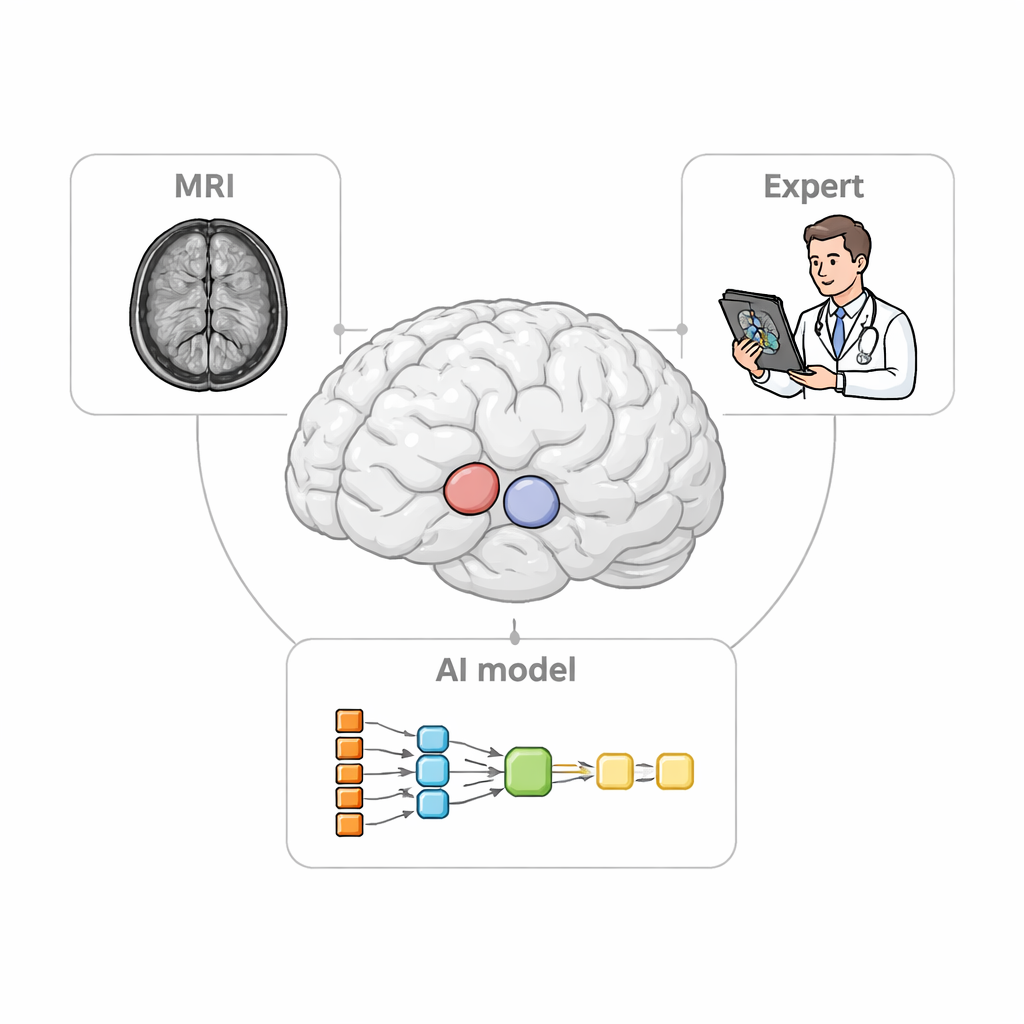
المشكلة السريرية الظاهرة للعيان
عندما يقيم أطباء الأعصاب حالات مثل مرض باركنسون، يعتمدون على مسحات PET لتتبع كيف تتغير الإشارات المرتبطة بالدوبامين عبر أجزاء مختلفة من السترياتوم. وللقيام بذلك بشكل صحيح، يجب أولاً تحديد «مناطق الاهتمام» الثلاثية الأبعاد الصغيرة على صور MRI، والتي تعمل كأوعية قياس لبيانات PET. إن الرسم اليدوي لهذه المناطق عمل بطيء وممل وقد يختلف من خبير لآخر. البرامج الحالية يمكن أن تحدد تلقائياً الهياكل الأكبر فقط وغالباً ما تواجه صعوبة مع المرضى الذين تقلصت أدمغتهم أو تشوّهت، وهو وضع شائع في المراحل المتقدمة للأمراض العصبية التنكسية. هذه النقائص يمكن أن تطمس نمط التلف الحقيقي وتقلل من فاعلية التصوير كأداة تشخيصية.
مساعد أذكى على مرحلتين
صمم الباحثون StriaSeg‑iARM كنظام تعلم عميق من مرحلتين يعمل مباشرة في فضاء دماغ كل شخص بدلاً من إجبار المسحة على قالب معياري. في المرحلة الأولى، يحدد البرنامج السترياتوم العام على صورة MRI ثلاثية الأبعاد. في المرحلة الثانية، يقسم هذا التركيب إلى 12 منطقة فرعية محددة تشريحياً على جانبي الدماغ. وبين هاتين المرحلتين يكمن الابتكار الرئيسي: خطوة تفاعلية يمكن للخبير من خلالها فحص وإصلاح المخطط الخشن الذي أنتجته المرحلة الأولى بسرعة، إذا لزم الأمر، قبل إجراء التقسيم الأدق. هذا النهج يمزج سرعة الأتمتة مع حكم المراقب البشري المدرب.
التدريب والاختبار على أدمغة العالم الحقيقي
لتعليم النظام ما يبحث عنه، جمع الفريق مئات صور MRI من مستشفيات وأنواع أجهزة مسح متعددة، وأنشأوا رسوماً يدوية دقيقة للـ12 منطقة فرعية في السترياتوم. ثم اختبروا النموذج على مجموعتي بيانات خارجيتين تضمّان كل من MRI ومسحات PET المرتبطة بالدوبامين: إحداهما من مرضى باركنسون في مراحل مبكرة إلى جانب متطوعين أصحاء، والأخرى من مجموعة سريرية أكبر سناً وأكثر تأثراً بتقلص في الدماغ وتشخيصات مختلطة. عبر هذه الحالات الصعبة، طابق StriaSeg‑iARM باستمرار الرسوم اليدوية للخبراء أفضل من الطرق القائمة على الأطلس ونموذج التعلم العميق أحادي المرحلة، مع تداخل أعلى، وحدود أكثر دقة، وقياسات حجم مستقرة.
قياسات أدق لمسحات كيمياء الدماغ
بما أن الهدف النهائي هو كمية إشارات PET، فحص المؤلفون أيضاً كيف تؤثر طرق التقسيم المختلفة على قراءات PET. باستخدام مقياس معيار لالتصاق المُتتبِّع في كل منطقة فرعية، قارنوا النتائج التلقائية بتلك المستندة إلى الرسوم اليدوية. ميّلت طريقة الأطلس إلى التقليل من الالتصاق، خاصةً لدى المرضى ذوي التغيرات الأشد، بينما أظهر نموذج التعلم العميق الأساسي تحيّزاً ملحوظاً في بعض المناطق. في المقابل، قدمت النماذج المتسلسلة—وخاصة عند استخدام خطوة التصحيح التفاعلية—قيم PET تقارب مرجع الخبير إلى حد كبير، مع تحيّز وتشتت أدنى. كما أظهر الفريق أن درجة بسيطة لقياس عدم اليقين من المرحلة الأولى يمكن أن تميّز نحو ربع أصعب الحالات التي تحتاج فعلاً إلى تنقيح خبير، مما يبقي الباقي آلياً تماماً.
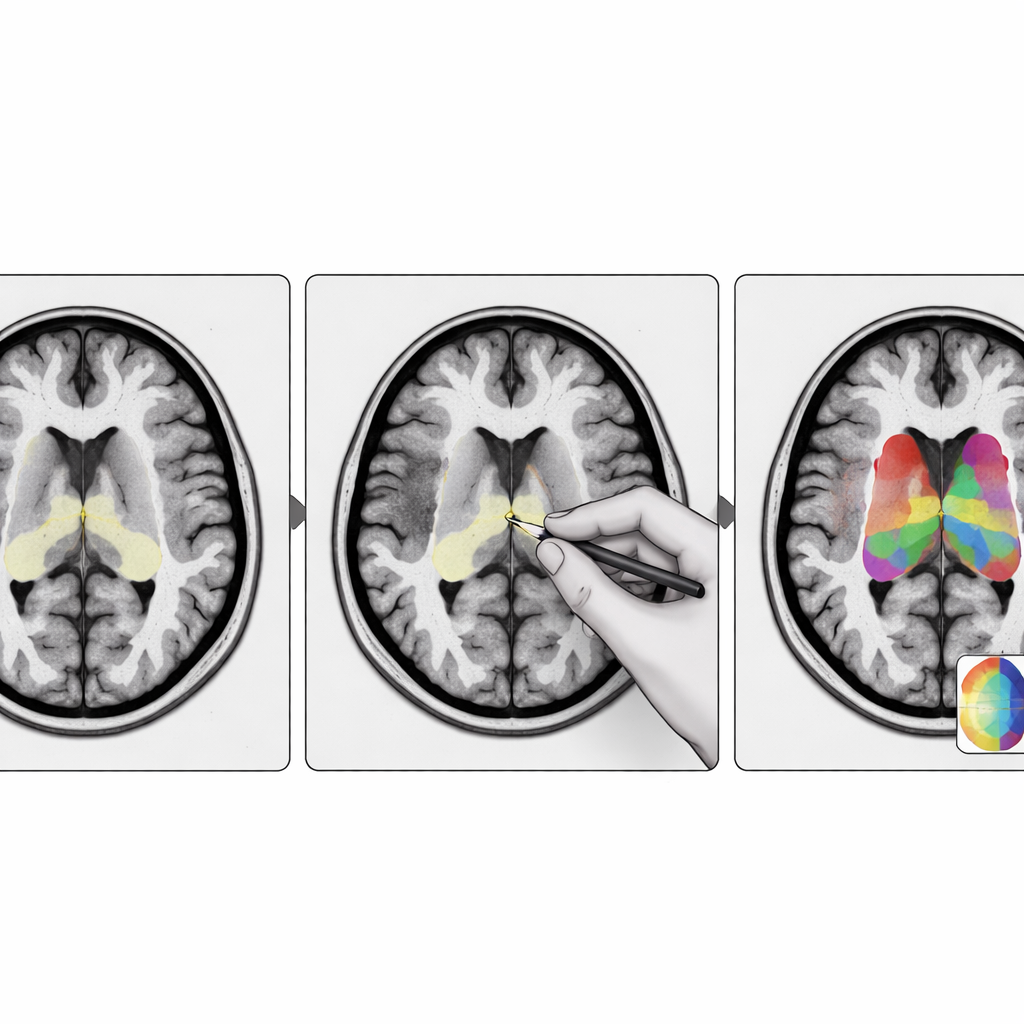
ما الذي يعنيه هذا للمرضى والأطباء
بالنسبة لغير المتخصصين، الخلاصة أن خرائط رقمية أفضل للمناطق الدماغية الصغيرة يمكن أن تجعل مسحات كيمياء الدماغ أكثر موثوقية. يوفر StriaSeg‑iARM إطاراً مرناً يقوم فيه نموذج التعلم العميق بمعظم العمل، لكن لا يزال بإمكان الأخصائيين التدخّل لتصحيح الحالات المعقدة دون الحاجة إلى إعادة تدريب النظام. هذا المزيج من الأتمتة والإشراف الخبيري يحسّن دقة القياسات المستخدمة في تشخيص وتتبع اضطرابات مثل مرض باركنسون، ويمكن تكييفه أيضاً لأعضاء وأمراض أخرى حيث تحمل البنى الصغيرة صعبة الرصد أدلة حيوية.
الاستشهاد: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
الكلمات المفتاحية: تصوير مرض باركنسون, تقسيم النطاق المخطط, التعلم العميق في الأشعة, تصوير الرنين المغناطيسي وبوزيترون الدماغ, مؤشرات حيوية للأمراض العصبية التنكسية