Clear Sky Science · ar
تطبيق نهج الفرز الافتراضي عالي الإنتاجية (HTVS) لتحديد مثبطات لازتات ديهيدروجيناز (LDH) جديدة ذات خصائص مضادة للسرطان
لماذا يهم هذا البحث لعلاج السرطان
تعيد خلايا السرطان غالبًا توصيل طرق توليد الطاقة لديها، ويمكن استغلال هذا التحول لتصميم أدوية أكثر ذكاءً وانتقائية. تستكشف هذه الدراسة إنزيمًا استقلابيًا رئيسيًا يُدعى لازتات ديهيدروجيناز (LDH)، الذي يساعد الأورام على الازدهار في ظروف قاسية ومقاومة العلاج. باستخدام تقنيات فرز متقدمة قائمة على الحاسوب وتجارب مخبرية، حدد الباحثون جزيئتين صغيرتين جديدتين تُثبطان LDH وتظهران تأثيرات واعدة مضادة للسرطان في سلالات خلايا سرطان البروستات.
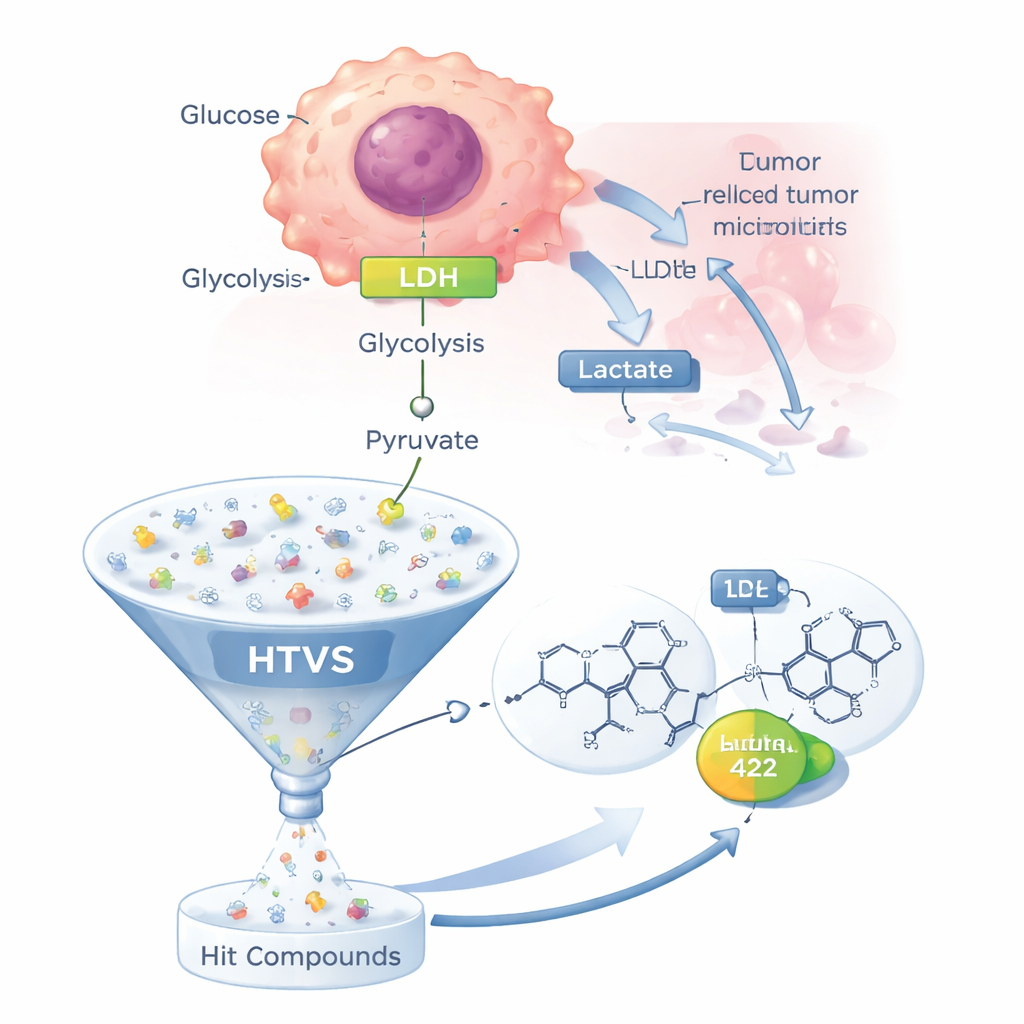
التمثيل الغذائي الغريب لخلايا السرطان
تستخدم معظم الخلايا السليمة الأكسجين بكفاءة في الميتوكوندريا لتوليد الطاقة. تعتمد العديد من خلايا السرطان، مع ذلك، بشكل كبير على مسار أقل كفاءة يسمى تحلل السكر (glycolysis)، حتى عندما يكون الأكسجين متوفرًا—وهي ظاهرة تُعرف بتأثير واربورغ. في هذا المسار المختصر، يتفكك الجلوكوز إلى بيروفات، والتي تتحول بعد ذلك إلى لاكتات بوساطة LDH بدل أن تُغذَّى إلى الميتوكوندريا. تُضخ اللاكتات خارج الخلية، مُحمِّضة محيط الورم، مما يساعد خلايا السرطان على تجنب الموت الخلوي، وإضعاف الاستجابة المناعية، وحتى تقليل فعالية العديد من أدوية الكيمياء العلاجية. وبما أن LDH يقع في قلب هذا التمثيل الغذائي المُعدل ولم يُوافق بعد على أي دواء يستهدفه، فقد أصبح هدفًا ذا أولوية عالية لتطوير علاجات مضادة للسرطان.
استخدام الحواسيب لتنقية نصف مليون جزيء
بدلاً من اختبار الأدوية المحتملة واحدًا تلو الآخر في المختبر، استخدم الفريق استراتيجية فرز افتراضي عالي الإنتاجية (HTVS). بدأوا بـ 28 جزيءًا معروفًا مبلّغًا عنها في الأدبيات العلمية وتسببوا منها في «فارفاخور» (pharmacophore)—نمط ثلاثي الأبعاد مجرد للميزات التي من المرجح أن تشترك فيها أي مثبط جيد لـ LDH. طبقوا بعد ذلك هذا النموذج على مكتبة تجارية تضم نحو 500,000 جزيء شبيه بالدواء، وسألوا أي المرشحين يتطابقون مع الميزات الأساسية. اجتاز نحو 110,000 جزيء هذا المرشح الأولي، وقيدت عملية الاختيار الإضافية المبنية على قواعد «ملاءمة الدواء» القياسية القائمة إلى 2,337 مرشحًا أكثر واقعية للربط الميكانيكي (docking) مع إنزيم LDH.
التركيز على أقوى الملتزمين
كانت الخطوة التالية تقدير مدى إحكام ملاءمة هؤلاء المرشحين لموقع الفعالية في LDH. باستخدام عدة مستويات من الربط الحاسوبي، حسب الباحثون كيف قد يتفاعل كل جزيء مع أحماض أمينية محددة داخل جيب الإنزيم. ضيق هذا الإجراء متعدد المراحل المجموعة تدريجيًا من آلاف المرشحين إلى 59 جزيئًا واعدًا، ثم إلى خمس «ضربات» واضحة ذات ارتباطات متوقعة قوية بشكل خاص. برز اثنان من هذه، الموسومان المركبان 15 و422، لأن محاكاة الديناميكيات الجزيئية القائمة على الحاسوب أشارت إلى أنهما يشكلان مركبات مستقرة للغاية مع LDH بمرور الوقت، محافظة على اتصالات أساسية مع بقايا حاسمة في موقع الفعالية مع الحفاظ على بنية بروتينية إجمالية معقولة.
من الفحص إلى خلايا السرطان الحية
للاطلاع على ما إذا كانت هذه الضربات مهمة في النظم الحية، اشترى العلماء المركبين 15 و422 واختبروهما في سلالات خلايا سرطان البروستات DU-145 وPC-3. كلتا المادتين حمّلتا نشاط LDH داخل الخلايا عند تراكيز نانومولية وأبطأتا أيضًا مباشرة نشاط إنزيم LDH المنقى، رغم أنهما كانا أقل فاعلية بعض الشيء من مثبط تجريبي معروف يُدعى GNE‑140. في اختبارات النمو، قللّت المركبات من بقاء خلايا السرطان عند جرعات ميكرومولية منخفضة، مقتربة مرة أخرى من أداء GNE‑140. أظهرت تجارب إضافية أن المعالجات زادت قليلًا الإجهاد التأكسدي، وأخلّت بالجهد الغشائي للميتوكوندريا—وهو علامة على تعطّل «مصانع الطاقة»—وأطلقت الخلايا المبرمجة للموت (الاستماتة) في خلايا DU‑145، وكان المركب 15 أكثر نشاطًا من بين الاثنين.
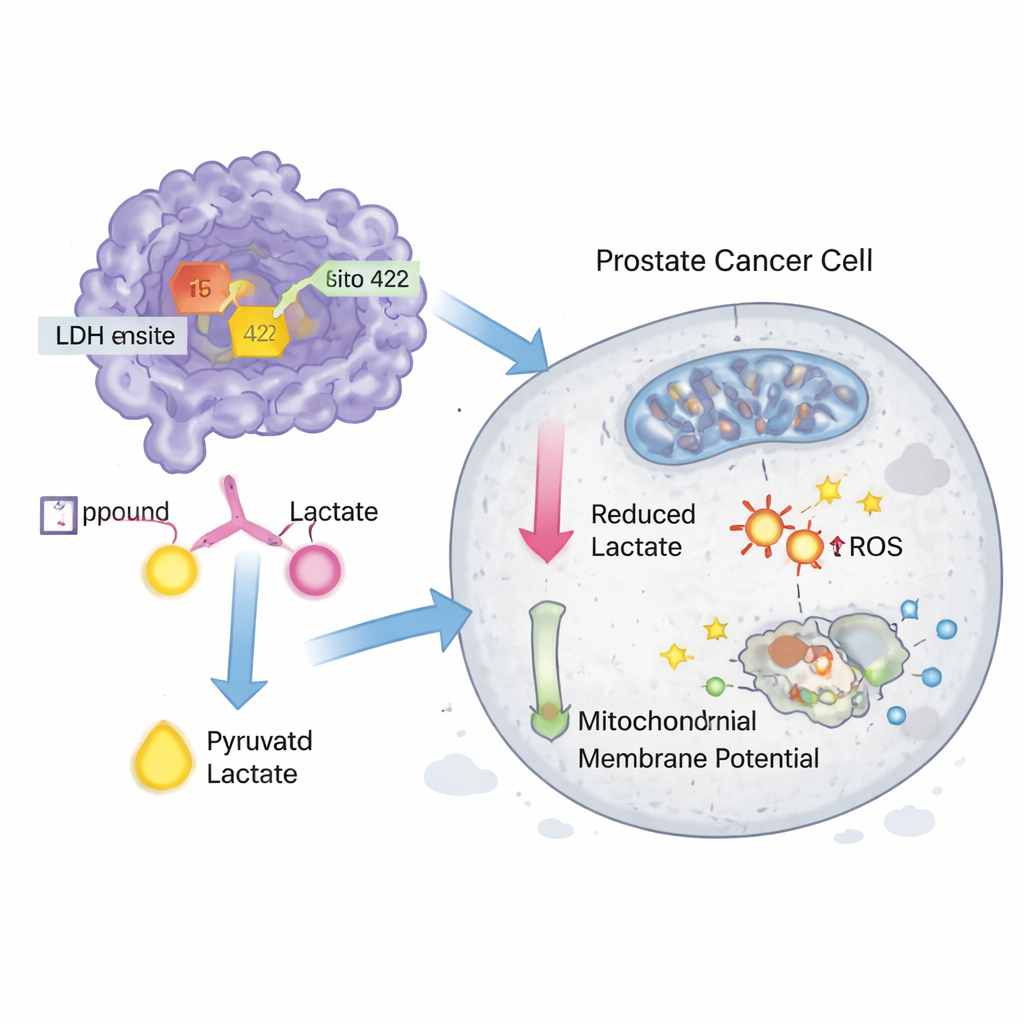
ماذا قد يعني هذا لأدوية السرطان المستقبلية
بينما هذه الجزيئات ليست أدوية جاهزة، فإنها توفر نقاط انطلاق قيِّمة لتصميم الأدوية. يمتلك كل من المركبين 15 و422 خصائص كيميائية توحي بتحسين الذوبان والنفاذية و«ملاءمة الدواء» العامة مقارنة ببعض مثبطات LDH الحالية، مما يجعلهما مرشحين جذابين لمزيد من التحسين. تُظهر الدراسة كيف يمكن للفرز الحاسوبي واسع النطاق، الموجَّه بميزات هيكلية معروفة، أن يكشف مثبطات LDH جديدة تضعف خلايا السرطان من خلال تجويع مصدر طاقتها المُعدّل. مع عمل مستقبلي لتحسين هياكلها، واختبار الارتباط المباشر بمزيد من الصرامة، ودراسة سلوكها في الحيوانات، قد تساهم هذه المركبات في فئة جديدة من العوامل المضادة للسرطان التي تهاجم الأورام عبر هشاشاتها الأيضية الفريدة.
الاستشهاد: Huang, Y., Benni, S., Yadav, U.P. et al. Deploying the high-throughput virtual screening (HTVS) approach for the identification of new lactate dehydrogenase (LDH) inhibitors with anticancer assets. Sci Rep 16, 5921 (2026). https://doi.org/10.1038/s41598-026-36385-6
الكلمات المفتاحية: مثبطات لازتات ديهيدروجيناز, تمثيل غذائي للسرطان, الفرز الافتراضي, سرطان البروستات, اكتشاف أدوية مضادة للسرطان