Clear Sky Science · ar
زيادة تعبير MGMT تتوسط مقاومة التيموزولوميد الناجمة عن اعتماد USP5
لماذا تتوقف بعض أورام الدماغ عن الاستجابة لدواء رئيسي
بالنسبة لمرضى سرطان الدماغ العدواني الغلِيُوبلاستومة، يعد التيموزولوميد واحدًا من الأدوية الرئيسية التي يعتمد عليها الأطباء. في البداية، قد يبطئ هذا العلاج الكيميائي تقدّم المرض، لكن الأورام غالبًا ما تتعلم كيف تتجاهله. تطرح هذه الدراسة سؤالًا ذا أثر عملي وحاسم: ما الذي يسمح لهذه الخلايا السرطانية بالهرب من الدواء بالضبط، وهل يمكننا اكتشاف نقاط ضعف جديدة لمهاجمتها ليعود العلاج فعّالًا؟
دواء يساعد في البداية ثم يفقد تأثيره
يعمل التيموزولوميد عن طريق إتلاف الحمض النووي للخلايا السرطانية سريعة الانقسام، مما يجبرها على الموت. ومع ذلك، تنتج العديد من أورام الغلِيُوبلاستومة بروتين إصلاح يُدعى MGMT يمكنه عكس هذا التلف. المرضى الذين تفعل أورامهم MGMT يميلون إلى الأداء الأسوأ لأن تأثير الدواء يُلغى. يستطيع الأطباء إلى حد ما التنبؤ بالاستجابة بفحص ما إذا كان جين MGMT مُطفأ كيميائيًا (مثيّل) أم مُشغّل (غير مثيّل)، لكن هذا لا يشرح تمامًا لماذا تتطوّر المقاومة أو كيف تظل مستويات MGMT مرتفعة داخل خلايا الورم مع مرور الوقت.
مساعدون خفيّون يحميان بروتين الإصلاح
نظر المؤلفون إلى طبقة تحكّم أخرى: «فرق التنظيف» الجزيئية التي تقرر أي البروتينات تُدمَّر وأيها تُنقَذ. عادةً ما تُعلّم الخلايا البروتينات البالية ليتم تفكيكها، بينما تستطيع مجموعة من الإنزيمات تُدعى إنزيمات إزالة اليوبيكيتين (DUBs) إنقاذ البروتينات من هذا المصير. من خلال تحليل قواعد بيانات سرطانية عامة كبيرة وفحص خطوط خلايا غلِيُوبلاستومة المقاومة للأدوية المزروعة في المختبر، حدّد الفريق اثنين من هذه الإنزيمات، USP5 وUSP8. في عينات أورام من مئات المرضى، مال مستوى USP5 العالي لأن يظهر مع مستويات MGMT الأعلى، والمرضى الذين كانت أورامهم تُظهر ارتفاعًا في كلا الجينين عمومًا توفوا أسرع.
بناء المقاومة في المختبر
لتقليد ما يحدث لدى المرضى، عرض الباحثون خطّي خلايا غلِيُوبلاستومة شائعين تدريجيًا لجرعات متزايدة من التيموزولوميد حتى أصبحت الخلايا مقاومة. في هذه الخلايا المتحملة، ارتفعت عدة إنزيمات DUB، لكن USP5 وUSP8 وUSP10 وبروتين الإصلاح MGMT كانت مرتفعة بشكل خاص. عندما استخدم الفريق جزيئات RNA صغيرة لإسكات USP5 أو USP8، أصبحت الخلايا المقاومة فجأة هشة: نشّطت برامج الانتحار الخلوية، بما في ذلك الاستماتة (apoptosis) وشكل من الهضم الذاتي الناتج عن الإجهاد يُعرف بالالتهام الذاتي (autophagy). في الوقت نفسه، انخفضت مستويات MGMT بشكل حاد، كما انخفض بروتين آخر مرتبط بالمقاومة، USP10، مما يشير إلى أن هذه الإنزيمات تحتل موقعًا علويًا في شبكة النجاة.
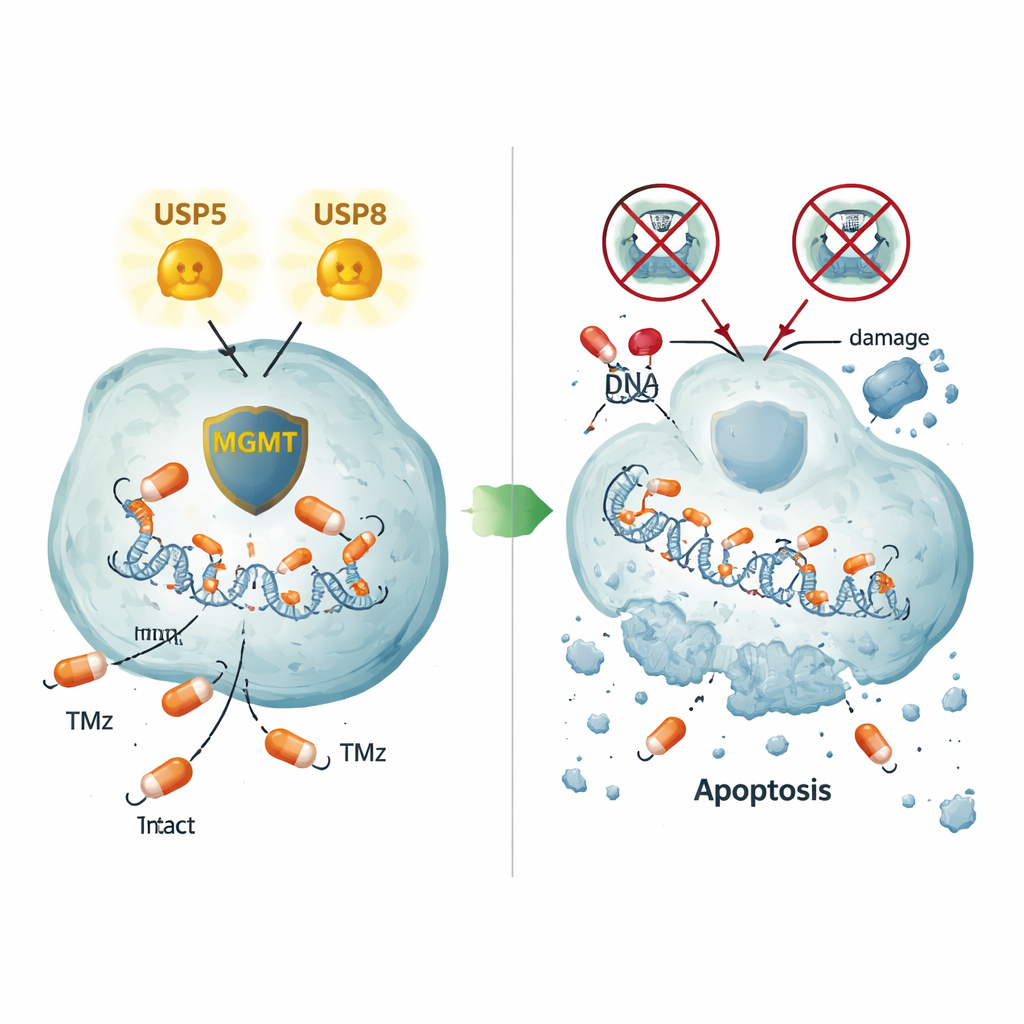
طريقتان مختلفتان للحفاظ على MGMT
أظهرت تصويرات دقيقة لخلايا الورم وأنسجة ورمية بشرية أن USP5 وMGMT غالبًا ما يتواجدان معًا في نفس مناطق الخلية، خاصة في السيتوبلازم. إن تعطيل USP5 لم يخفض MGMT فحسب، بل أدى أيضًا إلى تحلل MGMT بواسطة آلية تكسير البروتينات داخل الخلية، وهي عملية يمكن عكسها بدواء بورتزوميب الذي يعيق البروتيازوم. كما كان تكاثر إنتاج USP5 في خلايا سلبية لـMGMT كافيًا لرفع مستويات بروتين MGMT، حتى في خط خَلَوي غير دماغي، مما يؤكد تأثيرًا مثبتًا مباشرًا. تبين أن USP8 يعمل بطريقة مختلفة: إن إسكات USP8 خفض أيضًا MGMT لكن دون تغيير USP5 نفسه، كاشفًا عن مسار ثانٍ مستقل عن USP5 يساعد في إبقاء MGMT موجودًا. وحتى في خط خلوي مقاوم لم يكن يصنع MGMT على الإطلاق، أدى إيقاف USP5 أو USP8 إلى موت خلوي واسع النطاق، ما يشير إلى مسارات مقاومة إضافية يتحكم بها هذان الإنزيمان.
روابط بالجهاز المناعي وأفكار علاجية جديدة
بعيدًا عن مقاومة الدواء، تربط الدراسة USP5 بكيفية تفاعل الغلِيُوبلاستومة مع الجهاز المناعي. أشارت تحليلات بيانات جينومية إلى أن تغيّرات في مستويات USP5 ونسخ الجين تُغيّر توازن خلايا مناعية مختلفة حول الورم، بما في ذلك خلايا T القاتلة وخلايا T المنظمة. وقد أظهرت أعمال سابقة أيضًا أن USP5 يمكنه تثبيت PD‑L1، البروتين الذي تستخدمه الأورام لإيقاف خلايا T المهاجمة. مجتمعة، توحي النتائج بأن USP5 قد يساعد الأورام على النجاة من العلاج الكيميائي وتفادي الهجوم المناعي، مما يجعله هدفًا علاجيًا جذابًا بشكل خاص.
ماذا يعني ذلك لعلاجات سرطان الدماغ المستقبلية
بعبارة واضحة، تحدد هذه الدراسة USP5 وUSP8 كحماة رئيسيين يحميان بروتين الإصلاح MGMT ويساعدان خلايا الغلِيُوبلاستومة على مقاومة التيموزولوميد. من خلال تفكيك هؤلاء الحماة، استطاع المؤلفون قتل الخلايا المقاومة في المختبر وخفض مستويات MGMT، حتى في بعض الحالات التي لم تكن مقاومة MGMT هي المشكلة الوحيدة. يثير ذلك الأمل في أن أدوية مستقبلية تستهدف USP5 أو USP8، ربما بالاشتراك مع العلاج الكيميائي الحالي وأدوية قائمة على الجهاز المناعي، قد تعيد حساسية الأورام العنيدة وتمنح المرضى مزيدًا من الوقت.
الاستشهاد: Bhardwaj, S., Sanjay, Sharma, D. et al. MGMT upregulation mediates Temozolomide resistance conferred USP5 dependency. Sci Rep 16, 6118 (2026). https://doi.org/10.1038/s41598-026-36379-4
الكلمات المفتاحية: السِرطانُ الدِماغِيُّ الغلِيُوبلاستومي, مقاومة التيموزولوميد, MGMT, USP5, إنزيمات إزالة اليوبيكيتين