Clear Sky Science · ar
دور تعديلات الهستون التي يتوسطها MNX1 وعائلة جينات PBX في تحوير تكون اللوكيميا المستحث بواسطة MNX1
لماذا يهم خلل جيني طفيف الأطفال المرضى
معظم أنواع اللوكيميا الطفولية باتت الآن قابلة للعلاج، لكن شكلًا نادرًا يُسمى اللوكيميا الحادة لدى الرضع (AML) يبقى شديد الخطورة. كثير من هؤلاء الرضع يشتركون في نفس الحادثة الجينية: تبادل قطع بين كروموسوماتين يحول جين تطويري هادئًا يُدعى MNX1 إلى مُنبّه مفرط النشاط. تطرح هذه الدراسة سؤالًا بسيطًا لكنه حاسمًا: بعد أن يُنشَّط MNX1، ماذا يفعل فعليًا داخل خلايا الدم الصغيرة لدفعها نحو السرطان—وهل يمكن مقاطعة تلك العملية؟
من خلايا دم رضيع طبيعية إلى نمو خارق
تنشأ اللوكيميا عندما تتوقف خلايا الدم غير الناضجة عن النضوج وتبدأ بالتكاثر بشكل غير منضبط. في الرضع الحاملين تبادل الكروموسومات t(7;12)، يصبح MNX1 مفرط النشاط بشكل غير طبيعي في خلايا تكوين الدم المبكرة الموجودة في الكبد الجنيني ونخاع العظم. بنى الباحثون نموذجًا فأريًا يُحاكي هذا الوضع: شغّلوا MNX1 البشري في خلايا جذعية دموية جنينية، وزرعوه في فئران، ورصدوا تقدّم الحيوانات من حالة ما قبل اللوكيميا إلى اللوكيميا الكاملة. بمقارنة الخلايا في هذه المراحل المختلفة مع الضوابط الصحية، تمكّنوا من تتبّع كيف يعيد MNX1 توصيل أنظمة التحكم الداخلية للخلايا مع مرور الوقت.
كيف يعيد MNX1 كتابة كتاب تعليمات الخلية
MNX1 هو عامل نسخي، بروتين يرتبط بالحمض النووي ويضبط أي الجينات تُشغّل أو تُطفأ. جمع الفريق بين عدة أساليب قوية—مثل قياس الطيف الكتلي، وتسلسل الرنا، وتحليل الكروماتين—ليرى مع من يتعامل MNX1 وأي الجينات يغيّر. وجدوا أن MNX1 يتعاون مع إنزيمات تُضيف علامات كيميائية على بروتينات الهستون، الهياكل الملفوفة التي يُلفّ حولها الحمض النووي. على وجه الخصوص، يعزّز MNX1 علامة "تشغيل" تُدعى H3K4me3 ويقلل من علامة "إيقاف" تُدعى H3K27me3 في مواضع محددة في الجينوم. هذه التغييرات تُرخّي بنية الحمض النووي المحلية وتجعل من الأسهل أن تُشَغّل جينات رئيسية متعلقة بالنمو.
دفعة سريعة وراحلة على جين تحكم حاسم
من بين العديد من الجينات المتأثرة، برز واحد: Pbx1، جزء من عائلة PBX لبروتينات رابطة الحمض النووي المرتبطة منذ زمن باللوكيميا. تُظهر الدراسة أن MNX1 يرتبط مباشرة بمنطقة التحكم في جين Pbx1، مزيلاً علامة الإيقاف ومزيدًا من علامة التشغيل هناك. هذا يطلق تعبير Pbx1 في مرحلة مبكرة جدًا، عندما تكون الخلايا لا تزال في حالة ما قبل اللوكيميا. بشكل مفاجئ، لاحقًا—بعد تكامل اللوكيميا—لم يعد MNX1 مرتبطًا بقوة في ذلك الموقع، ومع ذلك يبقى جين Pbx1 مشتغلًا وتستمر علامات الهستون في تكوين يدعم النمو. وهذا يوحي بآلية "ضربة وابتعاد": يزورها MNX1 بشكل عابر مناطق رئيسية من الكروماتين، يترك وراءه علامات ولاجينية دائمة، ثم يرحل بينما يستمر الوضع المعدّل في تغذية المرض.
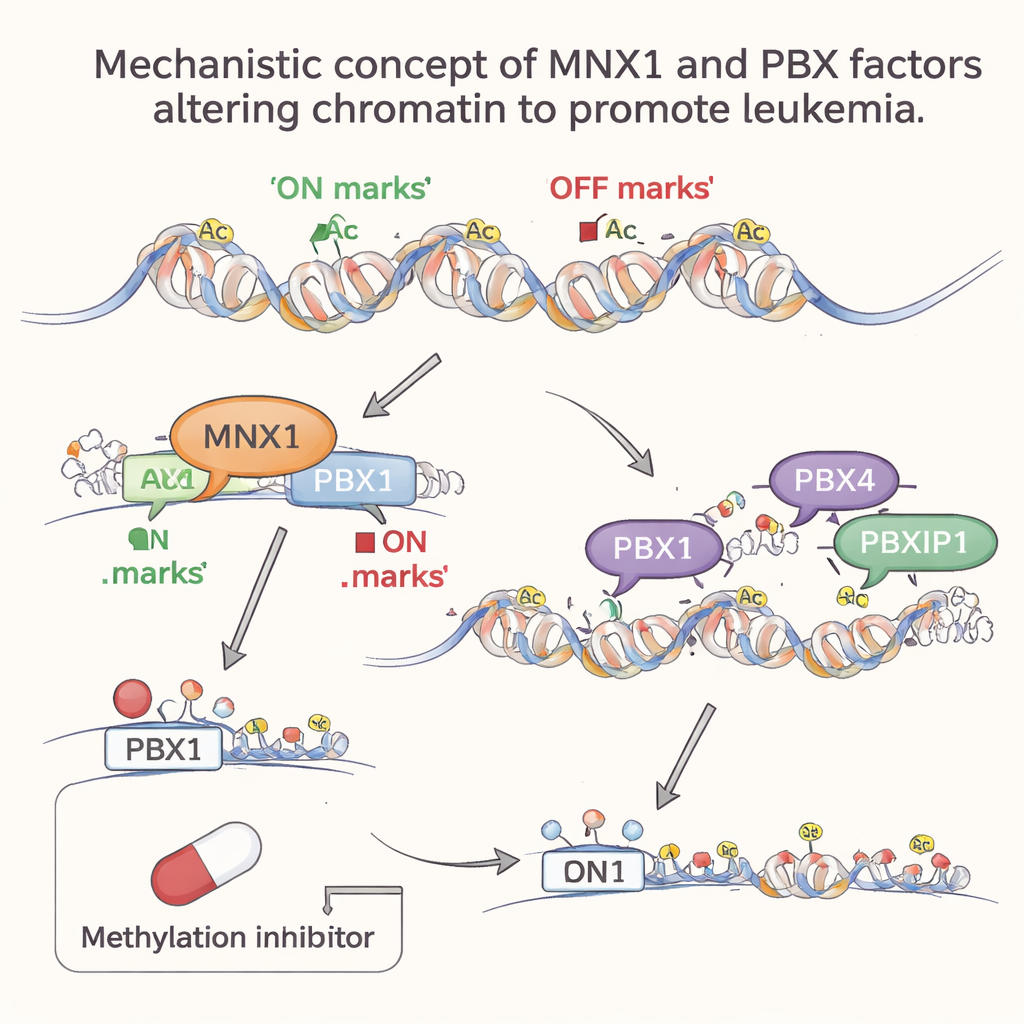
مساعدون لاحقون ينضمون لتثبيت حالة السرطان
مع تقدّم اللوكيميا، تصبح أعضاء أخرى من عائلة PBX، مثل PBX4 وPBXIP1، أكثر نشاطًا، ولكن فقط في مرحلة لاحقة. أظهرت التحليلات على مدى الجينوم أن الزخارف النمطية المفضلة لديهم مُثرية بكثافة في مناطق الكروماتين المفتوح والنشط التي أعيد تشكيلها عقب نشاط MNX1. بعبارة أخرى، يعيد MNX1 في البداية تشكيل مشهد الكروماتين ويشغّل Pbx1؛ ثم تنتقل PBX4 وPBXIP1 إلى هذه المناطق الجديدة المتاحة لتعزيز برامج جينية شاذة تُروّج لانقسام الخلايا، وتعيق تطوّر الدم الطبيعي، وتضعف إصلاح الحمض النووي. هذه المشاركة المرحلية توحي بتقسيم للعمل: يعمل PBX1 كمفتاح مبكّر معتمد على MNX1، بينما تساعد PBX4 وPBXIP1 في الحفاظ على برنامج اللوكيميا.
حجب العلامات الكيميائية التي تغذي اللوكيميا
بما أن MNX1 يعمل عبر إنزيمات تضيف مجموعات ميثيل إلى الهستونات، اختبر الفريق ما إذا كان مُثبّط واسع للميثيلترانسفيرازات، سينيفنغين (Sinefungin)، يمكنه تعطيل سلسلة الأحداث هذه. في خلايا دموية جنينية في حالة ما قبل اللوكيميا تعبر MNX1، قلّل سينيفنغين بشكل حاد مستويات Pbx1، متوافقًا مع حجب الميثلة الخاصة بالمروج التي يعتمد عليها MNX1. بالمقابل، تكاد مستويات PBX4 وPBXIP1 لا تتغير، ما يتناسب مع تنشيطها اللاحق وغير المباشر أثناء تقدم المرض. مجتمعة، تُقدّم هذه النتائج دليلًا قويًا أن اللوكيميا الطفيلية لدى الرضع التي تحمل t(7;12) تُدفع ليس فقط بواسطة جين مصاب، بل بسلسلة من التغييرات اللاجينية الدائمة التي يُطلقها MNX1.
ماذا يعني هذا للعلاجات المستقبلية
بالنسبة لغير المختصين، الخلاصة أن هذه الدراسة ترسم تتابعًا تفاعليًا: جين MNX1 المفرط النشاط يعيد توصيل العلامات الكيميائية على بروتينات تغليف الحمض النووي، يشغّل PBX1 مبكرًا، ويمهّد الطريق أمام PBX4 وPBXIP1 للمساعدة في تثبيت الخلايا في حالة لوكيمية. وبما أن هذه الخطوات تعتمد على أنماط ميثلة هستون محددة، فإنها توفر أهدافًا واضحة وقابلة للاختبار للأدوية التي تتداخل مع تلك العلامات. على المدى الطويل، قد تساعد العلاجات الموجهة لمحور MNX1–PBX أو للإنزيمات التي تضع هذه الوسومات اللاجينية في إيقاف التعليمات الخاطئة التي تُحرّك هذه اللوكيميا العدوانية لدى الرضع، مما يحسّن فرص تحقيق شِفَاء دائم.
الاستشهاد: Malmhäll-Bah, E., Östlund, A., Nilsson, T. et al. Role of MNX1-mediated histone modifications and PBX gene family in MNX1-induced leukemogenesis. Sci Rep 16, 2593 (2026). https://doi.org/10.1038/s41598-026-36367-8
الكلمات المفتاحية: اللوكيميا الحادة لدى الرضع, MNX1, PBX1 PBX4 PBXIP1, الميثلة اللاجينية للهستون, الانتقال الكروموسومي t(7;12)