Clear Sky Science · ar
تثبيط CDC25C يثبط نمو سرطان الكبد عبر الإجهاد الميتوكوندري المحفِّز للالتهام الذاتي والموت المبرمج
لماذا تهم هذه الدراسة عن سرطان الكبد
يعد سرطان الكبد واحداً من أخطر السرطانات على مستوى العالم، ويُشخَّص العديد من المرضى في مراحل متأخرة تجعل الجراحة أو العلاجات القياسية أقل فاعلية. تستقصي هذه الدراسة مفتاحاً خلوياً واحداً — بروتين يُدعى CDC25C — يبدو أنه يحفز نمو سرطان الكبد بينما يكون أقل أهمية للخلايا الكبدية السليمة. عبر خفض نشاط هذا المفتاح، وجد الباحثون أنهم يستطيعون إحداث إجهاد وقتل الخلايا السرطانية في نهاية المطاف عبر آليات التنظيف الذاتي والانتحار الخلوي الخاصة بالخلايا، مما يشير إلى استراتيجية علاجية واعدة وأكثر انتقائية.
مفتاح النمو داخل أورام الكبد
كل خلية يجب أن تقرر متى تنقسم ومتى تتوقف. يعد CDC25C واحداً من البروتينات الأساسية التي تدفع الخلايا طوال دورة الانقسام. في سرطان الكبد، يكون هذا المفتاح غالباً عالقاً في وضع "تشغيل"، مما يساعد الأورام على النمو والانتشار. استخدم الفريق خلايا سرطان كبد الفأر وخلايا كبد فأرية طبيعية، بالإضافة إلى فئران حاملة للأورام، لتقليل مستويات CDC25C اصطناعياً. وأكدوا، باستخدام اختبارات جينية وبروتينية معيارية، أن CDC25C انخفض بشكل حاد في المجموعة التجريبية مقارنةً بالمعايير، فأنشأوا نموذجاً قوياً لدراسة ما يحدث عندما يُخفَض هذا المفتاح النموّي.
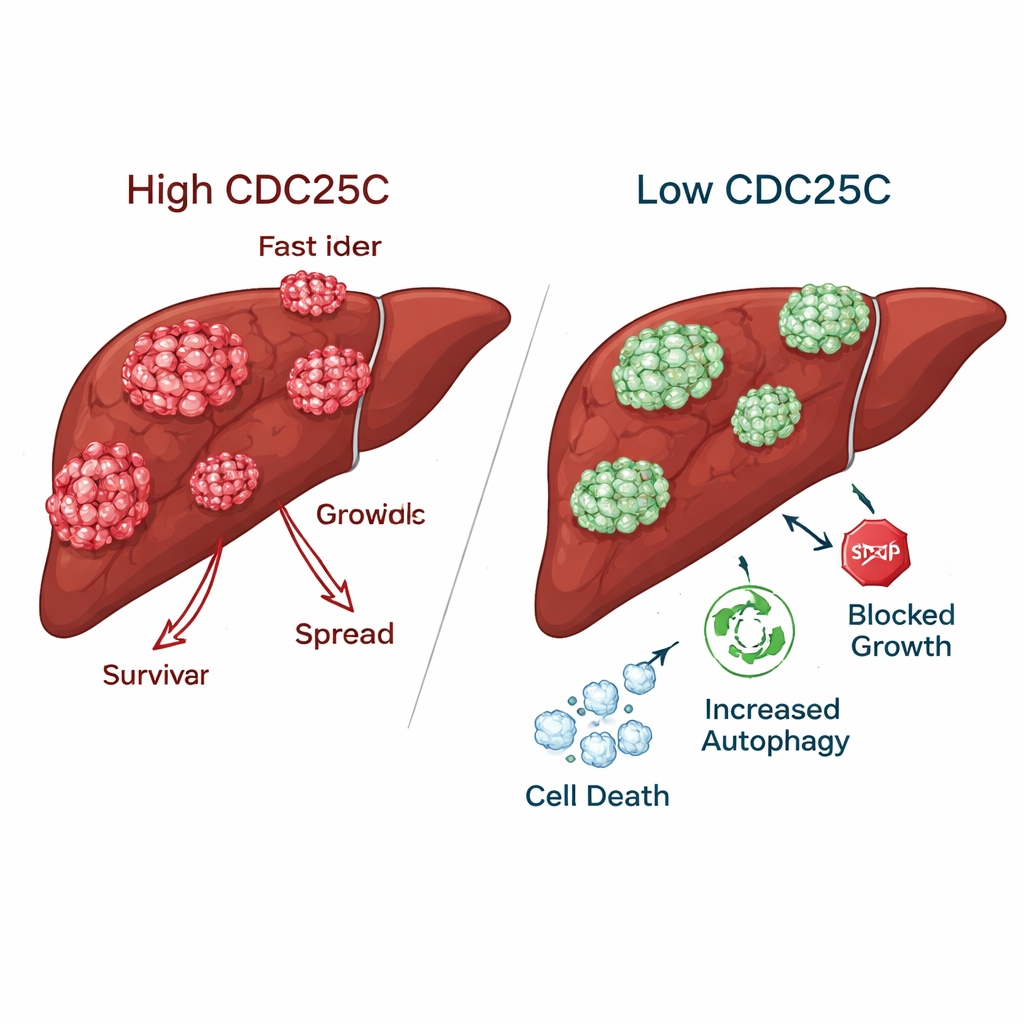
إبطاء السرطان مع الحفاظ على خلايا الكبد السليمة
عندما خُفِّض CDC25C في خلايا سرطان الكبد، فقدت الأورام العديد من صفاتها العدوانية. شكلت خلايا السرطان مستعمرات أقل بكثير، وتحركت ببطء أكبر عبر "جروح" صناعية، وكانت أقل قدرة على النفاذ عبر الحواجز في اختبارات المختبر. على النقيض من ذلك، أظهرت خلايا الكبد الطبيعية نمواً وحركة محسّنين فعلاً عند انخفاض CDC25C، ما يوحي أن النسيج السليم قد يتحمل أو يستفيد من تثبيط CDC25C. في الفئران، أظهرت الأورام المهندسة لتقليل CDC25C مستويات أدنى من هذا البروتين على مستوى الجين والبروتين، مؤكدة أن نفس التأثير حدث في حيوانات حية.
إجهاد محطات الطاقة و"فرِيق" التنظيف الخلوي
عند فحص داخل الخلايا بمجاهر إلكترونية، رصد الباحثون أن خلايا السرطان ذات CDC25C المنخفض احتوت ميتوكوندريات متورمة ومتضررة — محطات الطاقة الصغيرة في الخلية — إلى جانب هياكل شبيهة بالفقاعات تسمى الحويصلات الالتهامية التي تشير إلى تنشيط نظام إعادة التدوير الداخلي للخلية، أي الالتهام الذاتي. ثم قاسوا علامات رئيسية للإجهاد الميتوكوندري: مستويات الكالسيوم وأنواع الأكسجين التفاعلية (ROS)، وكلاهما ارتفع في خلايا السرطان بعد خفض CDC25C. كما زادت مؤشرات استجابة الإجهاد الميتوكوندري، بما في ذلك بروتينات مساعدة مثل HSP60 وإنزيمان من نوع "مراقبة الجودة" الميتوكوندرية، وكذلك CHOP، وهو عامل مرتبط بالإجهاد يربط مشكلات الميتوكوندريا باستجابات خلوية أوسع. اللافت أن إشارات الإجهاد هذه حركت في الاتجاه المعاكس في خلايا الكبد الطبيعية، مما يعزز الفكرة أن الخلايا السرطانية والسليمة تستجيبان بشكل مختلف جداً لفقدان CDC25C.
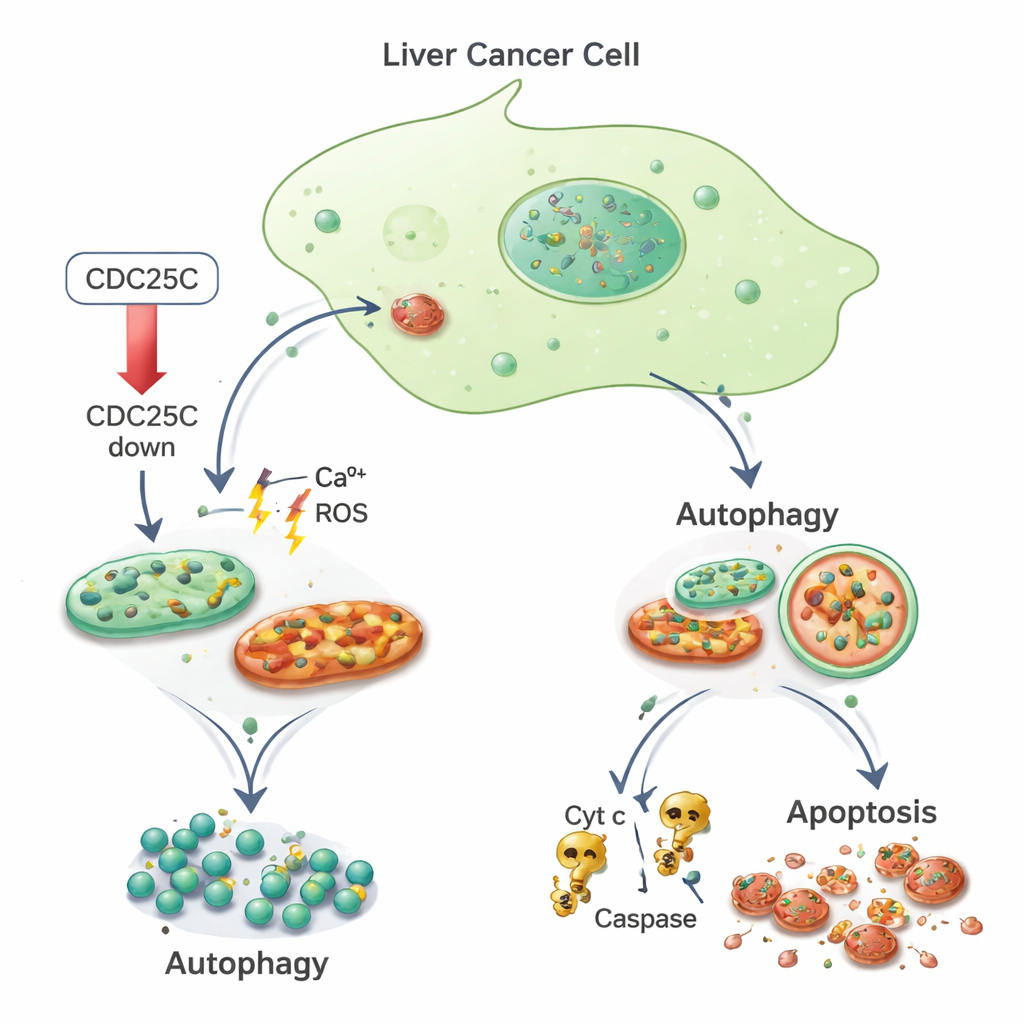
من الإجهاد إلى الهضم الذاتي والموت الخلوي
سأل الفريق بعد ذلك كيف تتعامل هذه الخلايا السرطانية المُجهدة مع الوضع. وجدوا أن مؤشرات الالتهام الذاتي ارتفعت في كل من خلايا السرطان وخلايا الكبد الطبيعية عند خفض CDC25C. ارتفعت مستويات بروتينات مثل LC3 وp62، التي تعكس تشكل ونشاط الحويصلات الالتهامية، مما يدل على أن الخلايا تكثف آليات التنظيف لديها. في الوقت نفسه، في خلايا السرطان فقط، يبدو أن الضرر الميتوكوندري يدفع الخلايا إلى ما بعد نقطة الإصلاح نحو الموت المبرمج. باستخدام صبغات فلورية والقياس الخلوي بالتدفق، رأى الباحثون مزيداً من خلايا السرطان ذات نوى متفتتة وذات تلون ساطع — سمة مميزة للاعتلال المبرمج — وانخفاضاً في جهد غشاء الميتوكوندريا. كما وجدوا ارتفاعاً في مستويات السيتوكروم c والإنزيمين Caspase-3 وCaspase-9، وهي مكونات كلاسيكية لمسار الموت المدفوع بالميتوكوندريا. بالمقابل، أظهرت خلايا الكبد الطبيعية مقداراً أقل من الموت المبرمج تحت نفس ظروف خفض CDC25C.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
للقارئ غير المتخصص، الرسالة الأساسية هي أن خفض CDC25C يبدو أنه يصيب خلايا سرطان الكبد في نقاط ضعفها: يفرط في تحميل محطات طاقتها، يدفع أنظمة إعادة التدوير إلى العمل المفرط، وفي النهاية يحفز الانتحار الخلوي المنظم — بينما يعفي إلى حد كبير خلايا الكبد السليمة. يستنتج المؤلفون أن CDC25C أكثر من مجرد مفتاح نمو بسيط؛ فهو يشكل أيضاً طريقة تعامل الخلايا مع الإجهاد والتنظيف والموت. وبما أن الخلايا السرطانية تعتمد بدرجة كبيرة على CDC25C وتستجيب لفقدانه بإجهاد ميتوكوندري قاتل وموت مبرمج، فقد توفر الأدوية التي تستهدف هذا البروتين أو مسارات الإجهاد المتبعة به يوماً ما وسيلة أكثر انتقائية لعلاج سرطان الكبد مع أضرار أقل للنسيج الكبدي السليم.
الاستشهاد: Miao, X., Zheng, F., Mo, X. et al. CDC25C downregulation suppresses HCC growth via mitochondrial stress-induced autophagy and apoptosis. Sci Rep 16, 5631 (2026). https://doi.org/10.1038/s41598-026-36351-2
الكلمات المفتاحية: سرطان الكبدة الخلوي, CDC25C, الإجهاد الميتوكوندري, الالتهام الذاتي, الموت المبرمج