Clear Sky Science · ar
التعلّم الآلي الذي يدمج بين التصوير بالرنين المغناطيسي والميزات السريرية يتنبأ بالانتكاس المبكر لسرطان الكبد بعد الاستئصال
لماذا يهم عودة السرطان المبكرة
بالنسبة للأشخاص الذين يخضعون لعملية جراحية لإزالة سرطان الكبد، تبقى واحدة من أكبر المخاوف هي ما إذا كانت الإصابة ستعود بسرعة. يشير الارتداد المبكر لسرطان الكبد البطاني الحرشفي—أكثر أنواع سرطان الكبد الأولية شيوعًا—غالبًا إلى ورم عدواني ومعدل بقاء أقل. يرغب الأطباء في معرفة، حتى قبل الجراحة، أي المرضى هم الأكثر عرضة لانتكاس مبكر حتى يتمكنوا من تخصيص فحوصات متابعة وعلاجات إضافية. تستكشف هذه الدراسة ما إذا كان الذكاء الاصطناعي قادرًا على دمج تحاليل الدم الروتينية، ونتائج فحوصات الرنين المغناطيسي، ونتائج النسج لتوفير إشارة إنذار مبكر.
جمع الدلالات المتعددة معًا
حلّل الباحثون بيانات 240 مريضًا بسرطان الكبد خضعوا لعملية جراحية في مستشفيين بالصين. قبل العمليات، أجرى جميع المرضى فحوصات رنين مغناطيسي معيارية مع مادة تباين واختبارات دم شائعة، وبعد الجراحة فُحصت أورامهم تحت المجهر. بدلًا من النظر إلى عامل واحد في كل مرة—مثل حجم الورم أو علامة دموية مفردة—أدخل الفريق عشرات من هذه القياسات إلى خوارزميات التعلّم الآلي. صُممت هذه الأساليب لاكتشاف أنماط وتفاعلات معقدة قد تفلت من الأدوات الإحصائية التقليدية، خصوصًا عندما لا تكون العلاقات ببساطة «الأكبر أسوأ» أو «الأعلى أفضل».
كيفية بناء نماذج الذكاء الاصطناعي
لتجنب تحميل النظام زائد ما يحتمل، قلّص المحققون أولًا قائمة الميزات المرشحة الطويلة. أزالوا القياسات التي كانت شبه مكررة لبعضها البعض ثم استخدموا تقنية إحصائية تسمى LASSO لاختيار 14 من أكثر العوامل معلوماتية. باستخدام هذه الميزات، درّبوا عدة نماذج تعلّم آلي تعتمد على الأشجار—ExtraTrees و XGBoost و LightGBM و GradientBoosting—لتوقّع ما إذا كان المريض سيشهد عودة السرطان خلال عامين من الجراحة. تمت معايرة النماذج على بيانات من مستشفى واحد ثم اختُبرت على مجموعة مستقلة من المرضى من المستشفى الثاني، وهو اختبار أصعب يعكس أفضل استخدام عملي في العالم الحقيقي.
مدى أداء النماذج
أظهرت ثلاثة من نماذج الذكاء الاصطناعي—ExtraTrees و XGBoost و LightGBM—قدرة قوية على التمييز بين المرضى الذين حدث لديهم انتكاس مبكر والذين لم يحدث لديهم. في مجموعة التدريب، تراوحت درجات أدائها (المقاسة بمساحة تحت منحنى ROC، أو AUC) من حوالي 0.82 إلى 0.98، حيث 1.0 تعني مثالية و0.5 لا تختلف عن الصدفة. في مجموعة الاختبار الخارجية، كانت قيم AUC أقل قليلًا، نحو 0.76 إلى 0.79، لكنها لا تزال تدل على قدرة تنبؤية مفيدة. أشارت تحليلات منحنى القرار، وهي طريقة تُقدّر ما إذا كان النموذج سيساعد الأطباء فعليًا على اتخاذ قرارات أفضل، إلى أن استخدام هذه الأدوات قد يوفر فائدة أكبر من معاملة جميع المرضى على نحو موحّد أو الاعتماد على الصدفة. عمومًا، بدت النماذج دقيقة إلى حد معقول وذات معنى سريري.
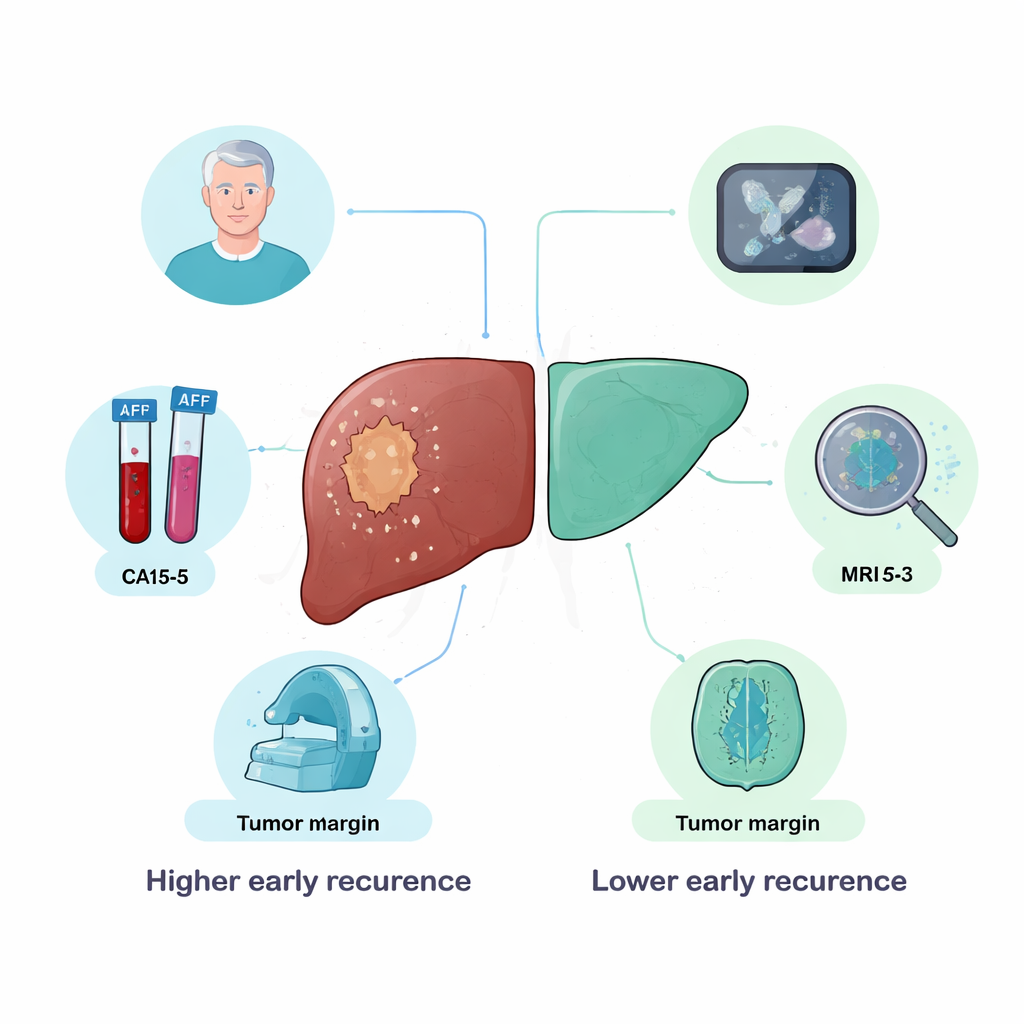
ما الذي قاد التنبؤات
من خلال فحص المدخلات التي اعتمدت عليها النماذج أكثر من غيرها، تقدم الدراسة رؤى حول ما يبدو مهمًا للانتكاس المبكر. اثنان من العلامات الدموية—AFP، المستخدمة منذ زمن في رعاية سرطان الكبد، وCA15‑3، الأكثر شهرة في سرطان الثدي—تصدرتا باستمرار قائمة الميزات ذات التأثير الأكبر. ارتبطت إشارات الرنين المغناطيسي لهامش ورم غير منتظم وغير أملس ارتباطًا قويًا بالانتكاس المبكر، ما يعكس أعمالًا سابقة ربطت بين الخطوط المتعرجة للورم وسلوك أكثر تغلغلاً وانتشارًا خفيًا داخل الكبد. لعب العمر دورًا أيضًا، إذ بدا أن المرضى الأصغر سنًا أكثر عرضة للانتكاس المبكر بصورة مفاجئة، ربما مما يعكس بيولوجيا أورام أكثر عدوانية في هذه الفئة. دعمت السمات المجهرية مثل مجموعات صغيرة من خلايا السرطان داخل أوعية دموية دقيقة تقديرات المخاطر التي قدمها الذكاء الاصطناعي.
ماذا يعني هذا للمرضى والأطباء
بالنسبة لشخص يواجه جراحة سرطان الكبد، لا تحل النماذج الموضحة في هذه الدراسة محل حكم الطبيب، لكنها قد تقدّم طبقة إضافية من الإرشاد. من خلال دمج معلومات تُجمع بالفعل في الرعاية الروتينية—تحاليل الدم، ونتائج الرنين المغناطيسي، وعلامات النسج القياسية—يمكن لأدوات الذكاء الاصطناعي تمييز المرضى ذوي المخاطر الأعلى للارتداد المبكر. قد يستفيد هؤلاء الأشخاص من متابعة تصويرية أكثر تكرارًا، أو فحوص دم متكررة، أو النظر في علاجات إضافية بعد الجراحة. لأن الدراسة كانت استعادية ومحدودة بمركزين في منطقة واحدة، يؤكد المؤلفون على حاجة تجارب أكبر مستقبلية قبل أن تصبح مثل هذه النماذج معيارًا. ومع ذلك، تشير هذه العمل إلى مستقبل قد يساعد فيه الذكاء الاصطناعي الأطباء على تخصيص المراقبة والعلاج بهدف اكتشاف عودة سرطان الكبد في وقت أبكر وتحسين النتائج طويلة الأمد.
الاستشهاد: Feng, L., Luo, N., Ruan, F. et al. Machine learning integrating MRI and clinical features predicts early recurrence of hepatocellular carcinoma after resection. Sci Rep 16, 5653 (2026). https://doi.org/10.1038/s41598-026-36261-3
الكلمات المفتاحية: سرطان الكبد, التعلّم الآلي, التصوير بالرنين المغناطيسي, تكرار الورم, مؤشرات حيوية في الدم