Clear Sky Science · ar
إعادة توظيف داباجليفلوزين عبر نانوجيلات بوليمرية لعلاج سرطان القولون والمستقيم
لماذا قد يساعد دواء للسكري في مكافحة سرطان القولون
يُعد سرطان القولون والمستقيم أحد الأسباب الرئيسية للوفيات المرتبطة بالسرطان على مستوى العالم، وما زال العديد من المرضى يعانون من انتكاسات رغم الجراحة والعلاج الكيميائي. تستكشف هذه الدراسة حليفًا غير متوقع ضد هذا المرض: داباجليفلوزين، حبة شائعة لعلاج داء السكري من النوع الثاني. من خلال تعبئة هذا الدواء في جزيئات ناعمة صغيرة تتحول إلى هلام لطيف في المعدة، يهدف الباحثون إلى توصيل كمية أكبر منه إلى الأمعاء الغليظة — حيث تنشأ أورام القولون — مع إبقاء الجرعة التي تؤخذ عن طريق الفم مشابهة للأقراص الحالية.
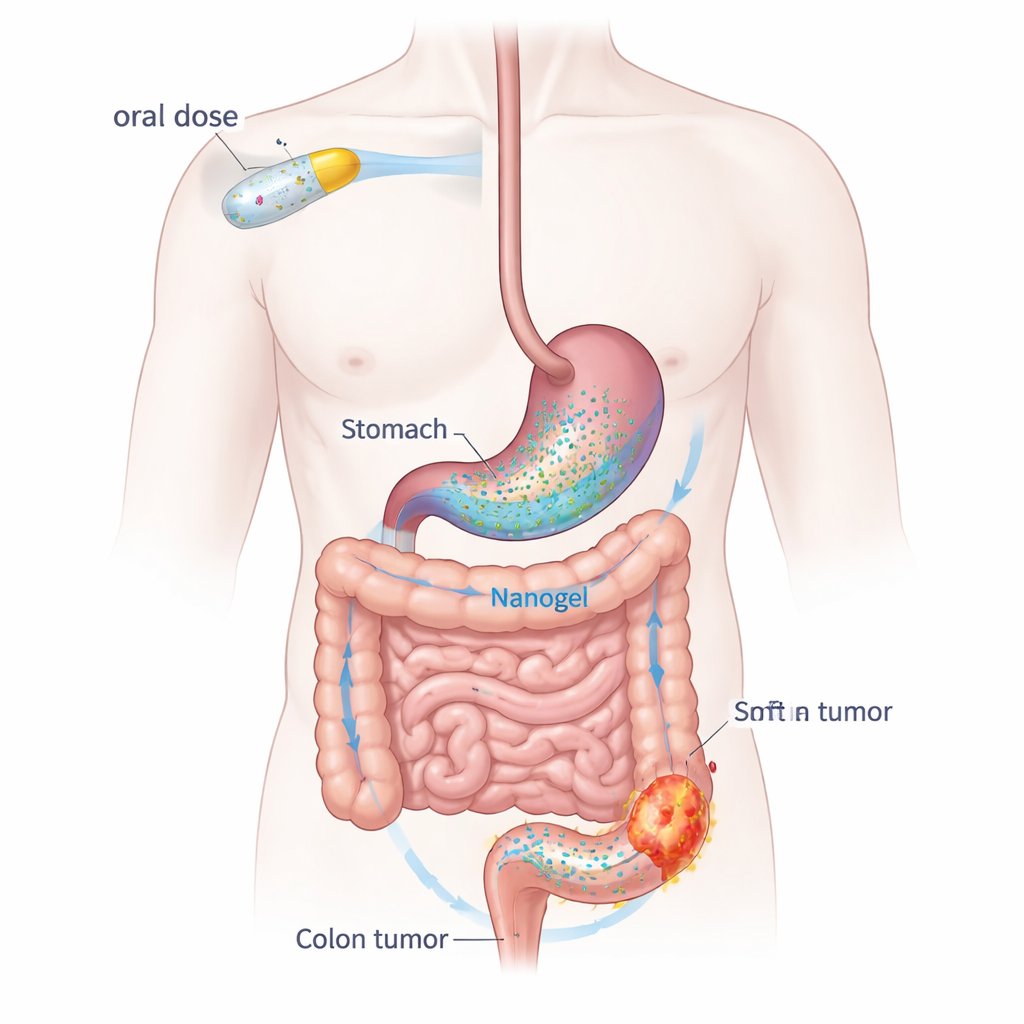
تحويل حبة يومية إلى حمولة مستهدفة للسرطان
يعمل داباجليفلوزين عادة في الكلى لخفض مستوى السكر في الدم، لكنه أيضًا يهدئ الالتهاب ويبطئ نمو الخلايا — وهما عمليتان تعتمد عليهما السرطانات. ومع ذلك، يذوب الدواء بمفرده بشكل ضعيف في الماء ويُزال من الجسم بسرعة إلى حد ما. للتغلب على ذلك، بنى الفريق نظام توصيل "نانوجيل" باستخدام بوليمرات شبيهة بالطعام: ألجinate الصوديوم المستخرج من الطحالب البحرية، وبوليفينيل الكحول، وهو مادة مثخنة متوافقة حيويًا ومستخدمة على نطاق واسع. يُحبس الدواء داخل جسيمات نانوية يبلغ قطرها نحو عُشر ألف من المليمتر. عندما تواجه هذه الجسيمات حمض المعدة، تستقر وتتشابك لتشكل كتلة هيدروجيل ناعمة تبقى لفترة، ثم تطلق الدواء تدريجيًا أثناء تنقله نحو القولون.
جعل الدواء أكثر ذوبانًا وأبطأ في الغياب
بدأ العلماء أولًا بتحسين طريقة تصنيع الجسيمات، وضبطوا نسبة البوليمرين حتى تظل الجسيمات النانوية صغيرة ومتناسقة الحجم ومستقرة في المحلول. أكدوا أن الدواء مدمج جيدًا داخل شبكة البوليمر وتحول جزئيًا من شكل بلوري إلى شكل أمورفي أكثر، والذي يذوب عمومًا بشكل أفضل. في سوائل اختبارية تحاكي سوائل المعدة والأمعاء، زادت صيغة النانوجيل من الذوبان الظاهر للداباجليفلوزين بنحو 1.7–1.8 مرة مقارنة بالدواء الخام. عندما راقبوا سرعة تسرب الدواء، أظهر النانوجيل منحنى تحرير لطيف "بطيء الإفراج" على مدى عدة ساعات، بدلًا من الطفرة السريعة المرصودة مع الدواء الخالص. شكلت وصفة معينة، أطلقوا عليها اسم F2، هيدروجيلًا مضغوطًا ومتينًا حافظ على تماسكه لمدة ساعتين على الأقل في ظروف حمضية بينما أطلق الدواء بثبات.
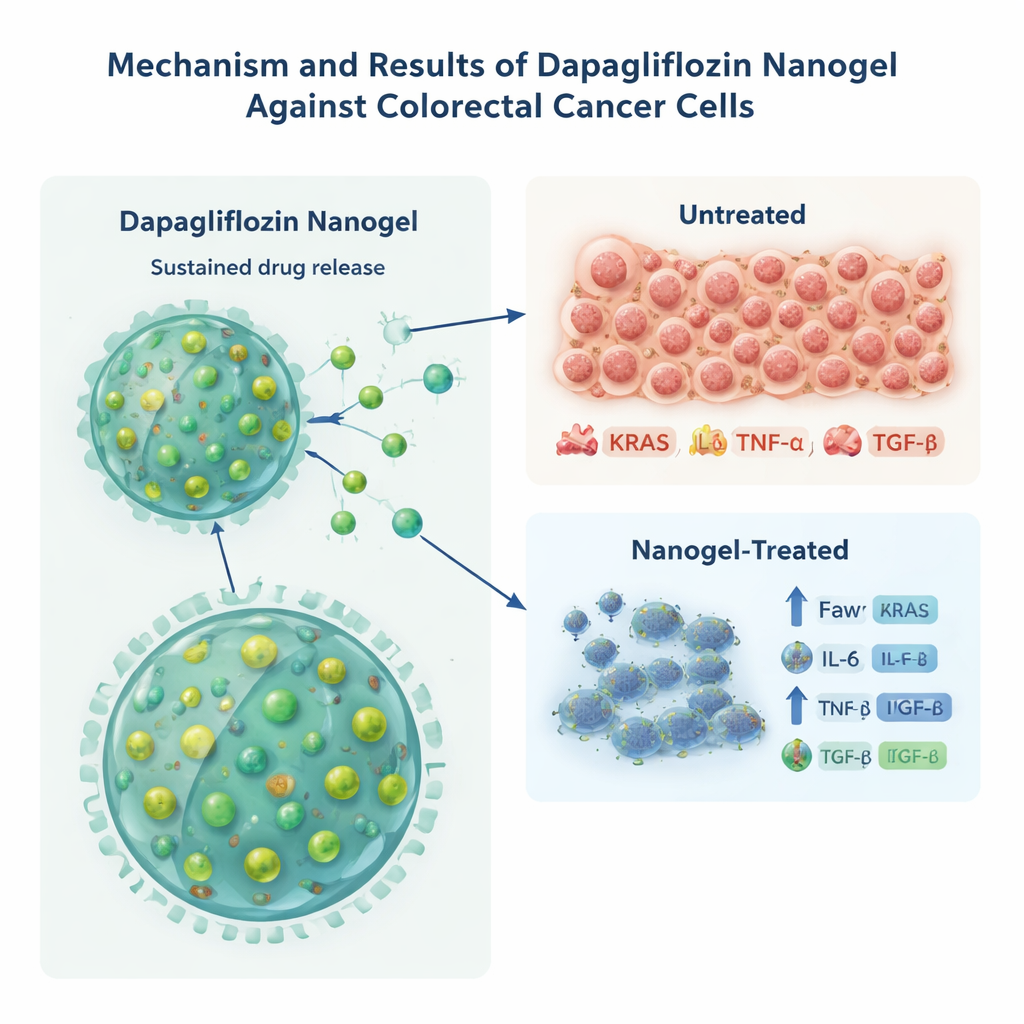
إجهاد خلايا السرطان في المختبر
لاختبار ما إذا كان هذا الشكل الجديد من داباجليفلوزين قادرًا فعليًا على إيذاء خلايا السرطان، اختبر الفريق تركيزه على خلايا سرطان القولون والمستقيم HCT-116 المزروعة في أطباق مخبرية. بالمقارنة مع نفس كمية الدواء الحر، قتل شكل النانوجيل الخلايا بسرعات أقل من حيث التركيز، حيث خفّض الجرعة المطلوبة لإعاقة نمو الخلايا إلى النصف بنحو ثُلث. ثم نظر الباحثون إلى جزيئات مرتبطة بالسلوك الورمي العدواني والالتهاب المزمن، بما في ذلك KRAS (بروتين رئيسي يدفع السرطان) والبروتينات الإشارية IL-6 وTNF-α وTGF-β. أظهرت الخلايا المعالجة بالنانوجيل المحمّل بالدواء مستويات أقل بكثير من كل هذه المؤشرات مقارنة بالخلايا المعالجة بالدواء الحر أو بالجسيمات الفارغة، مما يشير إلى أن التعرض المستمر من الجسيمات النانوية خفّض إشارات تتعلق بالسرطان والالتهاب بشكل أكثر فعالية. وبما أن خط الخلايا يحمل بالفعل طفرة ثابتة في KRAS، يحذر المؤلفون من أن هذا الانخفاض في بروتين KRAS قد يعكس استجابات إجهادية بدلاً من تصحيح جيني مباشر، لكنه لا يزال يدعم تأثيرًا بيولوجيًا قويًا.
تغيير كيفية تعامل الجسم مع الدواء
انتقل الفريق بعدها إلى دراسات حيوانية، حيث أعطوا الفئران إما معلقًا بسيطًا من مسحوق داباجليفلوزين أو النانوجيل المحسن، كلاهما عن طريق الفم وبنفس الجرعة. في مجموعة النانوجيل، ظهرت مستويات الذروة للدواء في الدم متأخرة وكانت أدنى، لكن بقي الدواء في الدورة الدموية لفترة أطول. ارتفعت التعرض الكلي (المقاس بمساحة تحت المنحنى) باعتدال بنحو 7%، وتضاعف تقريبًا العمر النصفي الظاهر. تعني هذه التغيرات أن الجسم يرى جرعة أكثر سلاسة وممتدة عبر الزمن بدلًا من قفزة حادة ثم انخفاض سريع. يتطابق هذا السلوك مع ما صممه الباحثون للجيل: احتجاز الدواء في الأمعاء، إطلاقه ببطء، واحتمال بقاء مستويات أعلى منه تغمر الجزء السفلي من الأمعاء والقولون حيث تنشأ الأورام.
ما الذي قد يعنيه هذا لرعاية السرطان في المستقبل
ببساطة، تأخذ هذه الدراسة دواءً معروفًا للسكري وتجهزه بـ"بدلة توصيل" جديدة حتى يتمكن من الوصول بشكل أفضل والبقاء بالقرب من أورام القولون. يجعل النانوجيل الدواء أسهل في الذوبان، يبطئ هروبه من الأمعاء، ويبدو أنه يجعله أكثر سمية لخلايا سرطان القولون والمستقيم مع خفض إشارات الالتهاب والنمو الرئيسية. في الفئران، يطيل بهدوء تواجد الدواء في مجرى الدم دون زيادة كبيرة في الجرعة الكلية. العمل لا يزال في مرحلة مبكرة — محدود بخط خلية سرطانية واحد واختبارات حيوانية قصيرة الأمد — ولم يُظهر بعد انكماشًا مباشرًا للأورام في حيوانات أو بشر أحياء. ومع ذلك، يضع ذلك أساسًا مفصلاً لإعادة توظيف داباجليفلوزين كجزء من علاجات مستقبلية لسرطان القولون والمستقيم، باستخدام نانوجيلات فموية ذكية لتحويل حبة مألوفة إلى أداة مضادة للسرطان أكثر استهدافًا.
الاستشهاد: Abdullah, S., Thiab, S., Altamimi, A.A. et al. A repurposing Dapagliflozin via polymeric nanogels for colorectal cancer therapy. Sci Rep 16, 5625 (2026). https://doi.org/10.1038/s41598-026-36232-8
الكلمات المفتاحية: سرطان القولون والمستقيم, إعادة توظيف الأدوية, جسيمات نانوية, إيصال الدواء عن طريق الفم, داباجليفلوزين