Clear Sky Science · ar
المراقبة الجينومية على مستوى البلاد لعزلات Klebsiella pneumoniae المقاومة للكاربينيم والقولستين من مجرى الدم في تايلاند (2020–2024)
ارتفاع عدوى الدم المميتة
تواجه المستشفيات في أنحاء العالم اتجاهًا مقلقًا: بكتيريا شائعة كانت تخضع لأقوى مضاداتنا الحيوية باتت تكاد تكون غير قابلة للعلاج. تركز هذه الدراسة على Klebsiella pneumoniae، الميكروب القادر على غزو مجرى الدم والتسبب في عدوى مهددة للحياة، وتتبع كيف تطور عبر تايلاند ليقاوم حتى الأدوية الملجأ الأخيرة. فهم أماكن انتشار هذه البكتيريا الخارقة وكيفية تهربها من الأدوية أمر بالغ الأهمية لحماية المرضى، وتوجيه اختيارات الأطباء، وصياغة سياسات الصحة العامة.
تتبع بكتيريا المستشفيات عبر أمة
حلل الباحثون 227 عينة من Klebsiella pneumoniae مأخوذة من دم مرضى في مستشفيات تايلاند بين عامي 2020 و2024. جاءت هذه العينات من شبكة مراقبة وطنية تجمع بيانات بانتظام عن العدوى المقاومة للأدوية. أظهرت الاختبارات المخبرية أن أكثر من 93% من هذه العزلات من مجرى الدم كانت مقاومة للكاربينيمات، فئة قوية من المضادات تُستخدم غالبًا عندما تفشل أدوية أخرى. والمقلق أن ما يقرب من ثلث السلالات المقاومة للكاربينيم كانت أيضًا مقاومة للقولستين، أحد الخيارات الأخيرة لدى الأطباء عند نفاد البدائل. بربط اختبارات الحساسية التقليدية بتسلسل الجينوم الكامل، استطاع الفريق رؤية ليس فقط الأدوية التي فشلت، بل أيضًا الحيل الجينية التي استخدمتها البكتيريا للبقاء.
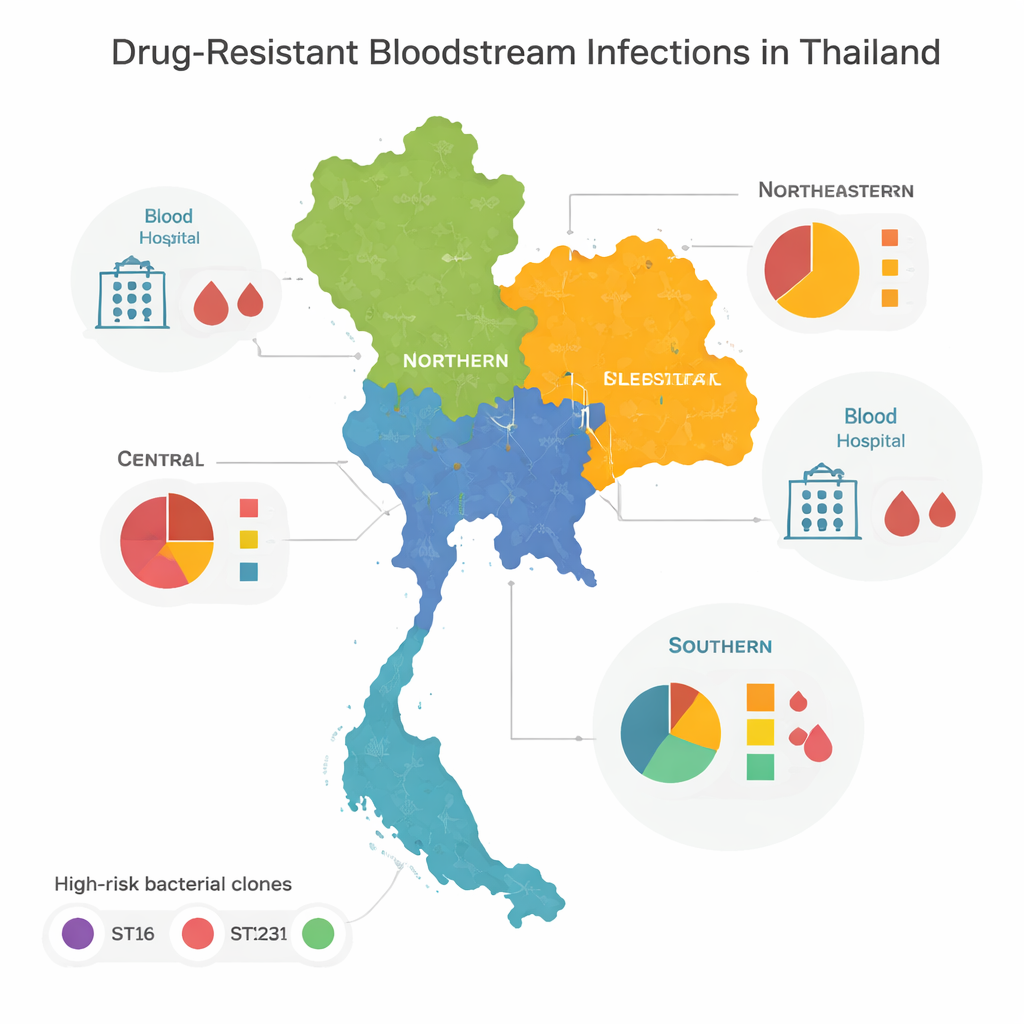
نسخ عالية الخطورة وأنماط إقليمية
عند مقارنة الجينومات، وجد الفريق أن معظم البكتيريا المقاومة تنتمي إلى عدد قليل من العائلات «عالية الخطورة» أو النسخ، المعروفة عالميًا بتسببها في تفشيات داخل المستشفيات. ثلاث منها على وجه الخصوص — المسماة ST16 وST147 وST231 — طغت في وسط وشمال وشمال شرق تايلاند. انتشرت هذه النسخ على نطاق واسع عبر المناطق، مما يشير إلى تحرك متكرر للمرضى أو الموظفين أو البكتيريا بين المستشفيات. بدا الجزء الجنوبي من البلاد مختلفًا: بدلاً من هيمنة نوعين أو ثلاثة، احتوى على تنوع واسع من السلالات البكتيرية، العديد منها شوهد مرة واحدة فقط. هذا التنوع يشير إلى مزيج أكثر تعقيدًا من التفشيات المحلية والمصادر البيئية والحركة عبر الحدود بدلاً من سيطرة نسخة أو اثنتين هاربتين.
كيف تتفوق البكتيريا على المضادات الحيوية
كشفت الدراسة كيف تراكمت لدى هذه البكتيريا آليات مقاومة متعددة. حملت العديد من سلالات ST16 وST231 جينات معروفة باسم blaNDM وblaOXA، التي تنتج إنزيمات تكسر مضادات الكاربينيم قبل أن تؤدي وظيفتها. كما ظهر أن بعض العزلات أظهرت تغييرات في غشاءها الخارجي تقلل دخول الدواء، ما يجتمع ليخلق مقاومة بمستويات عالية جدًا. غالبًا ما حملت سلالات ST231 جينًا إضافيًا، rmtF1، الذي يعيق فئة مهمة من الأدوية تسمى الأمينوجليكوزيدات، مقلصًا خيارات العلاج بشكل أكبر. برزت ST147 بمرونتها الجينية: مزجت ووافقت بين جينات ومسوحات (بلازميدات) مختلفة للمقاومة — حلقات حمض نووي صغيرة متحركة — مما يجعلها مركزًا محتملاً لنقل صفات المقاومة إلى بكتيريا أخرى.
فشل الخيارات الأخيرة ومخاطر خفية
أكثر النتائج إثارة للقلق كانت متعلقة بالمقاومة للقولستين، الدواء الذي يحتفظ به الأطباء للمواقف اليائسة. حملت بعض العائلات البكتيرية النادرة جينات mcr، التي يمكن أن تقفز بين الأنواع على البلازميدات وتسبب مقاومة القولستين بشكل مباشر. أخرى، خاصة داخل نسخة ST16، كانت مقاومة للقولستين رغم أنها تفتقر لأي جينات أو طفرات معروفة للمقاومة. هذا يوحي بأن العلماء لم يرسموا بعد كل الطرق التي يمكن للبكتيريا أن تعطل بها هذا الدواء الملجأ الأخير. كما حدد الفريق سلالات فرط-ممرضة — بكتيريا شديدة القدرة على التسبب في مرض خطير — بما في ذلك خط واحد جمع بين فرط القوة والقدرة على مقاومة جميع الكاربينيمات المختبرة، وهو مزيج شديد الخطورة.
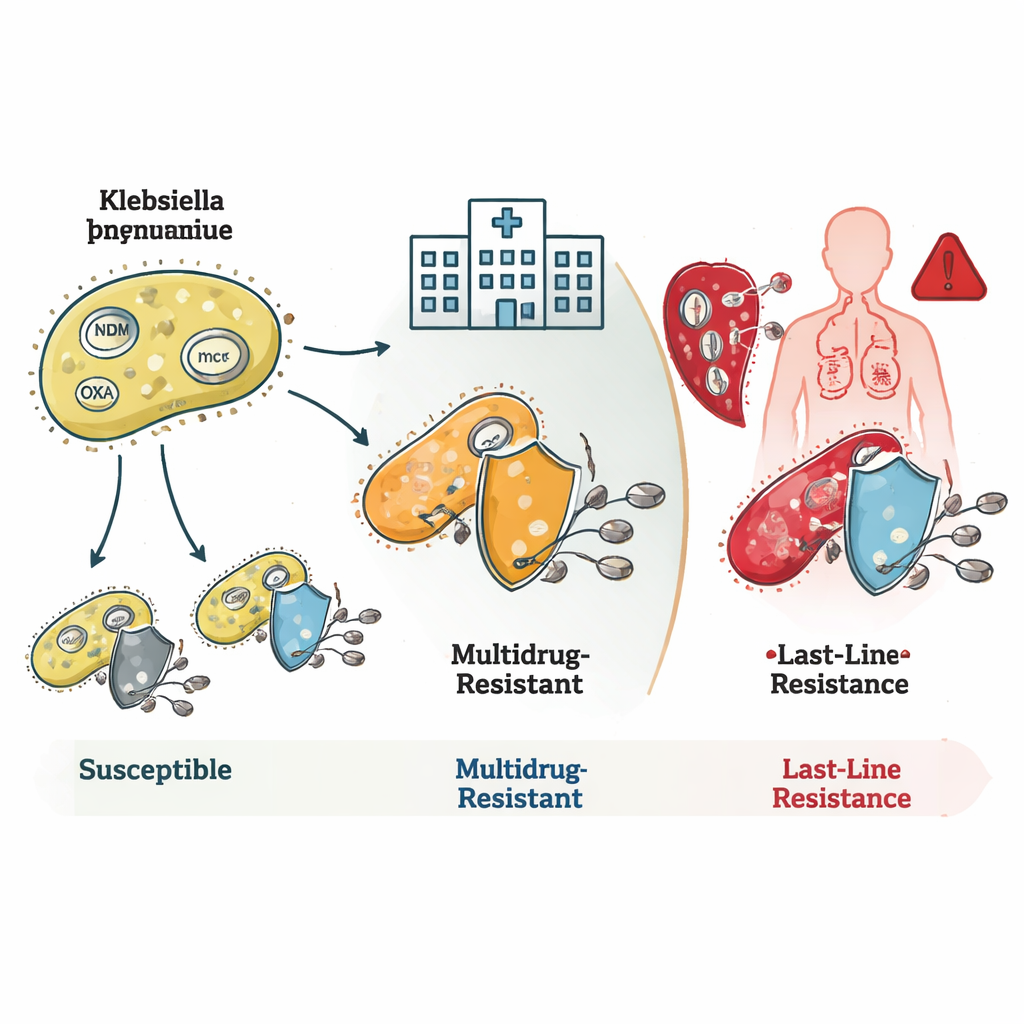
لماذا تهم المراقبة الجينومية
لفهم كيف تحولت التغيرات الجينية إلى فشل دوائي في العالم الحقيقي، استخدم الباحثون نماذج إحصائية لربط جينات مقاومة محددة بنتائج الاختبارات المخبرية الفعلية. أظهرت جينات مثل blaNDM-1 وأقاربها ارتباطات قوية للغاية مع مقاومة الكاربينيم، مؤكدة دورها المركزي في دفع فشل العلاج. ومع ذلك، بالنسبة للقولستين، كان لدى معظم البكتيريا المقاومة علامات مقاومة غير معروفة، ما يشير إلى آليات خفية لا تزال بحاجة لاكتشاف. يجادل المؤلفون بأن الاستخدام الروتيني لتسلسل الجينوم الكامل في مراقبة المستشفيات يمكن أن يعمل كرادار إنذار مبكر، يكتشف النسخ عالية الخطورة الناشئة، ويتتبع حركتها عبر المناطق والحدود، ويوجه استجابات سريعة للسيطرة على العدوى.
ماذا يعني هذا للمرضى والسياسة
بالنسبة للقارئ العادي، الرسالة صارخة وواضحة: بعض عدوى مجرى الدم في تايلاند تُسبَّب الآن ببكتيريا تقاوم تقريبًا كل الأدوية المتاحة للأطباء، وبعض عائلات هذه الميكروبات الخطرة تنتشر على نطاق واسع. في المقابل، تظهر الدراسة أنه بالأدوات المناسبة — عينات وطنية، وتحليل جيني، ومشاركة سريعة للبيانات — يمكن لأنظمة الصحة اكتشاف هذه التهديدات مبكرًا والتكيف معها. قد يساعد توسيع المراقبة الجينومية، وتطوير اختبارات جزيئية سريعة، وتشديد إجراءات مكافحة العدوى في إبطاء تقدم هذه البكتيريا الخارقة وكسب الوقت لتطوير علاجات ولقاحات جديدة.
الاستشهاد: Krobanan, K., Kamjumphol, W., Leethongdee, P. et al. Nationwide genomic surveillance of carbapenem- and colistin-resistant Klebsiella pneumoniae bloodstream isolates in Thailand (2020–2024). Sci Rep 16, 5853 (2026). https://doi.org/10.1038/s41598-026-36228-4
الكلمات المفتاحية: مقاومة المضادات الحيوية, Klebsiella pneumoniae, عدوى مجرى الدم, المراقبة الجينومية, الرعاية الصحية في تايلاند