Clear Sky Science · ar
الصبغات الدِّستيريـل-BODIPY المستبدلة بالبيريدينيوم والبروم للمعالجة الضوئية الديناميكية الموجهة نحو الميتوكوندريا
إضاءة الخلايا السرطانية من الداخل
المعالجة الضوئية الديناميكية هي علاج للسرطان يستخدم أدوية خاصة تُفعَّل بالضوء لقتل الخلايا الورمية مع الحفاظ إلى حد كبير على الأنسجة السليمة. تبحث هذه الدراسة في عائلة جديدة من الصبغات الفلورية المصمَّمة للالتحاق بمصانع الطاقة داخل الخلية — الميتوكوندريا — وعند تسليط ضوء أحمر عميق عليها تولِّد أنواع أكسجين سامة يمكن أن تدمر الخلايا السرطانية. تعرض الدراسة كلًّا من الإمكانات والتحديات في هندسة مثل هذه الصبغات على المستوى الجزيئي.
لماذا استهداف محطات طاقة الخلية؟
تُعد الميتوكوندريا حاسمة لإنتاج الطاقة وتساهم في تقرير مصير الخلية بين البقاء والموت. تميل الخلايا السرطانية إلى امتلاك غشاء ميتوكوندري مشحون كهربائيًا بدرجة أكبر من الخلايا الطبيعية، وهذا يجعلها تجذب الجزيئات المشحونة إيجابيًا بقوة أكبر. استغل الباحثون هذه الخاصية بربط مجموعة بيريدينيوم موجبة الشحنة بسقالة صبغية فلورية معروفة باسم BODIPY. يساعد هذا التصميم في توجيه الصبغات إلى الميتوكوندريا، حيث يمكن أن تتسبب التفاعلات الكيميائية المحفزة بالضوء في إلحاق أقصى ضرر بالخلايا السرطانية مع الحد من الأذى في أماكن أخرى.
تصميم صبغات أفضل تتفعيلًا بالضوء
أنشأ الفريق ثلاث صبغات متقاربة تسمى PyBHI وPyBMI وPyBBrI تختلف أساسًا في عدد ذرات البروم التي تحتويها (لا شيء، ذرة واحدة، أو ذرتان). تشترك جميعها في بنية طويلة ممتدة تحول امتصاصها وانبعاثها الضوئي نحو نطاق الأشعة تحت الحمراء القريبة — نافذة مفيدة حيث يمكن للضوء أن يخترق الأنسجة أعمق. نظريًا، يمكن لهذه الصبغات أن تستخدم مسارين داخليين مختلفين للوصول إلى حالة مثارة ثلاثية (triplet) تنتج أكسجينًا مفردًا تفاعليًا: أحدهما تحفزه ذرات البروم الثقيلة والآخر ينتج عن تحول مؤقت للشحنة داخل الجزيء. 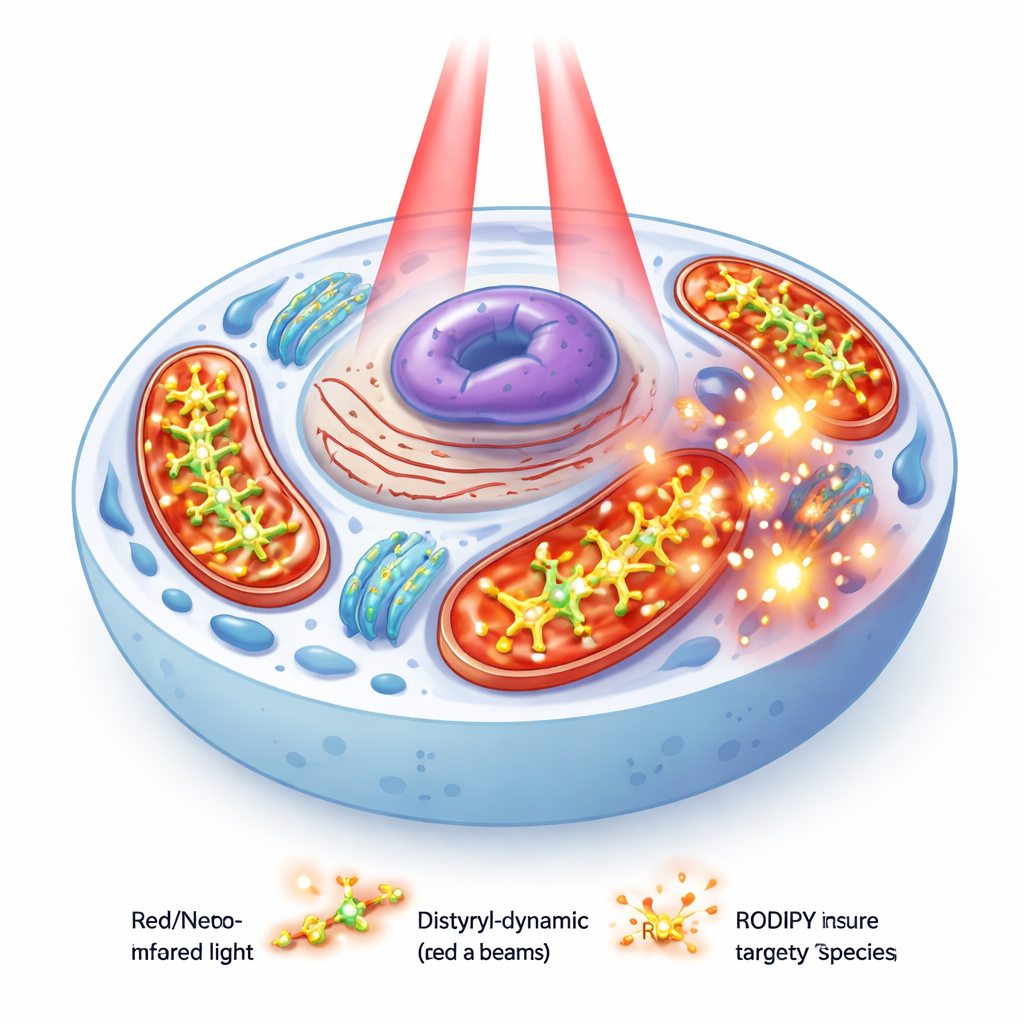
عندما تلتقي النظرية بالواقع التجريبي
على الرغم من التصميم الأنيق، أظهرت الاختبارات المفصَّلة أن الصبغات لم تولد الأكسجين المفرد بالكفاءة المتوقعة. باستخدام مجسات كيميائية تفقد لونها عند التفاعل مع الأكسجين المفرد، قاس الباحثون عائدات توليد أكسجين منخفضة جدًا لجميع الصبغات الثلاث، مع تحسّن طفيف فقط عند إضافة مزيد من ذرات البروم. كشفت تجارب الليزر فائقة السرعة السبب: بعد امتصاص الضوء، تدخل الصبغات بسرعة حالات مزاحة للشحنة ترتد غالبًا على شكل حرارة بدلاً من التحول إلى الحالة الثلاثية المرغوبة. في النسخ المبرومنة، تفتح الذرات الثقيلة مسارًا نحو الحالة الثلاثية، لكن هذا المسار أبطأ بكثير من فقدان الطاقة المتنافس، مما يقيد الكفاءة الإجمالية.
استهداف ميتوكوندريا الأورام في خلايا حية
يتغير المشهد في بيئة حيوية. في خلايا سرطانية بشرية مزروعة من الثدي (MCF-7) وعنق الرحم (HeLa)، أظهرت الميكروسكوبية الكونفوكالية أن الصبغات الثلاث تتراكم بقوة في الميتوكوندريا، مترافقة مع صبغة ميتوكوندرية معيارية. أظهرت اختبارات السمية في الظلام أن الصبغات آمنة إلى حد كبير بدون ضوء. مع الإشعاع الضوئي الأحمر، تسبب الصبغ ثنائي البروم PyBBrI موتًا كبيرًا للخلايا السرطانية، حيث أدت جرعات في نطاق النانومول المنخفض إلى تقليل حيوية الخلايا إلى النصف. كانت الصبغات الأخرى أقل فعالية بكثير. 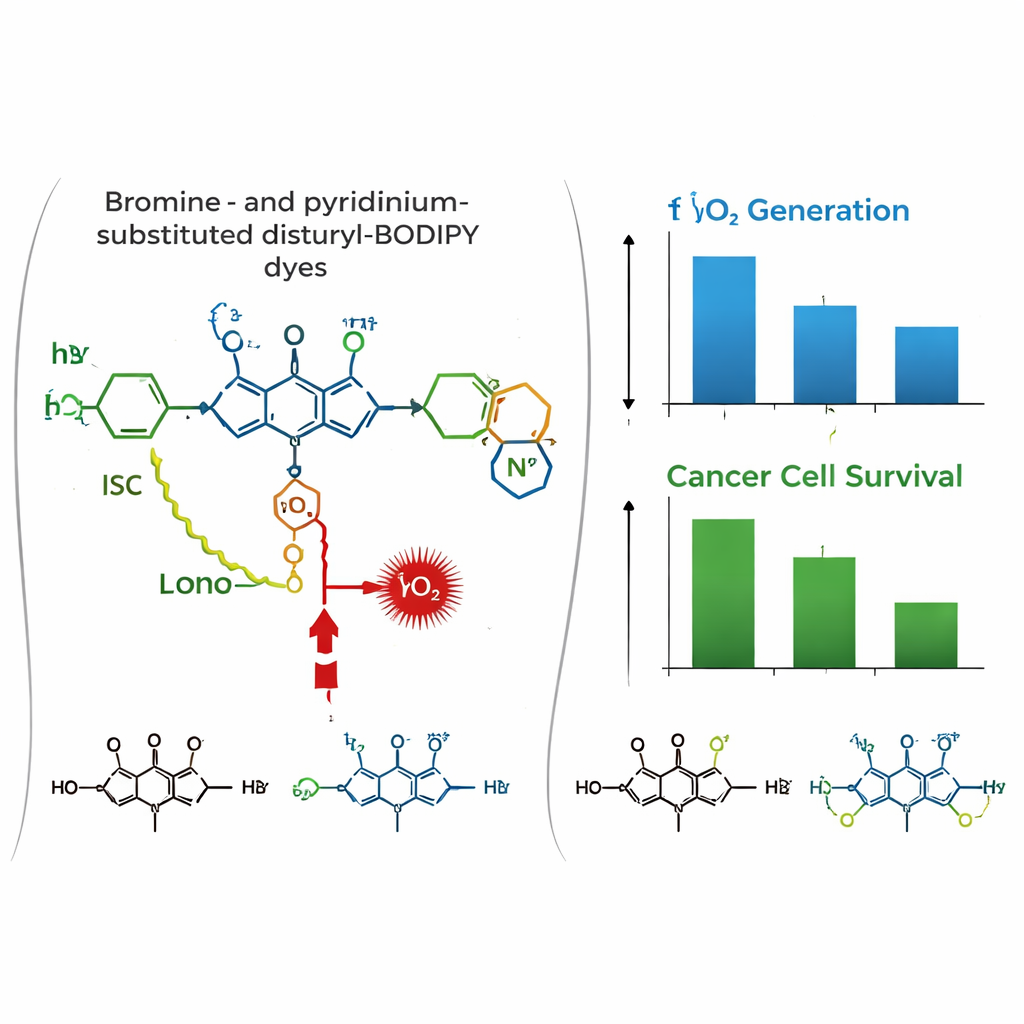
ما الذي يعنيه هذا لعلاجات السرطان المستقبلية
بالنسبة للقارئ غير المتخصص، الرسالة الأساسية هي أن تعديلات كيميائية صغيرة يمكن أن تغيّر بشكل جذري كيفية تصرُّف أدوية السرطان المنشَّطة بالضوء، وأن أداؤها في الخلايا الحية قد يكون أفضل — أو أسوأ — مما تتنبأ به القياسات الأساسية. في هذه الحالة، أظهر الصبغ الأكثر تعديلًا PyBBrI إنتاجًا متواضعًا لأكسجين تفاعلي في أنبوب الاختبار لكنه أبدى فعالية عالية ضد الخلايا السرطانية بمجرد وصوله إلى ميتوكوندرياتها. تُبرز الدراسة أهمية توجيه الأدوية نحو البنى الضعيفة داخل الخلايا السرطانية وتعقيد التنبؤ بكفاءة المعالجة الضوئية الديناميكية. وتشير إلى طريق نحو أجيال مقبلة من العلاجات الموجهة للميتوكوندريا التي تستخدم ضوءًا قريبًا من الأشعة تحت الحمراء لـ"تشغيل" الكيمياء القاتلة للخلايا بشكل انتقائي حيثما يكون ذلك ضروريًا.
الاستشهاد: Kim, C., Badon, I.W., Jo, J. et al. Pyridinium- and bromine-substituted distyryl-BODIPY dyes for mitochondria-targeted photodynamic therapy. Sci Rep 16, 6789 (2026). https://doi.org/10.1038/s41598-026-36213-x
الكلمات المفتاحية: المعالجة الضوئية الديناميكية, ألوان موجهة نحو الميتوكوندريا, BODIPY, أكسجين مفرد, خلايا سرطانية