Clear Sky Science · ar
الإشعاع γ يسبب تغيّرات خلوية فرعية محددة بالمناطق لمؤشرات التصلب الجانبي الضموري والخرف الجبهي الصدغي في دماغ الخنازير
لماذا تهم الجرعات الصغيرة من الإشعاع وأدمغة الخنازير
معظمنا يعتبر الإشعاع ضاراً بحتاً، خاصة للدماغ. لكن عالمنا مملوء بمستويات منخفضة من الإشعاع الناتج عن الفحوص الطبية، وركوب الطائرات، والبيئة. في الوقت نفسه، لا يزال العلماء يحاولون فهم أسباب التصلب الجانبي الضموري (ALS)، المرض الفتاك الذي شل لاعب البيسبول لو جيريغ، وابن عمه القريب، الخرف الجبهي الصدغي (FTD) الذي يهاجم السلوك والشخصية. تسأل هذه الدراسة سؤالاً مفاجئاً ومتفائلاً: هل يمكن لجرعة واحدة ومتواضعة من إشعاع غاما أن تعيد تشكيل كيمياء الدماغ بشكل دقيق بحيث لا تكون ضارة بالضرورة، وربما تكون واقية جزئياً من التغيرات الجزيئية المرتبطة بـ ALS وFTD؟
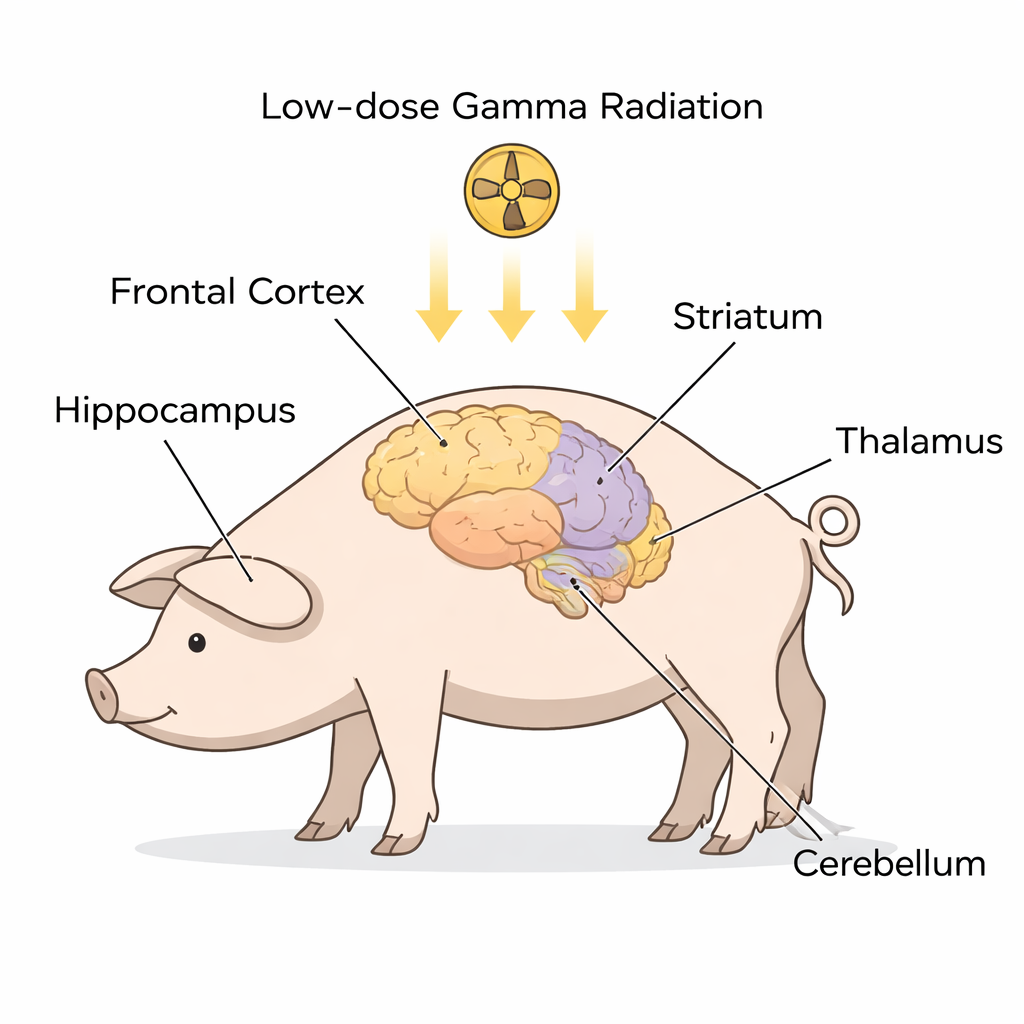
نظرة أقرب إلى علامات التحذير من ALS في الدماغ
بدلاً من فحص مرضى لديهم بالفعل ALS، عمل الباحثون مع خنازير صغيرة من سلالة غوتنغن الصحية، التي تشبه أدمغتها أدمغتنا تشريحياً. تلقى تسعة حيوانات تعرضاً واحداً لكامل الجسم لإشعاع غاما منخفض الجرعة، بينما خضعت ستة لحالة تخدير دون تعريض للإشعاع وكانت بمثابة ضوابط. بعد نحو شهر، قسمت الفرق العلمية خمسة مناطق دماغية رئيسية غالباً ما تُورط في ALS وFTD—القشرة الجبهية، وحصين الدماغ، والمخطط، والمهاد/تحت المهاد، والمخَيخ. في كل منطقة فصلوا محتويات الخلايا إلى قسمين رئيسيين: السيتوبلازم (المساحة المائية داخل الخلية) والنواة (الحجرة التي تحوي الحمض النووي). باستخدام تقنية تُدعى التحليل الغربي (Western blot)، قاسوا مستويات عدة بروتينات مرتبطة بقوة بـ ALS وALS‑FTD، بما في ذلك SOD1 وFUS وC9orf72 وSTMN2 واليوبيكويتين وTDP‑43 وشكل معدل منه يُسمى TDP‑43 المفسفر.
الإشعاع يترك بعض العلامات دون تغيير—وأخرى تتحول
اكتشاف مريح واحد هو أن المستويات الإجمالية لـ SOD1، البروتين الذي تسبب طفراته في بعض حالات ALS الوراثية، لم تتغير في أي منطقة بعد الإشعاع. وبالمثل، ظلت الأشكال الرئيسية من TDP‑43—وهو البروتين الذي يُعثر عليه عادة في تجمعات دماغية متصلة بـ ALS—مستقرة في كل من النواة والسيتوبلازم عبر جميع المناطق. لكن لم يكن كل شيء ثابتاً. رصد الفريق تحولات محددة بالمناطق وبالأقسام الخلوية لعدة بروتينات أخرى. على سبيل المثال، انخفض FUS، البروتين الذي يعيش عادة في النواة ويمكن أن يختل سلوكه ويتجمع في ALS، في سيتوبلازم المهاد/تحت المهاد بعد الإشعاع، بينما ارتفعت مستوياته النووية في القشرة الجبهية وراجعت في الحصين. البروتين المرتبط بـ ALS، C9orf72، لم يتغير في السائل الخلوي لكنه أظهر انخفاضاً داخل نوى الحصين. كما تراجع STMN2، المهم لصيانة المحاور العصبية، في نوى الحصين، مما يوحي باستجابة منسقة بين هذين الجزيئين في تلك المنطقة المرتبطة بالذاكرة.
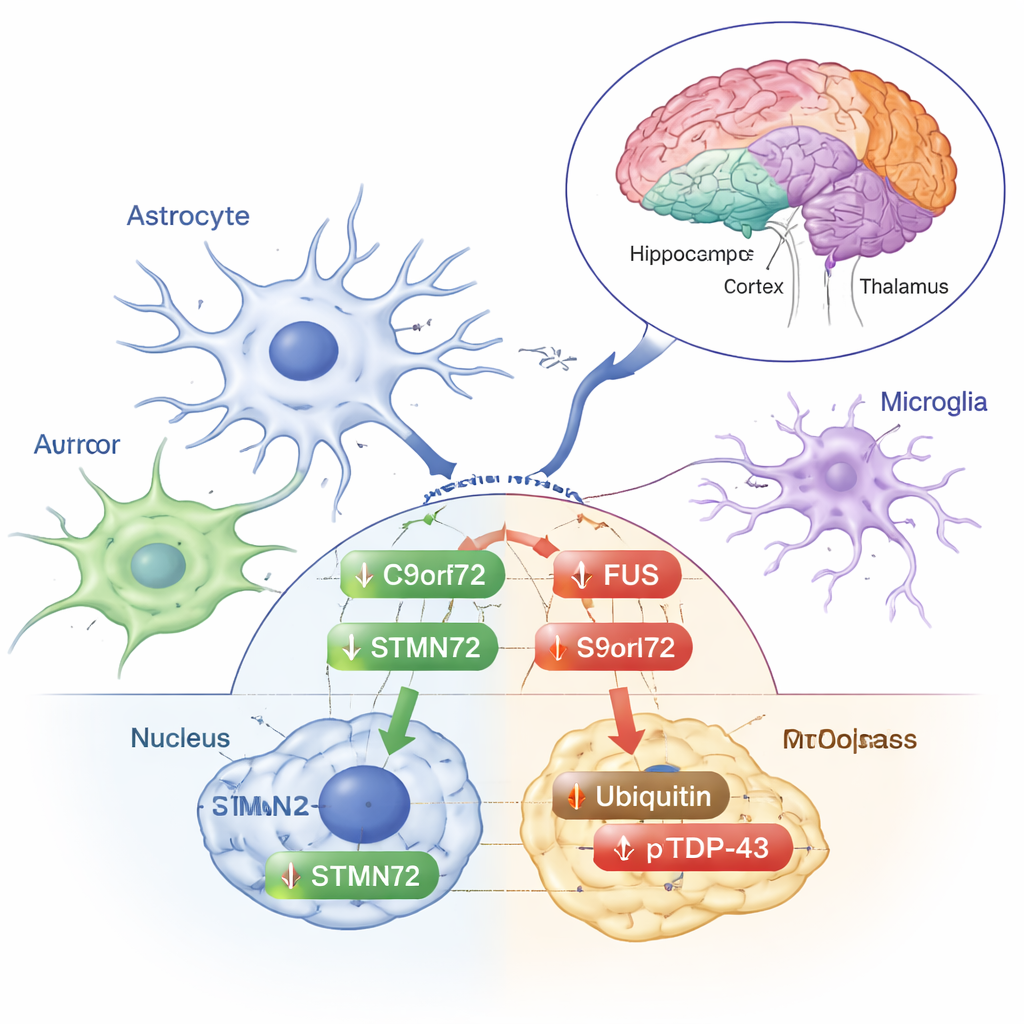
إشارات توتر أم حماية مبكرة؟
بدت تغييرات أخرى أشبه باستجابات توتر تقليدية. اليوبيكويتين—الوسم الصغير الذي تستخدمه الخلية لوضع علامة على البروتينات التالفة لتنظيفها—ازداد في الجزء السيتوبلازمي من القشرة الجبهية. الشكل المفسفر من TDP‑43، الذي يتراكم غالباً في الرواسب الشاذة المرصودة في ALS وFTD، ازداد في سيتوبلازم القشرة الجبهية والمخطط والمهاد/تحت المهاد، رغم أن إجمالي TDP‑43 لم يتغير. تشير هذه التحولات إلى أن الإشعاع منخفض الجرعة يحفز آليات التعامل مع البروتينات في الدماغ من دون أن يطلق أنماط الطي والتجمع الكاملة التي تميز المرض. يؤكد المؤلفون أن هذه الاستجابات تختلف بحسب المنطقة الدماغية وبحسب ما إذا كان البروتين داخل أو خارج النواة، مما يُبرز مدى دقة تكيّف الدماغ مع التوتر.
ما الذي قد يعنيه هذا لخطر ALS—وفوائد محتملة
هل يعني هذا أن الإشعاع منخفض الجرعة يسبب ALS؟ البيانات تبدو مخالفة لإجابة بسيطة بنعم. لم ير الباحثون التشويه المميز أو تراكم البروتينات الأساسية لـ ALS، وكثير من التغيرات تشير إلى تعديل تنظيمي بدل إتلاف صريح. ما يثير الاهتمام أن هذه النتائج تتماشى مع أعمال سابقة من نفس المجموعة وأخرى تقترح أن كميات صغيرة من الإشعاع قد تحرض أحياناً «مفعول الهرمِسِس» (hormesis)—وهي ظاهرة حيث ينشط الإجهاد الخفيف مسارات الإصلاح ويخفض البروتينات الضارة، مثل تلك المرتبطة بمرض ألزهايمر أو باركنسون في نماذج حيوانية. تلميح الدراسة الحالية هو أنه، على الأقل على المدى القصير، تعيد جرعة واحدة منخفضة من إشعاع غاما تشكيل مؤشرات مرتبطة بـ ALS بطرق قد تكون تكيفية أكثر منها مدمرة.
أسئلة كبيرة وأمل متحفظ
للقارئ العام، الخلاصة الأساسية هي أن العلاقة بين الإشعاع وصحة الدماغ أكثر تعقيداً من عبارة «كل الإشعاع ضار». في نموذج حيواني كبير هذا، أحدث التعرض لإشعاع غاما منخفض الجرعة تغييرات دقيقة ومحددة بالمناطق في بروتينات مرتبطة بـ ALS وFTD، من دون إعادة إنتاج أنماط الضرر التي تُرى في أدمغة المرضى. قد تعكس هذه التغيرات محاولة الدماغ التكيف مع التوتر وإصلاحه، وقد تكون في بعض الحالات مفيدة. مع ذلك، نظر الباحثون فقط بعد شهر واحد من تعرض وحيد، وفحصوا الدماغ فقط (وليس الحبل الشوكي، حيث يصيب ALS بشدة). هناك حاجة لدراسات طويلة الأمد ومتكررة الجرعات قبل التفكير في تطبيق هذه النتائج على البشر. ومع ذلك، تفتح هذه الدراسة نافذة جديدة على كيفية تفاعل الإشعاع بمستوى الحياة اليومية مع الجزيئات التي تقوم عليها أمراض التنكس العصبي المدمرة—وتطرح احتمال أنه في ظروف مراقبة بعناية، قد تُستخدم جرعات صغيرة في المستقبل لتحفيز دفاعات الدماغ.
الاستشهاد: Iacono, D., Murphy, E.K., Perl, D.P. et al. γ-Radiation induces region-specific subcellular alterations of amyotrophic lateral sclerosis and frontotemporal dementia markers in swine brain. Sci Rep 16, 5627 (2026). https://doi.org/10.1038/s41598-026-36208-8
الكلمات المفتاحية: التصلب الجانبي الضموري, الخرف الجبهي الصدغي, الإشعاع منخفض الجرعة, بروتينات الدماغ, نموذج خنزير مصغر