Clear Sky Science · ar
خُرطوشة التحلل في الفاج العملاق PhiKZ
كيف تُفجِّر الفيروسات العملاقة البكتيريا
العاثيات—التي تُسمى أيضًا الفيروسات البكتيرية—تُستَخدم كأدوات دقيقة ضد عدوى خطرة مثل تلك التي يسببها Pseudomonas aeruginosa، وهو ميكروب مُقاوم في المستشفيات. أحد العاثيات الكبيرة جدًا، phiKZ، أثار فضول العلماء لأنه يبني حجرةً واقيةً «شبيهة بالنواة» داخل خليقته. ومع ذلك، لم يُعرَف حتى الآن كيف يفتح هذا الفاج العملاق خليقته ليخرج. تكشف هذه الدراسة عن مجموعة الجينات والأدوات الجزيئية التي يستخدمها phiKZ لتوقيت وتنفيذ تلك الخطوة النهائية المتفجرة.
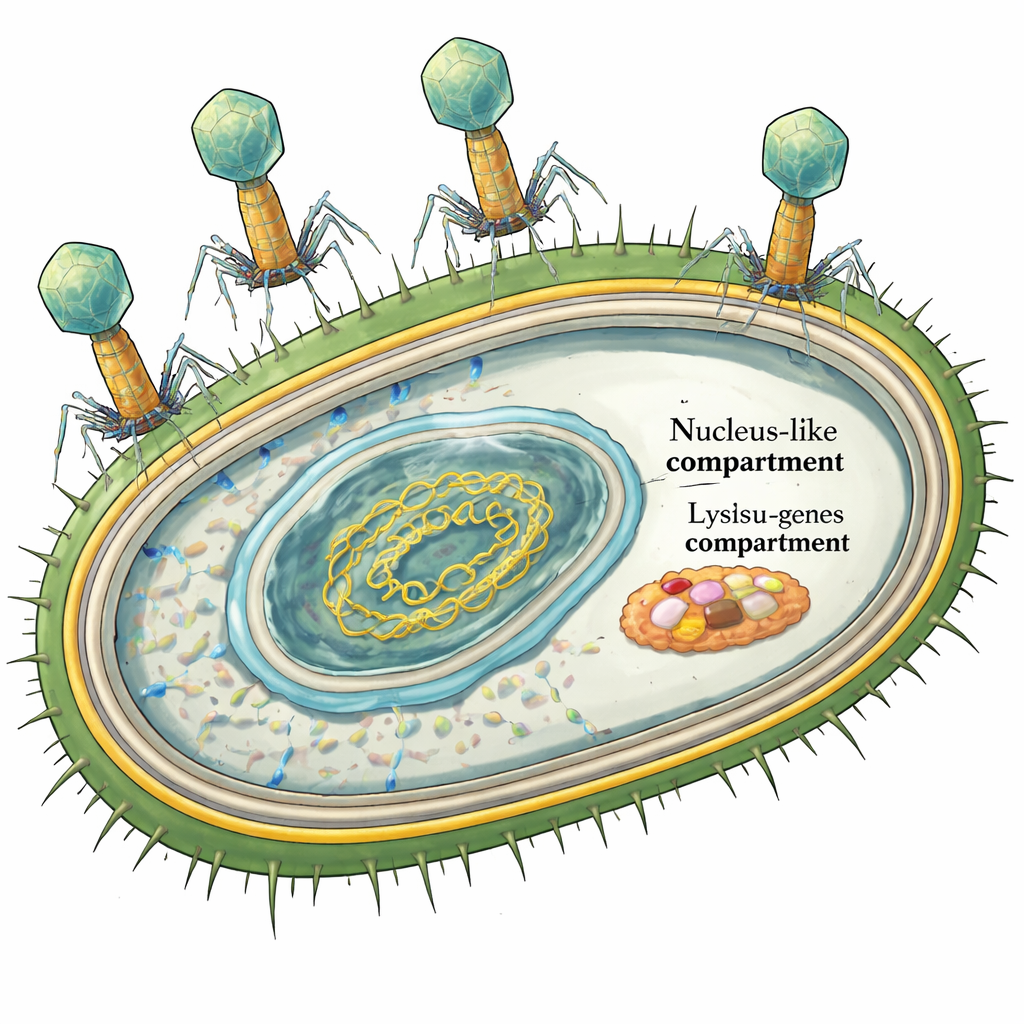
الفاج العملاق وخُطة الهروب
يعد phiKZ فاجًا «هائلاً»؛ جينومه يزيد عن 200000 قاعدية DNA. أظهرت أعمال سابقة بالتفصيل كيف يخفي DNAه داخل غلاف بروتيني ليتفادى دفاعات البكتيريا. لكن المشهد الأخير من العدوى—التدمير المنضبط للخلية البكتيرية—كان لغزًا. معظم العاثيات التي تصيب بكتيريا ذات غشائين، مثل Pseudomonas، تستخدم نظام تحلل مكوّنًا من أربعة أجزاء: بروتين يثقب الغشاء الداخلي، وآخر يقطع جدار الخلية، ومركَّب من جزأين يُسقِط الغشاء الخارجي. وبما أن جينوم phiKZ بدا خاليًا من جين معروف مكوّن للثقوب، اقترح بعض الباحثين أنه قد يستخدم استراتيجية مختلفة تمامًا لإيصال إنزيم قطع الجدار إلى مكانه.
العثور على مجموعة أدوات التحلل المخفية
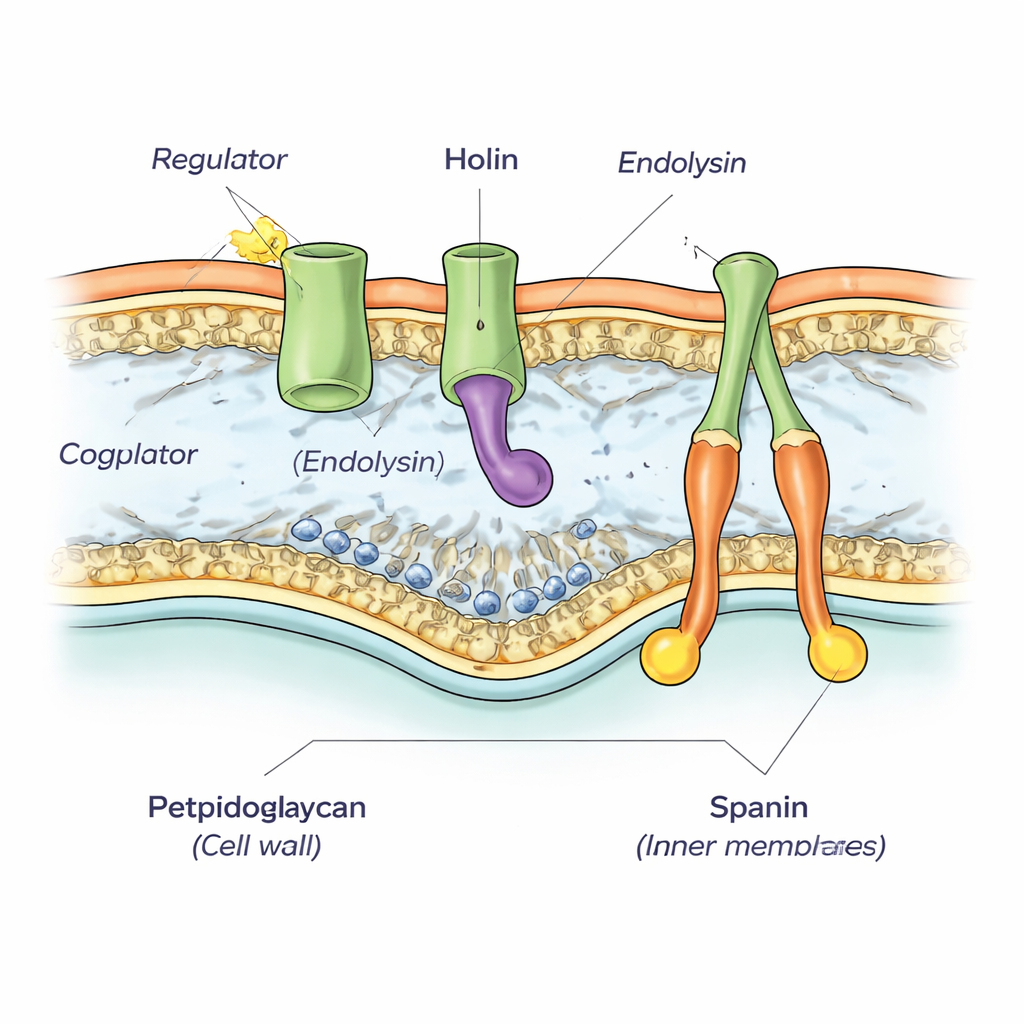
من خلال إعادة فحص المنطقة المحيطة بجين معروف لإنزيم قطع الجدار (المسمى إندوليزين) في جينوم phiKZ، اكتشف المؤلفون مجموعة مترابطة ومكدسة من خمسة جينات. عبر تحليل التسلسل وتنبؤات الحاسوب، أظهروا أن اثنين من هذه الجينات يشفران الـ spanins، زوجًا من البروتينات التي تربط الغشاءين الداخلي والخارجي وتساعد لاحقًا على اندماجهما. جين آخر يشفر الإندوليزين نفسه. أما الجين الرابع فتبين أنه الهولين المفقود—البروتين الذي يتراكم بصمت في الغشاء الداخلي قبل أن يفتح فجأة ثقوبًا كبيرة. أكد الباحثون هذه الوظائف تجريبيًا بنقل جينات phiKZ إلى نظامي العاثية اللمبادية (lambda) وEscherichia coli المعروفين، وأظهروا أن نسخ phiKZ قادرة على تعويض الأجزاء المفقودة.
مفتاح توقيت لتدمير الخلية
الجين الخامس في المجموعة يشفر بروتينًا صغيرًا يبقى في سيتوبلازم البكتيريا بدلًا من الاندماج في غشاء. عندما عبّر المؤلفون عن هذا البروتين بالاشتراك مع الهولين في E. coli، ماتت الخلايا مبكرًا بشكل ملحوظ مقارنةً بعمل الهولين بمفرده، رغم غياب بقية آلية التحلل. يوحي هذا بأن البروتين الإضافي يعمل كمُنظِّم، يدفع الهولين نحو تشكيل المسام أبكر أو بشكل أقوى. عندما قَصَّ الفريق أجزاءً من ذيل الهولين الطويل المواجه للداخل، وجدوا أن المنظّم لم يعد قادرًا على تسريع العملية وفي بعض الحالات حتى أعاق التحلل. النماذج البنائية المُنتَجة عبر برنامج AlphaFold دعمت وجود شراكة فيزيائية بين ذيل الهولين الداخلي والمنظّم، مكوّنة مركبًا ثنائي البروتين مستقرًا.
إشارات إلى آلية تأخير عند جرعات فيروسية عالية
عندما عدَّى الباحثون مزروعات بكتيرية بعدد متغير من جسيمات phiKZ، لاحظوا نمطًا مثيرًا للاهتمام. عند الجرعات الفيروسية المنخفضة، تحللت الثقافة بسرعة وبحدة. لكن عند الجرعات العالية، تأخر التحلل وتمدد على مدى أكثر من ساعتين. هذا الإبطاء غير البديهي يذكّر بظاهرة معروفة باسم تثبيط التحلل (lysis inhibition)، المرصودة في فاج آخر يُدعى T4، حيث تؤدي الإصابات الإضافية إلى إبلاغ الفاج بتأجيل تفجير الخلية ليُنتَج مزيد من الجسيمات الفيروسية. وبما أن phiKZ يمتلك زوج هولين-منظّم قادرًا على تقديم التحلل وأيضًا على منعه في ظل ظروف معينة، يقترح المؤلفون أن نظام تأخير مشابه قد يوجد في هذا الفاج العملاق.
لماذا يهم هذا لِعلاج بالعاثيات
بإثبات أن phiKZ يحمل خرطوشة تحلل تقليدية وإن كانت متطورة—تتضمن هولين، إندوليزين، spanins، ومنظّم توقيت—تُظهر هذه الدراسة أن حتى العاثيات العملاقة الغريبة تعتمد على أدوات مألوفة للخروج من خليقها. للخارجين عن التخصص، الخلاصة أن "توقيت الانفجار" في العاثيات العلاجية يمكن ضبطه بواسطة بروتينات تنظيمية صغيرة تتواصل مع الهولينات مُشكِّلة المسام. فهم هذه مفاتيح التوقيت وتصميمها مستقبليًا قد يساعد في هندسة علاجات عاثية تقتل البكتيريا بأسرع ما يمكن أو—عندما يكون ذلك مطلوبًا—تؤجِّل التحلل لتعظيم تضخيم الفيروسات قبل الضربة النهائية.
الاستشهاد: Manohar, P., Wan, J., Ganser, G. et al. The Lysis cassette of jumbophage PhiKZ. Sci Rep 16, 5840 (2026). https://doi.org/10.1038/s41598-026-36188-9
الكلمات المفتاحية: تحلل العاثيات البكتيرية, العاثية العملاقة phiKZ, نظام الهولين والإندوليزين, عاثية Pseudomonas aeruginosa, تثبيط التحلل