Clear Sky Science · ar
التفكيك البيوكيميائي والابيجينومي لوظيفة TFIIE يكشف عن حاجة انتقائية للجينات في النسخ البشري
إعادة التفكير في "مفبدل" جيني "عالمي"
تعتمد كل خلية في جسدك على نظام دقيق لتشغيل وإيقاف الجينات. غالبًا ما تشرح الكتب المدرسية هذا النظام على أنه يستخدم مجموعة أدوات ثابتة من العوامل "العامة" التي تحتاجها كل الجينات. تعيد هذه الدراسة النظر في هذه الفكرة بالنسبة لعامل واحد من هذا النوع، TFIIE، وتجد أنه ليس مكوّنًا يناسب الجميع. بدلًا من ذلك، يبدو أن TFIIE مهم بشكل خاص لمجموعات محددة من الجينات، العديد منها يساهم في تنظيم الحمض النووي والحفاظ على استقرار الجينوم. يقدّم فهم متى يكون TFIIE مطلوبًا ومتى يمكن تجاوزه صورة أكثر دقة عن كيفية تحكم خلايانا في نشاط الجينات واستجابتها للإجهاد أو المرض.
كيف تبدأ الخلايا عادةً قراءة الجينات
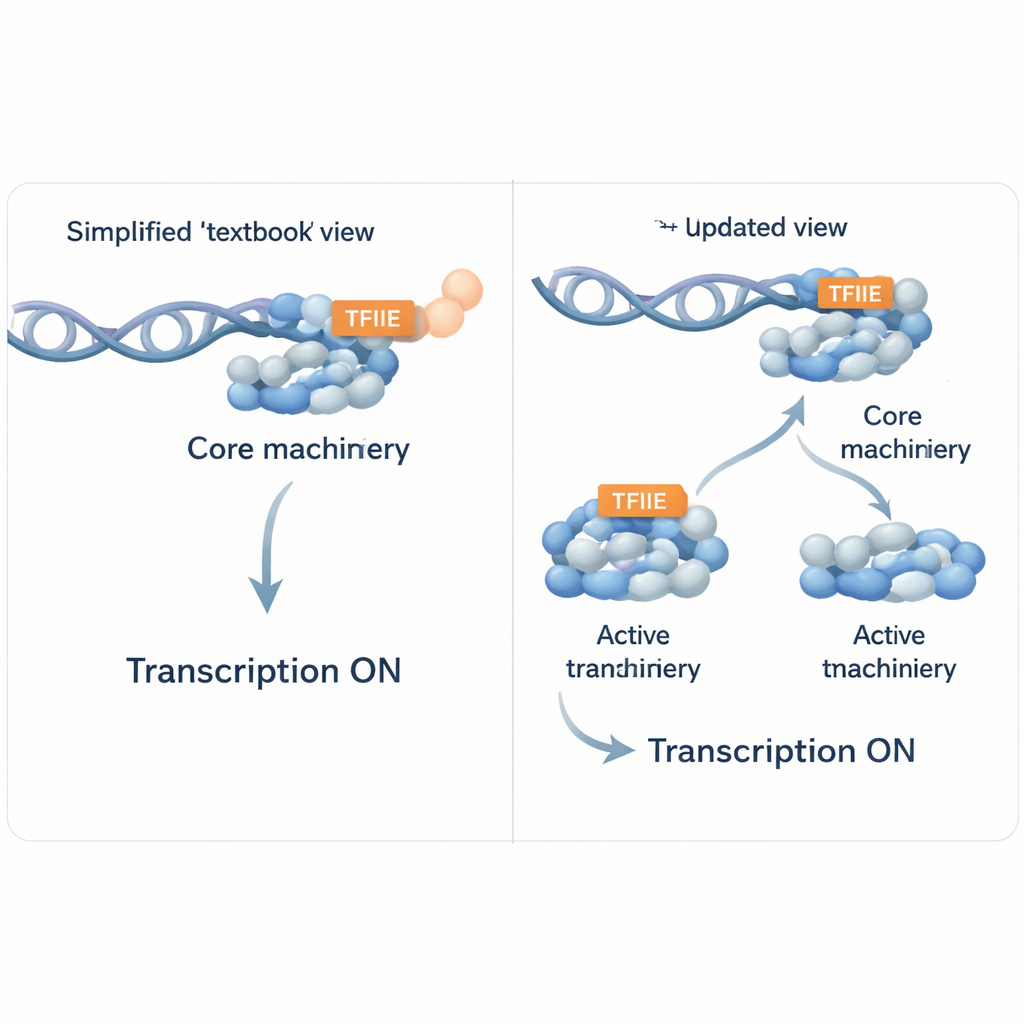
لتفعيل جين، تبني الخلايا مجموعة كبيرة من البروتينات عند "خط البداية" الخاص بالجين، المسمى المُروِّج. تُعرف هذه البنية باسم مركب ما قبل البدء، وتتضمن إنزيم بوليميراز RNA II (الإنزيم الذي يقرأ DNA إلى RNA) والعديد من البروتينات المساعدة التي تُسمى تقليديًا عوامل النسخ العامة. TFIIE هو أحد هذه العوامل المساعدة وكان يُعتقد لوقت طويل أنه أساسي عند تقريبًا كل مروِّج نشط. يساعد في جذب عامل آخر، TFIIH، الذي يفتح الحمض النووي ويسمح لبوليميراز II بالبدء في النسخ. في ظروف مخبرية مبسطة تحتوي فقط على مكوّنات مصفّاة، يبدو TFIIE حقًا لا غنى عنه: عند إزالته، يكاد النسخ الدقيق أن يتوقف.
متى تنهار قاعدة الكتاب المدرسي
سأل المؤلفون ماذا يحدث في بيئة أكثر واقعية لا تزال تسمح بالتحكم الدقيق. استخدموا مستخلصات نووية من خلايا بشرية—خليطًا معقدًا يحتوي على آلاف البروتينات—وأزالوا انتقائيًا مركبًا مساعدًا كبيرًا يسمّى المدييتور، الذي يساعد عادةً في جسر العناصر التنظيمية البعيدة بالمُروِّجات. في هذه المستخلصات الخالية من المدييتور، أعاد الفريق إضافة نسخ مصفّاة مختلفة من مركب المدييتور وراقبوا أي البروتينات ترتبط بمُروِّج نموذجي وما إذا كان يُنتج RNA. من المدهش أنه عندما تم استعادة نواة المدييتور الكاملة، استطاع بوليميراز RNA II أن يرتبط وينتج نسخًا بالرغم من أن TFIIE كان بالكاد قابلاً للكشف عند المروِّج. بعبارة أخرى، في بيئة نووية مزدحمة تحتوي على عوامل إضافية عديدة، يمكن لبعض الجينات أن تُنسَخ دون تجنيد واضح لـ TFIIE، مما يتحدى الفكرة القائلة بأن TFIIE مطلوب دائمًا.
التكبير على أحياء جينية محددة
للاطلاع على كيفية ترجمة هذه النتائج البيوكيميائية عبر الجينوم، فحص الباحثون مجموعات بيانات عامة تُرسم فيها مواقع وجود TFIIE وعوامل رئيسية أخرى على الحمض النووي في خلايا سرطان الدم البشرية. باستخدام تقنية تُسمى ChIP‑seq، ركزوا على المناطق حول مواقع بدء النسخ وسألوا أي المُروِّجات تحتلها TFIIE معًا مع TBP (وهو "وسادة هبوط" جوهرية مرتبطة بالحمض النووي)، وحدة من المدييتور (MED1)، أو مكوّن من مركب المُحَفّز ATAC (ZZZ3). وجدوا أن TFIIE لا يرتبط في كل مكان، بل بمجموعة مميزة من المُروِّجات. بعض المُروِّجات حملت TFIIE مع TBP وMED1، وأخرى مع TBP وZZZ3، ومجموعة ثالثة بدت غنية خصوصًا بـ TFIIE نفسه مع قليل من علامات المدييتور التقليدية. أشارت معاينة الإشارة الخام بعناية إلى أن المُروِّجات "التي تحتوي على TFIIE فقط" غالبًا ما تظهر حضورًا ضعيفًا لكن حقيقيًا لـ TBP، مما يدل على طيف من الشغل بدلًا من فئات صارمة من كلٍّ أو لا شيء.
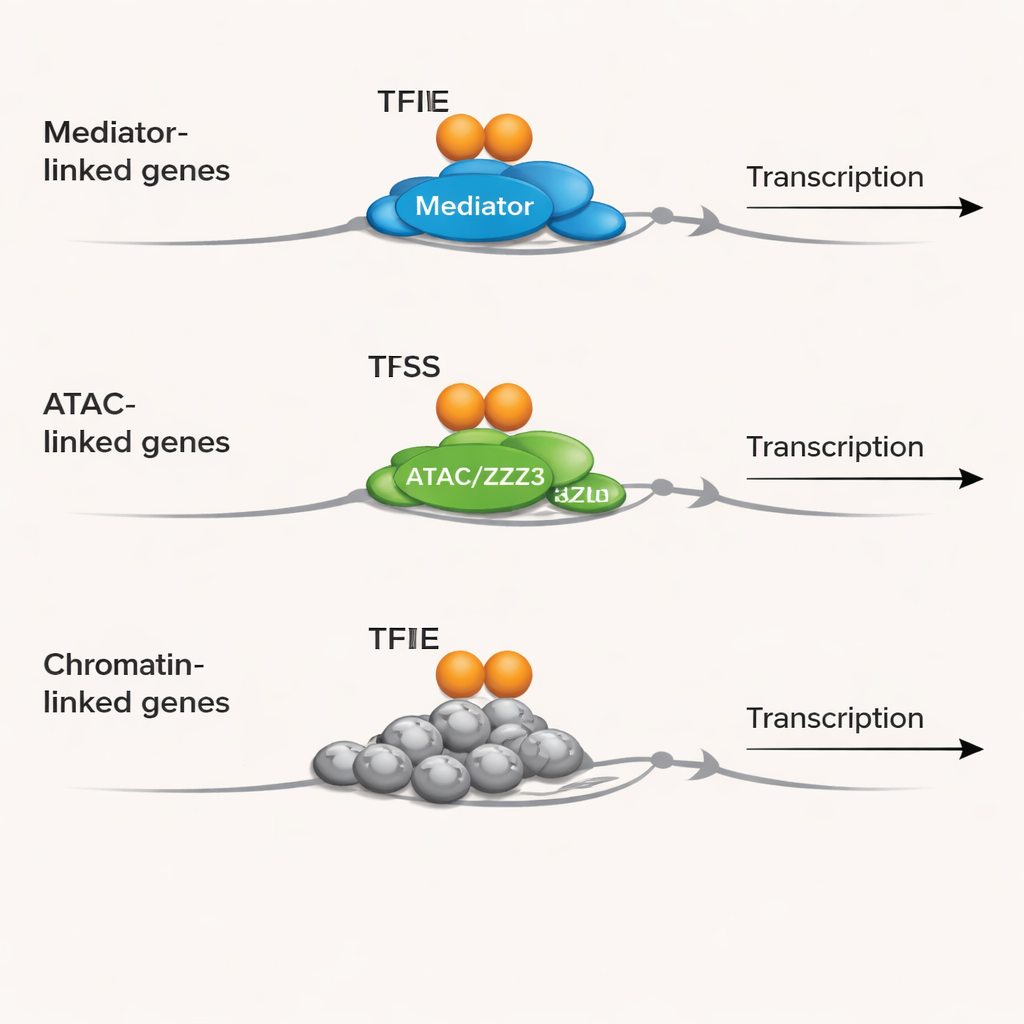
مجموعات شركاء مختلفة، وظائف مختلفة
من خلال ربط هذه المجموعات من المُروِّجات بالوظائف الجينية المعروفة، اكتشف الفريق أن TFIIE يبدو متخصِّصًا. المُروِّجات التي يعمل فيها TFIIE مع TBP وMED1 ترتبط بقوة بالجينات المشاركة في اقتران وتمييز الـ RNA، ومعالجة الـ RNA، والتحكم في إنتاج البروتين—خطوات تُنقّح وتفسّر الرسائل المكوّنة من الـ DNA. المُروِّجات التي يعمل فيها TFIIE مع TBP وZZZ3 مُثرية للجينات التي تبني الرايبوسومات، وتجميع مركبات البروتين–RNA، وإصلاح الحمض النووي، مما يربط TFIIE بنمو الخلية الأساسي وصيانة الجينوم. في الوقت نفسه، المُروِّجات المعلمة أساسًا بواسطة TFIIE نفسها مليئة بالجينات التي تشكل الكروماتين—الطريقة التي يلتف بها الـ DNA حول البروتينات لتشكيل النيكلوزومات—وتؤثر في التنظيم الابيجيني. يشير هذا النمط إلى أن TFIIE يساعد في تنسيق متى وكيف يتم ربط بنية الكروماتين وتعاملات الـ RNA ببدء النسخ.
ماذا يعني هذا لرؤيتنا عن التحكم الجيني
بشكل عام، تجادل الدراسة بأن TFIIE ليس متطلبًا جامدًا وعالميًا بل لاعبًا مرنًا تعتمد أهميته على البيئة المحلية للجين وشركائه. في الأنظمة المصفّاة، يؤدي إزالة TFIIE إلى توقف النسخ، لكن في بيئة النواة الغنية، يمكن لأحماض بروتينية أخرى أحيانًا التعويض بحيث تظل بعض الجينات قادرة على التشغيل. في الوقت نفسه، تكشف الخرائط عبر الجينوم أن TFIIE يميل إلى التركّز عند المُروِّجات التي تتحكم في معالجة الـ RNA، وإنتاج الرايبوسومات، وإصلاح الـ DNA، وتنظيم الكروماتين. للمختصر، أحد أجزاء آلة قراءة الجينات التي كان يُفترض أنها "أساسية" في الواقع يساعد في ضبط برامج متخصِّصة تحافظ على تنظيم الـ DNA وتوازن تداول المعلومات في خلايانا—رؤى قد تؤثر في النهاية على فهمنا للسرطان والاضطرابات النمائية وحالات أخرى يختل فيها تنظيم الجينات.
الاستشهاد: Cevher, M.A., Wijerathne, P.N., Yozgat, Y. et al. Biochemical and epigenomic dissection of TFIIE function reveals gene-selective requirement in human transcription. Sci Rep 16, 5797 (2026). https://doi.org/10.1038/s41598-026-36090-4
الكلمات المفتاحية: تنظيم الجينات, بدء النسخ, TFIIE, تنظيم الكروماتين, مركب المدييتور