Clear Sky Science · ar
مواقع R5 وR7 على هياكل الفلوروكينولونات تحفز تعطيل خيوط F-الاأكتين
تحويل المضادات الحيوية إلى مساعدات دماغية
تشترك العديد من اضطرابات الدماغ الشائعة، من مرض الزهايمر إلى باركنسون، في سبب خفي: قضبانٍ هيكلية دقيقة داخل خلايا العصبية تصبح عالقة ومتصلبة بمرور الوقت. هذه القضبان تتكوّن من بروتين يُدعى الأكتين، الذي يمثل عادةً جزءًا مرنًا من السقالة الداخلية للخلية. تستكشف هذه الدراسة احتمالًا مفاجئًا — أن فئة معروفة من المضادات الحيوية، الفلوروكينولونات، يمكن إعادة تصميمها لتفكك هذه الحزم الضارة من الأكتين برفق وربما تساعد في حماية الدماغ.
عندما تسوء سقالات الخلية
تُعيد خلايا الدماغ السليمة تشكيل هيكلها الداخلي باستمرار لتكوين وتعديل الروابط. خيوط الأكتين مركزية في هذه العملية، إذ تتكوّن وتذوب حسب الحاجة. تحت الضغوط، مع ذلك، يمكن أن يقفل الأكتين في شكل تكتلات عصوية عنيدة تُعيق الخلية، وتعرقل نقل الحمولة الحيوية، وتشجع تراكم بروتينات مرتبطة بالمرض مثل الأميلويد والتاو. على مدى سنوات، يمكن أن تتمايز هذه القضبان إلى هياكل كثيفة معروفة بأجسام هيرانو، والتي تُرى شائعًا في أدمغة أشخاص يعانون من عدة حالات تنكسية عصبية. وبما أن الأدوية الحالية المستهدفة للأكتين غالبًا ما تكون سامة للغاية، يحرص الباحثون على العثور على جزيئات صغيرة أكثر أمانًا تستطيع تفكيك هذه التكتلات دون إلحاق الضرر بالخلايا.
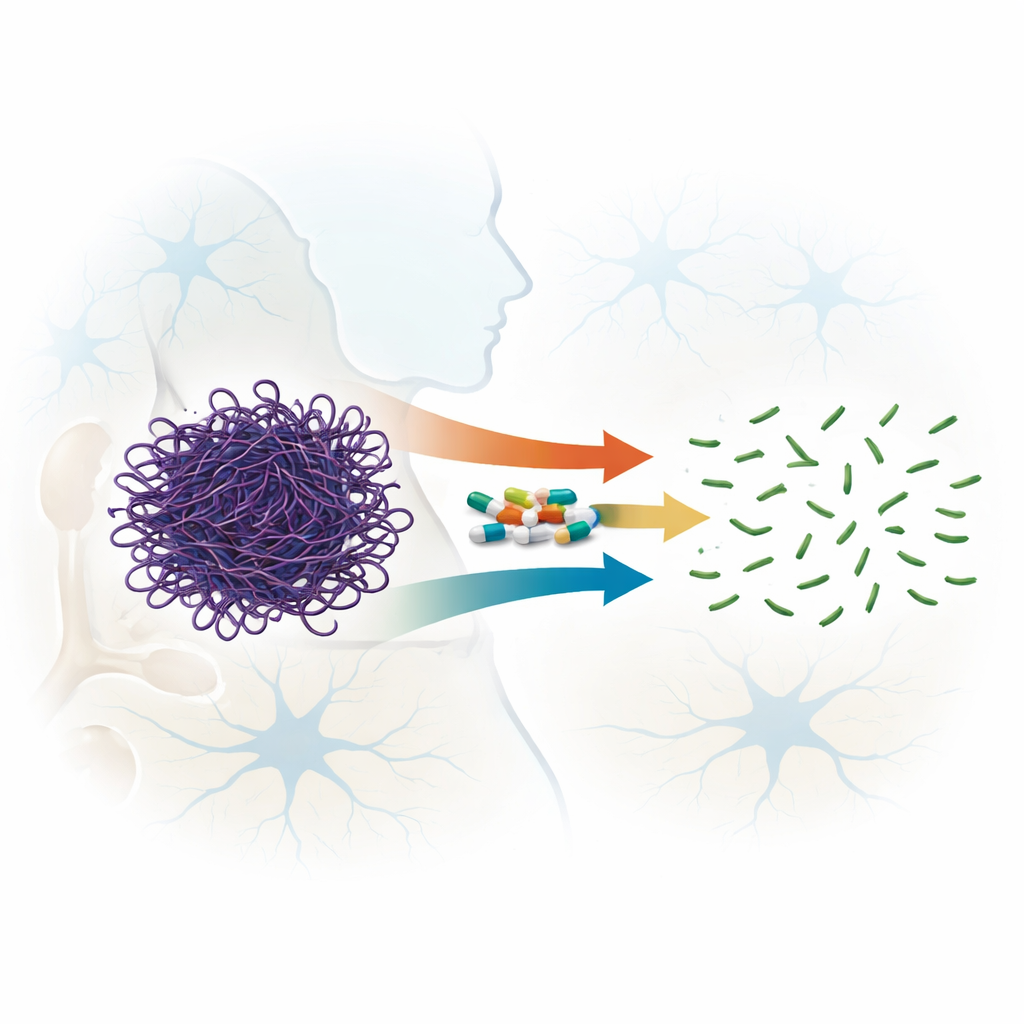
موهبة غير متوقعة لأدوية مألوفة
الفلوروكينولونات هي مضادات حيوية واسعة النطاق تُستخدم عالميًا لعلاج العدوى، وبعض الأعضاء الأحدث في هذه العائلة قادرة على عبور الحاجز الدماغي الدموي. أشارت مؤشرات سابقة إلى أن بعض الفلوروكينولونات قد تزعزع خيوط الأكتين. في هذا العمل، قارن المؤلفون منهجيًا سبعة مركبات مرتبطة، تمتد عبر أربعة أجيال من عائلة الدواء، ليروا مدى قدرتها على تفكيك خيوط الأكتين المشكلة سابقًا بدلاً من مجرد منع تكوّنها. باستخدام قياسات تشتت الضوء والمجهر الإلكتروني والترشيح الهلامي، أظهروا أن جميع الأدوية المختبرة قادرة على تعطيل خيوط الأكتين، لكن بقوة متفاوتة جدًا. برز عقاران، سبارفلوكساسين (مركب من الجيل الثالث) وموكسيفلوكساسين (الجيل الرابع)، بقدرتهما على تقطيع الخيوط الطويلة بسرعة وبشكل لا رجعة فيه إلى قطع أصغر بكثير، حتى عند نسب دواء إلى بروتين منخفضة نسبيًا.
رؤية تفكك الخيوط
كشفت تصويرات عالية الدقة وقياسات بيوفيزيائية كيف تتغير الخيوط تحت المعالجة الدوائية. أظهر المجهر الإلكتروني أن الأكتين غير المعالج يشكل خيوطًا طويلة ومستمرة، في حين أن الفلوروكينولونات الفعالة تحولها إلى شظايا قصيرة ومتفرقة. أنتجت الأعضاء الأقل فعالية خيوطًا مثنية ومحدبة لكنها لم تكسرها تمامًا. أكدت قياسات الاستقرار الحراري للبروتين هذا التفكك الفيزيائي: بعد المعالجة، تصرف الأكتين بشكل أقرب إلى شكله الحر غير المُركَّب، مع درجات انصهار أقل، ومع ذلك ظل بنيانه الأساسي للوحدات البنائية شبه دون تغيير. هذا يشير إلى أن الأدوية لا تُطيّل أو تتلف الأكتين نفسه — بل تفصل بشكل أساسي طريقة تلاصق الوحدات داخل الخيوط.
تكبير على القبضة الجزيئية
لفهم لماذا تعمل بعض الفلوروكينولونات أفضل من غيرها، جمع الفريق تجارب مطوّرة للرنين المغناطيسي النووي مع محاكيات حاسوبية لتداخلات الدواء–البروتين. وجدوا أن جميع المركبات تعتمد على "لب" حلقي مشترك للتلامس مع الأكتين، لا سيما عند موضعين على هذا اللب يلمسان الخيط بشكل متكرر. مع ذلك، تؤثر مجموعات كيميائية إضافية مرتبطة في مواقع محددة — تُدعى R5 وR7 — بشكل قوي على مدى وثوق ومكان ارتباط كل جزيء. في أقوى المركبات المفككة، تحمل هذه المواقع مجموعة أمينية وأنظمة حلقية كبيرة تمتد إلى جيبٍ صغير عند واجهة الأشرطة المجاورة للأكتين. هناك، تتداخل مع تلامسات تثبيت رئيسية، بما في ذلك جسر ملحي مهم يساعد عادةً على إبقاء الخيوط متماسكة.
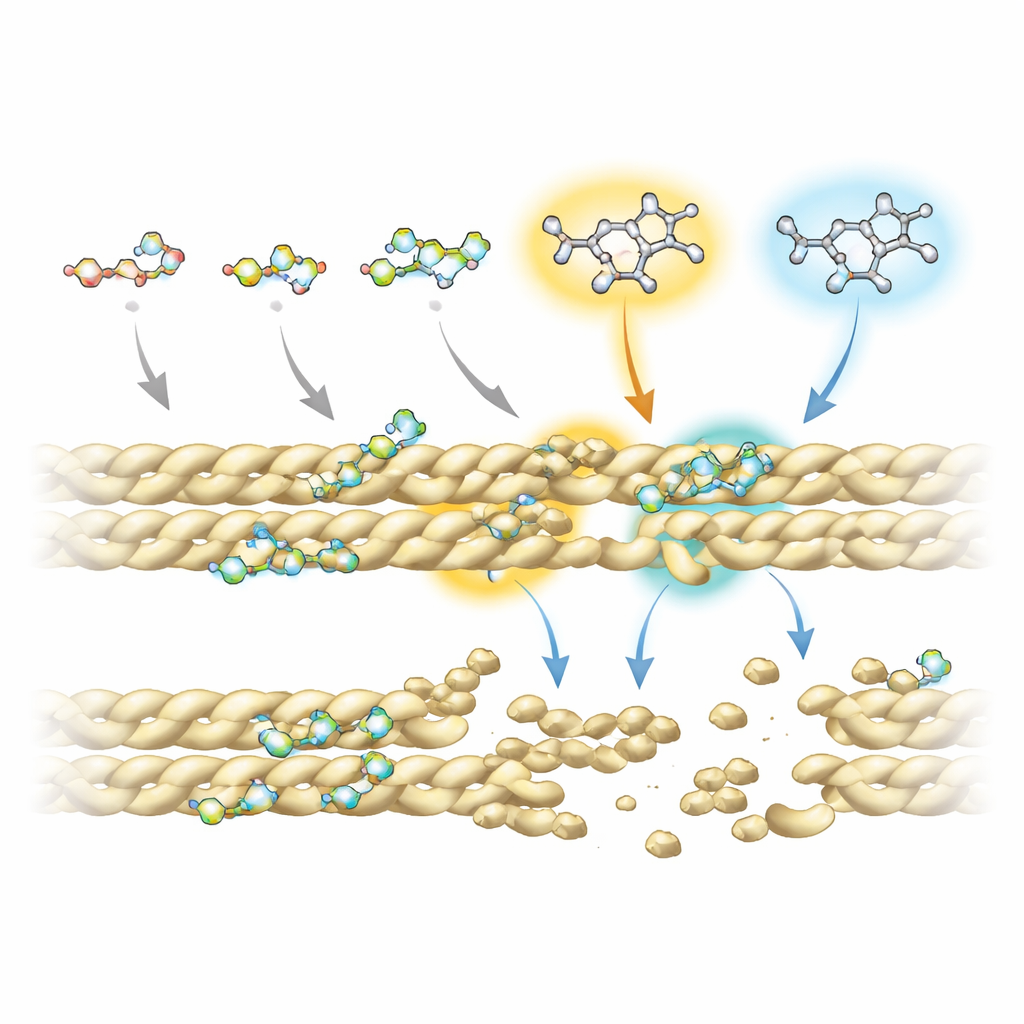
من خلايا الخميرة إلى علاجات مستقبلية
اختبر الباحثون أيضًا الأدوية في سلالة خميرة تتراكم طبيعيًا فيها حزم أكتين، محاكية جوانب من خلايا المرضى. تحت المجهر، أظهرت الخميرة غير المعالجة تجمعات أكتين كبيرة ومضيئة، بينما أظهرت الخلايا المعرضة للفلوروكينولونات — لا سيما سبارفلوكساسين وموكسيفلوكساسين، وعند جرعات أعلى، ناليديكسيك أسيد — أنماطًا أكثر تشتتًا ونقاطية، مما يشير إلى أن الحزم قد تفككت. والأهم أن تأثير الأدوية بدا لطيفًا نسبيًا: فقد أضعفت تعبئة الخيوط دون تحوير شكل الأكتين الأساسي بشكل فادح، وكان ارتباطها أضعف من ارتباط سموم الأكتين الكلاسيكية، مما قد يقلل من خطر الآثار الجانبية الشديدة.
تصميم أدوية أذكى تستهدف الأكتين
بشكل عام، تُظهر هذه الدراسة أن تعديلات طفيفة على مضادات حيوية معروفة يمكن أن تغير جذريًا كيفية تفاعلها مع السقالة الداخلية للخلية. من خلال تحديد موقعي R5 وR7 كـ"مقابض تحكم" رئيسية لكل من تعطيل الأكتين وقدرة النفاذ إلى الدماغ، يضع المؤلفون مخططًا لتصميم جزيئات جديدة مستلهمة من الفلوروكينولون تُفكك انتقائيًا تكتلات الأكتين الضارة. وبينما تظل هذه النتائج دليلًا واعدًا على مبدأ في مرحلة المختبر المبكرة، فإنها تثير احتمال أن تساعد أدوية مستقبلية مشتقة من مضادات حيوية مألوفة في إزالة الهياكل السامة داخل خلايا الأعصاب وإبطاء أو منع بعض أشكال التنكس العصبي.
الاستشهاد: Gupta, R.J., Nair, H., Sarhadi, T.R. et al. R5 and R7 positions on fluoroquinolone scaffolds drive F-actin filament disruption. Sci Rep 16, 9517 (2026). https://doi.org/10.1038/s41598-026-36089-x
الكلمات المفتاحية: تكتلات الأكتين, مضادات حيوية فلوروكينولون, أمراض تنكسية عصبية, إعادة توظيف الأدوية, الهيكل الخلوي