Clear Sky Science · ar
مستشعر ميتامادي غير هيرمتي معزز بالجرافين بتتابع Thue–Morse مستغلًا النقطة الاستثنائية لاكتشاف مؤشرات السرطان
لماذا يهم وجود مستشعر سرطاني أفضل
الاكتشاف المبكر للسرطان يمكن أن يفرق بين علاج بسيط ومرض يهدد الحياة. تعتمد العديد من الاختبارات الحديثة على تلوين الدم أو الأنسجة بصبغات أو جزيئات خاصة، ما قد يكون بطيئًا ومكلفًا ومعقدًا. تصف هذه الورقة نوعًا جديدًا من المستشعرات البصرية — شريحة رقيقة متعددة الطبقات تستخدم الضوء ومواد خاصة وصفائح جرافين فائقة الرقة — لاكتشاف تغيّرات دقيقة مرتبطة بخلايا السرطان والمؤشرات الحيوية دون الحاجة إلى وسم. النتيجة جهاز مدمج قد يساعد الأطباء يومًا ما على اكتشاف السرطان في وقت أبكر وبشكل أكثر موثوقية.
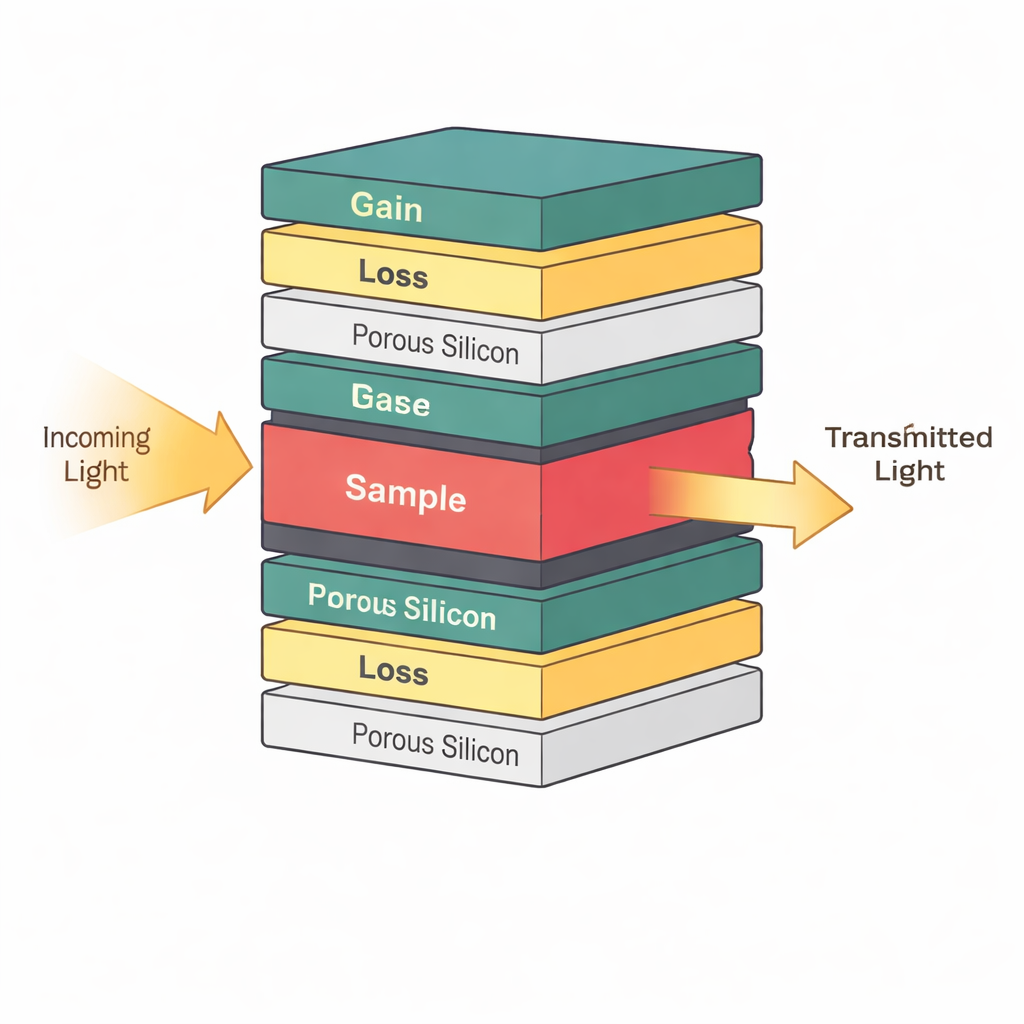
تكديس طبقات موجهة للضوء كقطع أحجية
في صميم الجهاز مجموعة مصممة بعناية من الطبقات فائقة الرقة التي توجه وتحبس الضوء. بدلًا من ترتيب هذه الطبقات بنمط متكرر تام، يستخدم المؤلفون وصفة رياضية تُدعى تتابع Thue–Morse، الذي يقع بين النظام واللاانتظام. هذا النمط شبه النظامي يخلق «نقاطًا حلوة» خاصة حيث يصبح الضوء محصورًا بقوة في مناطق ضيقة من المكدس. في منتصف هذا البناء يدرجون طبقة تحتوي العينة الفعلية — على سبيل المثال مائع يحتوي خلايا سليمة أو خلايا سرطانية. وبما أن الضوء مركز حول هذه الطبقة المركزية، فإن التغيرات الصغيرة في الخواص البصرية للعينة، مثل معامل الانكسار، يمكن أن تغير بشكل ملحوظ كيفية مرور الضوء عبر الجهاز.
استخدام التضخيم والامتصاص والنقاط الاستثنائية لتعزيز الإشارة
يستفيد المستشعر أيضًا من فكرة قوية في البصريات الحديثة تُعرف بتماثل الباريتي–الزمن (PT). ببساطة، بعض الطبقات في المكدس تضخم الضوء قليلًا بينما تمتصه طبقات أخرى قليلاً، مرتبة بحيث يتوازن التضخيم والخسارة حول المركز. عندما يتم ضبط هذا التوازن بشكل مناسب، يصل النظام إلى ما يسميه الفيزيائيون نقطة استثنائية، حيث تندمج وضعيتي ضوء في واحدة. قرب هذه النقطة يصبح الجهاز حساسًا للغاية: اضطراب طفيف في العينة — مثل تغيير بسيط في تركيز الخلايا السرطانية — يسبب تغييرًا كبيرًا بشكل غير متناسب في إشارة الضوء المارة. تظهر الدراسة أن التشغيل قرب هذا الوضع الخاص يجعل ذروة الرنين في الطيف أكثر حدّة، ما يحسّن مباشرة قدرة المستشعر على تمييز الأنسجة أو مستويات المؤشرات الحيوية.
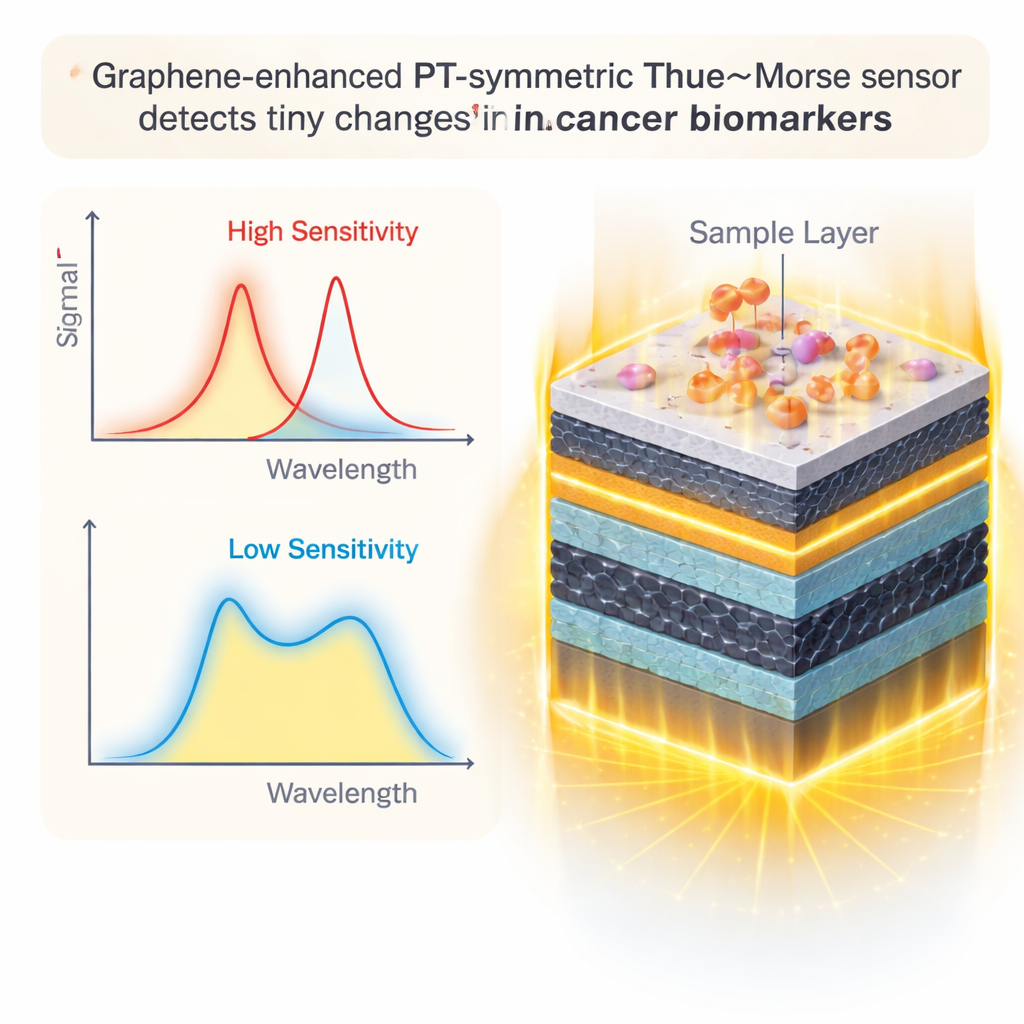
طبقات الجرافين كغطاء مرسّخ للضوء
لتعزيز الأداء أكثر، يضيف الباحثون شرائح من الجرافين — طبقات كربون بسمك ذرة واحدة — عند واجهات رئيسية حول العينة. الجرافين مشهور ليس فقط لقوته وموصلية التيار، بل لطريقة تفاعله مع الضوء. من خلال ضبط خواصه الكهربائية، يمكن للفريق أن يجعل الجرافين يجذب الضوء أقرب إلى منطقة العينة ويقلل الخسائر غير المرغوب فيها. تكشف محاكيات دقيقة أنه عند ضبط المفتاحين الرئيسيين في الجرافين — الكمون الكيميائي وزمن الاسترخاء — على قيم محددة، يصبح الرنين أضيق وأكثر تجاوبًا. إضافة حتى أربع طبقات جرافين حول العينة توفّر أفضل توازن: الإشارة تصبح أقوى وأكثر دقة دون أن تتخمّر بفعل امتصاص زائد.
موازنة تفاصيل التصميم والتصنيع الواقعي
يستخدم الجهاز أيضًا طبقات من السيليكون المسامي، المحفورة بثقوب صغيرة، لاستيعاب المواد البيولوجية وزيادة المساحة السطحية حيث يمكن للخلايا والمؤشرات الحيوية أن تلتصق. يغيّر المؤلفون بشكل منهجي معلمات تصميم عملية مثل سمك الطبقات والنفاذية وزاوية الضوء الداخل، ويفحصون كيف يمكن لأخطاء التصنيع الصغيرة أن تؤثر على الأداء. يجدون أن المستشعر يظل مستقرًا عندما تتغير هذه المعلمات بنحو اثنين في المئة، وهي نطاقات يمكن لتقنيات النانو الحالية تحقيقها عمليًا. مع زيادة عدد طبقات الجرافين يتحسن الحس عمومًا، لكن الكثير من الطبقات يؤدي في النهاية إلى خسارة مفرطة. تحدد الدراسة نقطة توازن في التكوين وظروف التشغيل قد تُرشِد نماذج تجريبية مستقبلية.
ماذا قد يعني هذا للتشخيص المستقبلي
بعبارات رقمية واضحة، يمكن للمستشعر المقترح أن يغير إشارته البصرية بأكثر من 1000 نانومتر لتغير وحدة واحدة في معامل انكسار العينة، مع حد اكتشاف دقيق بما يكفي لتمييز فروق صغيرة جدًا بين الخلايا السليمة والخلايا السرطانية. بينما تصل بعض الأنظمة القائمة على الألياف المتخصصة إلى حدود أدق، إلا أنها غالبًا ما تكون كبيرة الحجم أو صعبة الدمج. بالمقابل، هذا التصميم مدمج، متوافق مع السيليكون، ومصمم للاندماج على الشريحة مع قنوات ميكروفلويديك وطبقات كيميائية حيوية تستهدف مؤشرات سرطانية معينة. بعبارات بسيطة، توضح الدراسة كيف أن الجمع بين نمط طبقات غير اعتيادي، وتوازن التضخيم والخسارة، و«أغشية» الجرافين حول منطقة الاستشعار يمكن أن يحوّل شريحة بصرية صغيرة إلى كاشف سرطاني حساس وخالٍ من الوسم — خطوة واعدة نحو أدوات تشخيصية أسرع وأكثر وصولًا.
الاستشهاد: Mohammadpour, A., Vala, A.S. & Barvestani, J. Graphene-enhanced non-Hermitian Thue–Morse metamaterial sensor exploiting exceptional point for cancer biomarker detection. Sci Rep 16, 6521 (2026). https://doi.org/10.1038/s41598-026-36067-3
الكلمات المفتاحية: مستشعر بيولوجي للسرطان, بصريات الجرافين, جهاز استشعار بصري, بلورة ضوئية, كشف المؤشرات البيولوجية