Clear Sky Science · ar
التحليل البروتيو مثيّ لسيركيتوم خلايا السلف الباطني يحدد Serpine 1 كمُنظّم قوي لتكوّن العظم
شفاء العظم المكسور دون طعوم من المانح
عندما ينكسر العظم بشدة أو يفقد جزءًا منه، يكافح الجراحون غالبًا لاستعادة كل من القوة والشكل. الخيارات الحالية—أخذ عظمة من جزء آخر من الجسم أو استخدام طعوم صناعية—قد تكون مؤلمة، ومحفوفة بالمخاطر، وليست ناجحة دائمًا. تستكشف هذه الدراسة فكرة مختلفة: بدلًا من زرع الخلايا، هل يمكننا توصيل البروتينات الطبيعية المناسبة فقط لإشعال آليات بناء العظم لدى الجسم نفسه؟
لماذا ترفض بعض إصابات العظم الشفاء
تلتئم معظم الكسور من تلقاء نفسها، لكن الفجوات الكبيرة في العظم—مثل تلك الناتجة عن صدمات أو أورام أو تآكل شديد لعظم الفك—غالبًا لا تلتئم. في هذه الحالات، لا يتوفر لدى الجسم عدد كافٍ محليًا من خلايا الأوعية الدموية وخلايا السلف المكونة للعظم لإعادة بناء الجزء المفقود. يحاول الباحثون في هندسة الأنسجة حل هذه المشكلة عبر جمع ثلاثة مكونات: خلايا حية قادرة على تكوين عظم جديد، ومِدْرَع يوفر سطحًا للنمو، وإشارات تخبر الخلايا بما يجب فعله. قد تنجح زَرعات الخلايا، لكنها مكلفة، وتخضع لتنظيم صارم، وليست عملية دائمًا للاستخدام السريري اليومي. دفع ذلك العلماء إلى البحث عن حلول «خالية من الخلايا» تستند إلى مواد بيو-مادّة ذكية وبروتينات مختارة بدقة.
إشارات سرية من خلايا بناء الأوعية
خلايا السلف البطاني نادرة في الدم وتساعد على تشكيل أوعية دموية جديدة. أظهرت أعمال سابقة أنه عند زراعة هذه الخلايا بالقرب من العظم، فإنها تشجع على الشفاء—إلى حد كبير عن طريق إرسال إشارات ذائبة بدلاً من تحويلها إلى نسيج عظمي بنفسها. في الدراسة الجديدة جمع المؤلفون الوسط السائل الذي نمت فيه هذه الخلايا واستخدموا تحليلاً بروتيوميًا متقدماً لحصر مئات الجزيئات المفرَزة. ركزوا على ثمانية بروتينات مرتبطة بقوة بنمو الأوعية الدموية وتكوّن العظم. باستخدام خلايا جذعية نخاع العظم البشرية وخلايا بطانية دقيقة للأوعية البشرية في المختبر، اختبروا بشكل منهجي أيّ من هذه البروتينات عزز أفضل نمو الخلايا، وتوجيه هجراتها، وإطلاق تراكم معادن شبيهة بالعظم.
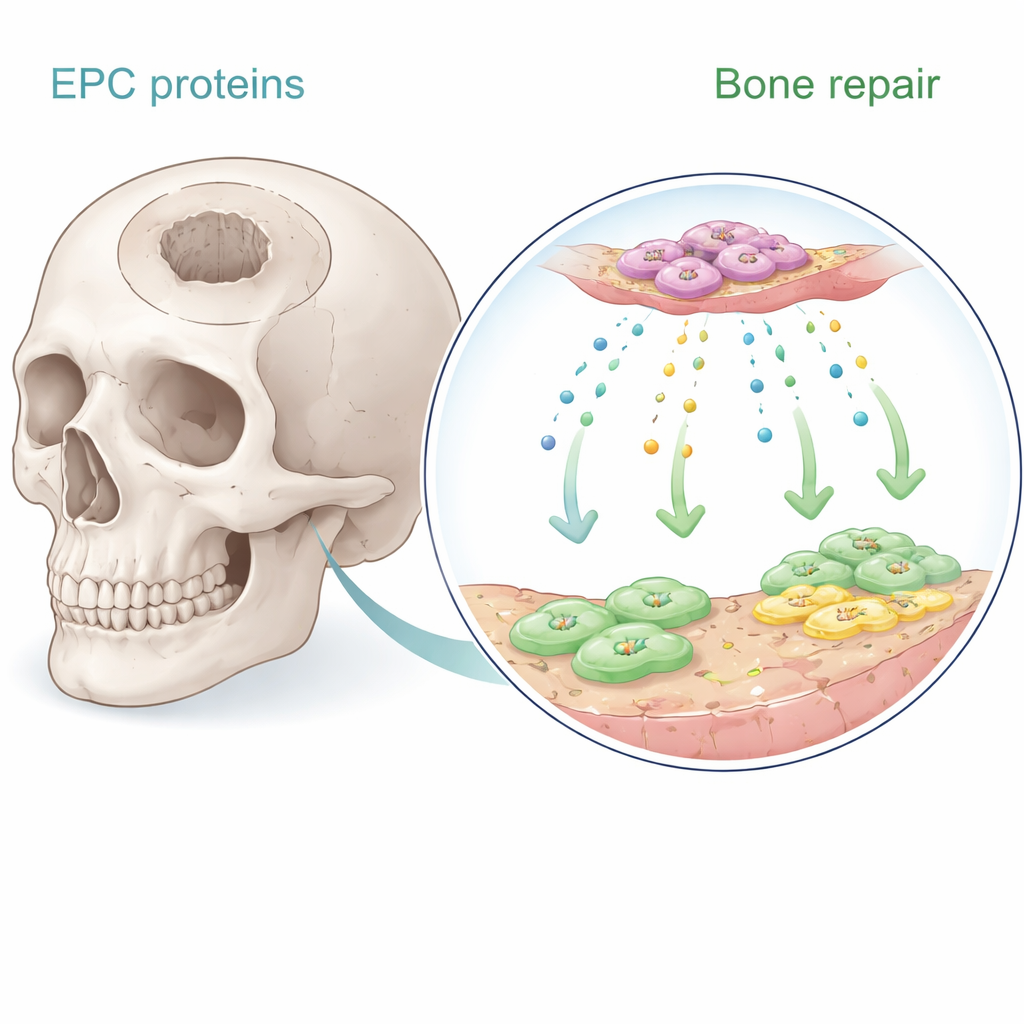
بروتين مفاجئ يتصدر المشهد
بين المرشحين، برز بروتين واحد: Serpine-1، المعروف أكثر بدوره في تنظيم تخثر الدم والتئام الجروح. في أطباق الزرع، زاد Serpine-1 بشكل كبير من تكاثر كل من خلايا جذع نخاع العظم والخلايا البطانية بمعدل مرتبط بالجرعة، متفوّقًا في هذا الجانب على عوامل نمو معروفة مثل BMP-2 وSDF-1. كما عزّز نضوج الخلايا الجذعية إلى خلايا مكونة للعظم، كما أظهرت طرق الصب التقليدية التي تكشف عن نشاط الفوسفاتاز القلوي وترسبات معدنية غنية بالكالسيوم. كانت بروتينات أخرى، مثل عامل نمو الصفائح الدموية وBMP-2، أكثر فاعلية في تحفيز الزحف الخلوي إلى منطقة «جريحة» في اختبارات الهجرة، لكن Serpine-1 قدّم مزيجًا نادرًا من زيادة عدد الخلايا وتعزيز السلوك البنائي للعظم.
تحويل بروتين إلى زِرْع عملي
إيجاد بروتين واعد هو نصف التحدي فقط؛ يجب أيضًا توصيله إلى موضع الإصابة بطريقة متحكم بها. أكمل الفريق Serpine-1 داخل كريات قابلة للتحلل الحيوي مصنوعة من بوليمر طبي يُدعى PLGA، ثم مزجوا هذه الميكروسفرات في هلام كولاجين ناعم. أنشأ هذا مصدًا يطلق البروتين ببطء مع مرور الوقت. اختبروه في الفئران بحفر ثقب دائري بقطر 4 مليمترات في الجمجمة—حجم عيب لا يلتئم من تلقاء نفسه. ملئت بعض العيوب بالكولاجين وحده، وبعضها بالكولاجين مع ميكروسفرات فارغة، وبعضها بمِدْرَع محمَّل بـSerpine-1. بعد ثمانية أسابيع، أظهرت صور ميكرو-CT عالية الدقة أن مجموعة Serpine-1 كانت لديها حجم عظمي وكثافة وسماكة أعلى داخل العيب. واللافت أن هذه الحيوانات فقط طوّرت عظمًا جديدًا في مركز الفجوة، وليس فقط على الحواف.
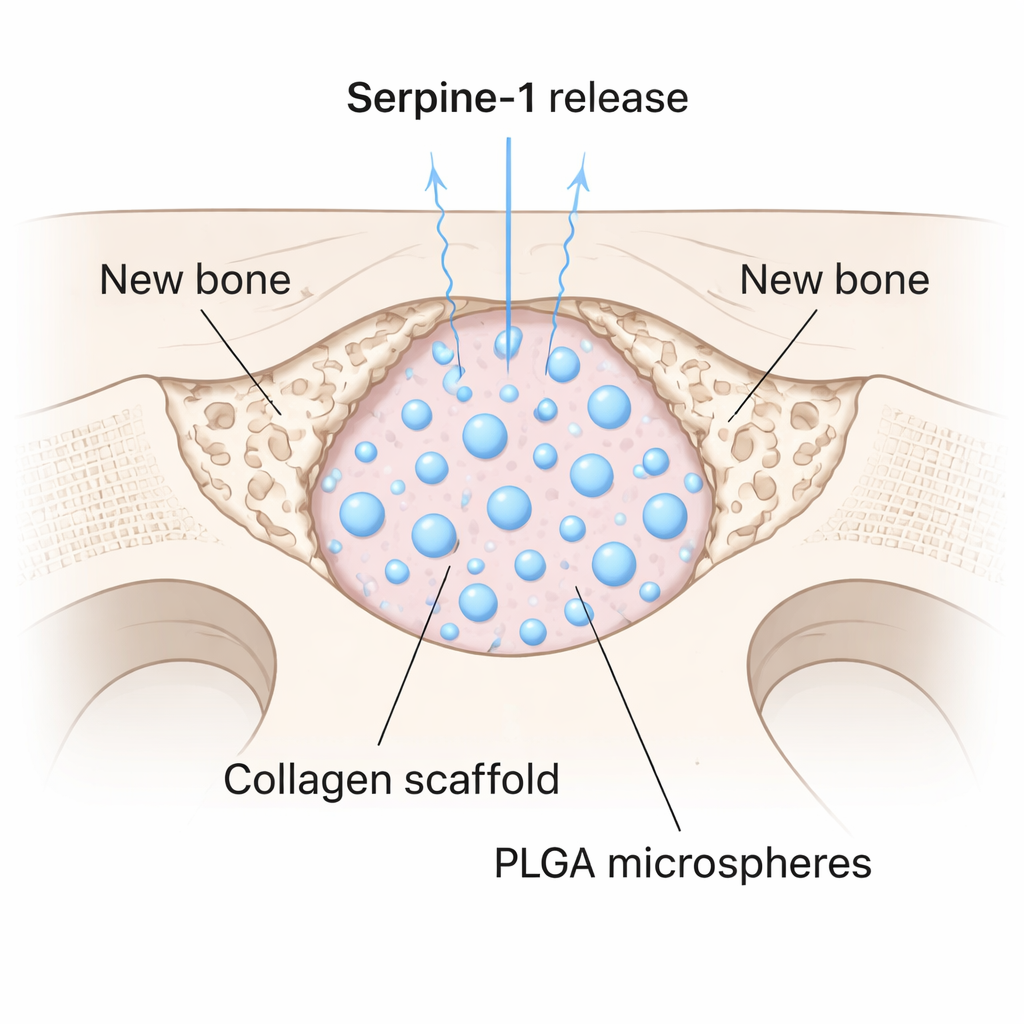
ما الذي قد يعنيه هذا لرعاية العظام في المستقبل
تقدم الدراسة Serpine-1 كإشارة قوية ولم تُقدَّر قيمتها سابقًا في تكوّن العظم. بدمج هذا البروتين مع مِدْرَع إطلاق بطيء، حقق الباحثون إعادة نمو عظمي معنوية في عيب عادةً ما يبقى فارغًا. وبينما لم يجذب Serpine-1 الخلايا إلى العيب بقوة مثل بعض العوامل الأخرى، فإن قدرته على مساعدة الخلايا الموجودة على التكاثر والنضوج تشير إلى أنه يمكن دمجه مع بروتينات تحفز الهجرة للحصول على نتائج أفضل. بالنسبة للمرضى، قد تقلل مثل هذه المواد المعتمدة على البروتين وخالية من الخلايا يومًا ما الحاجة إلى اقتطاع عظم من أجسامهم أو الاعتماد على علاجات خلوية معقدة، مما يقدم طريقة أبسط لحث إصابات العظام العنيدة على الشفاء أخيرًا.
الاستشهاد: Asbi, T., Tamari, T., Doppelt-Flikshtain, O. et al. Proteomic analysis of endothelial progenitor cells secretome identifies Serpine 1 as a potent regulator of osteogenesis. Sci Rep 16, 5165 (2026). https://doi.org/10.1038/s41598-026-36048-6
الكلمات المفتاحية: تجديد العظام, Serpine-1, هندسة الأنسجة, خلايا السلف البطاني, مصدة كولاجين