Clear Sky Science · ar
تأثيرات الازدحام الجزيئي على استقرار البروتين في البروتيوم البكتيري
لماذا تهمّ حياة البروتينات المزدحمة
داخل كل خلية حية، تعمل البروتينات في مساحة مكتظة بالجزيئات الأخرى إلى حد أن ما يقرب من نصف الحجم قد يكون مشغولاً. ومع ذلك، تدرس معظم التجارب المخبرية البروتينات في محاليل مخففة شبه فارغة. تسأل هذه الورقة سؤالاً بسيطاً لكن مهماً: كيف تغيّر هذه الحقيقة المزدحمة استقرار وسلوك البروتينات، وماذا يعني ذلك لعمل الحياة على مستوى الجزيئات؟
لمحة عن عالم خلوي مكتظ
لاستكشاف ذلك، عمل الباحثون مع بكتيريا تُدعى Cupriavidus necator، وهي ميكروب يثير الاهتمام للتقنيات الخضراء مثل احتجاز الكربون وإنتاج البلاستيك الحيوي. فتحوا الخلايا بلطف، محافظين على مئات البروتينات قريبة من أشكالها الطبيعية. ثم أضافوا تراكيز عالية من بوليمرات كبيرة محبة للماء — وكلاء ازدحام شائعة مثل PEG وdextran وFicoll — التي تُستخدم غالباً لمحاكاة داخل الخلايا الكثيف.
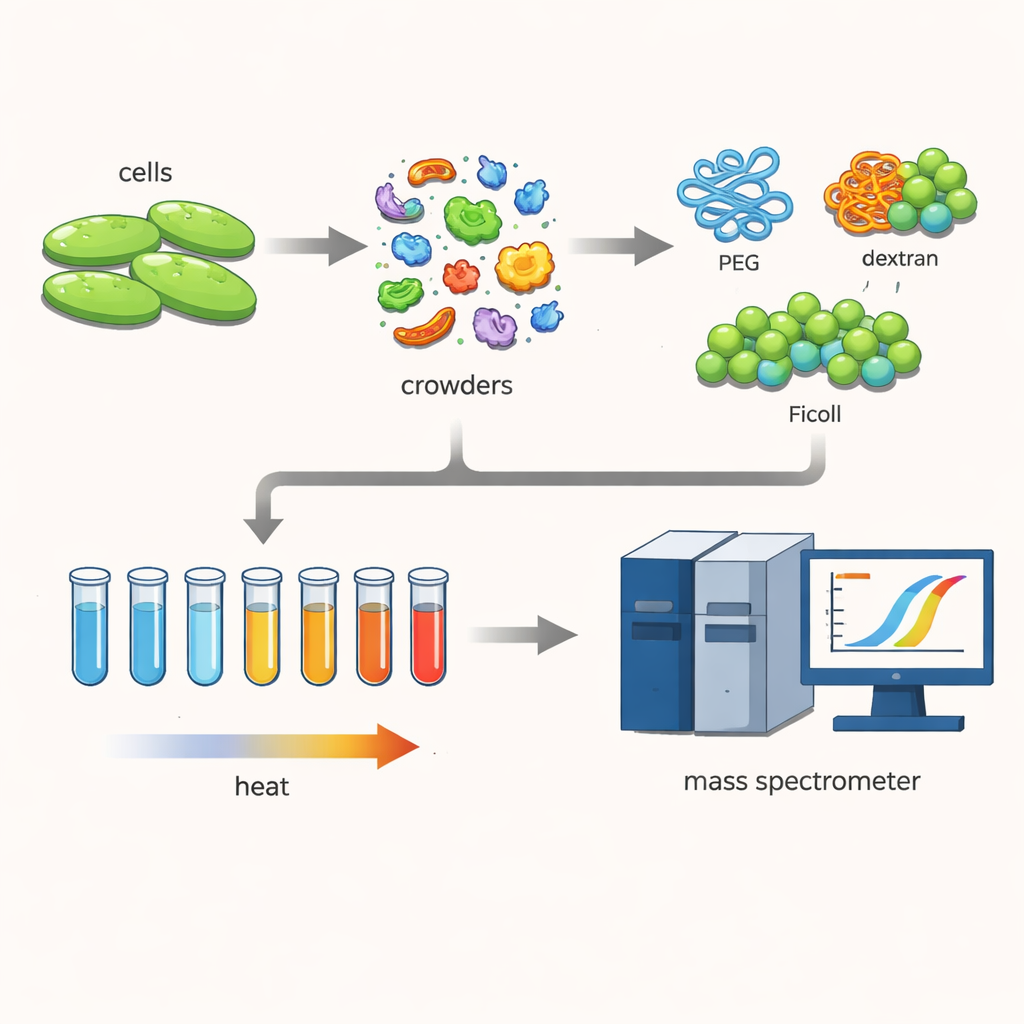
مراقبة ذوبان البروتينات
استخدم الفريق تقنية تُعرف باسم تحليل البروتيوم الحراري. سخّنوا العديد من العينات الصغيرة من مزيج البروتين تدريجياً من 30 إلى 70 درجة مئوية. مع ارتفاع الحرارة، انقلبت البروتينات الأقل استقراراً وتجمع بعضها مع بعض، فخرجت من المحلول. من خلال وسم البروتينات الذائبة المتبقية وقياسها بمطياف كتلة حساس، تمكّن العلماء من إعادة بناء منحنيات الذوبان لكل بروتين وتحديد درجة حرارة الذوبان — النقطة التي يغادر فيها نصف البروتين الحالة الذائبة العاملة. ومقارنة هذه الدرجات مع وجود أو عدم وجود عوامل الازدحام كشفت كيف تغيّر البيئة المزدحمة استقرار البروتينات.
صورة مختلطة: بعض البروتينات أكثر ثباتاً، وأخرى أقل
بشكل عام، أدّى إضافة أي من المواد البوليمرية الست إلى خفض درجات حرارة الذوبان عبر البروتيوم البكتيري، مما يوحي بتأثير مضعِّف طفيف إجمالاً. لكن هذا الاتجاه العام أخفى قصة أكثر تعقيداً. لعشرات البروتينات الفردية، رفعت عوامل الازدحام أو خفّضت الاستقرار بوضوح، أحياناً بعدة درجات. تأثرت معظم البروتينات بأحد المواد الست فقط، لكن عدد قليل منها استجاب لعدة عوامل، وكانت تقريباً كلها إما مُستقرة بصورة متسقة أو مُزعزعة بصورة متسقة، مما يوحي بوجود خصائص مشتركة تُحدّد كيفية تفاعلها مع عوامل الازدحام.
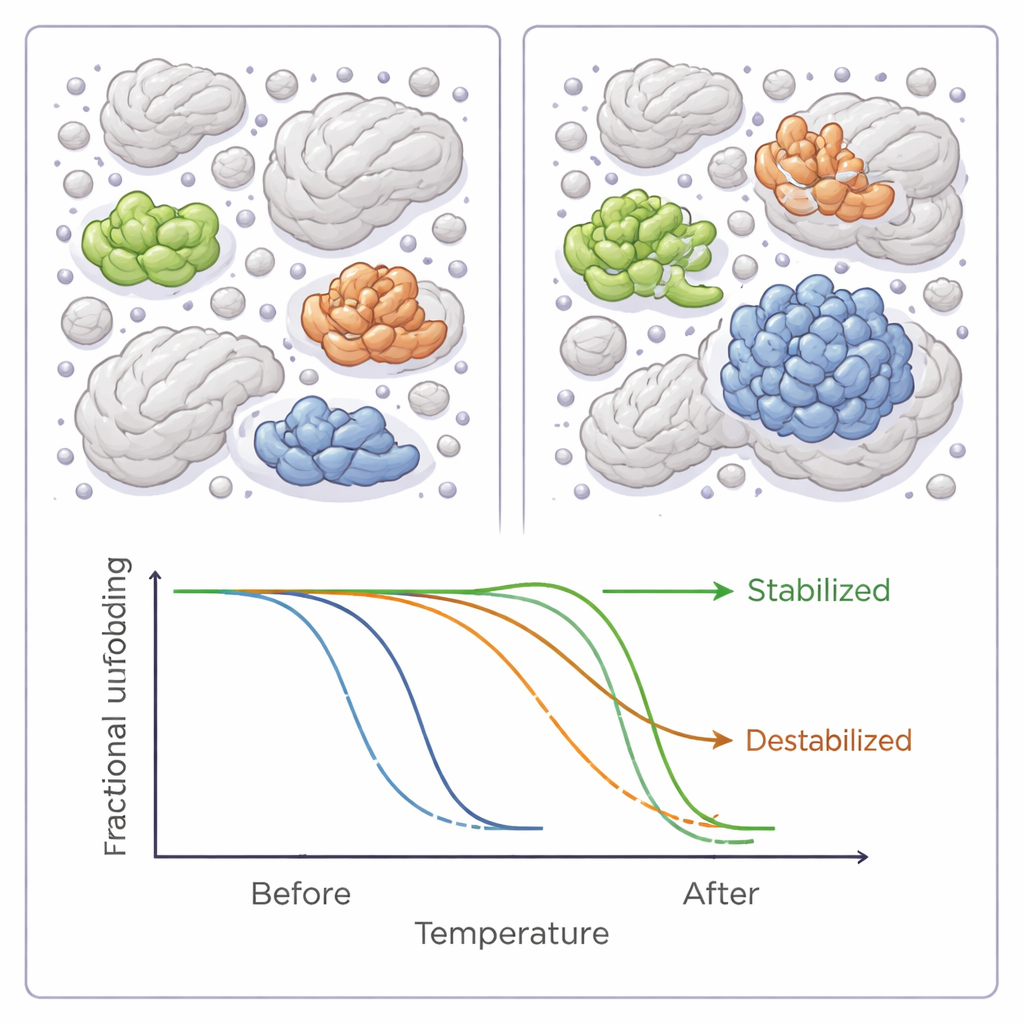
ما الذي يجعل البروتين ينتصر أو يخسر في الحشد
عند فحص خصائص هذه البروتينات الحسّاسة بشكل أدق، برزت أنماط. البروتينات التي أصبحت أكثر استقراراً في ظروف الازدحام كانت تميل لأن تكون أكثر كارهة للماء — أي لها أسطح تطرد الماء — وغالباً ما كانت إنزيمات قياسية ذات مواقع فعالة محددة جيداً. كما كان احتمال ارتباطها بتفاعلات بروتين‑بروتين أو حملها لتعديلات كيميائية تضبط وظيفتها أكبر. أما البروتينات التي أضحت أقل استقراراً فكانت في المتوسط أصغر ولديها عدد أقل من هذه التعديلات. تتناغم هذه النتائج مع نماذج حاسوبية وتجارب أخرى تشير إلى أن الازدحام قد يفضّل بعض البروتينات بينما يجعل أخرى أكثر عرضة للتأثر، اعتماداً على الحجم والشكل وكيفية تفاعلها المعتاد مع الشركاء.
أبعد من الضغط البسيط: كيف تعمل عوامل الازدحام فعلاً
تركز الشروحات التقليدية للازدحام الجزيئي على "الحجم المستبعد"، الفكرة القائلة إن الجزيئات الكبيرة تترك ببساطة مساحة أقل، مما يدفع البروتينات للبقاء مطوية. لو كانت هذه هي القصة كاملة، لكان من المتوقع أن تعمل عوامل الازدحام على استقرار البروتينات بشكل أساسي وأن تُظهر روابط قوية مع مدى ضخامة أو لزوجة البوليمرات. بدلاً من ذلك، لاحظ المؤلفون ارتباطات ضعيفة فقط بالحجم وسُمك البوليمرات. بياناتهم تناسبت بشكل أفضل مع صورة "الاستبعاد التفضيلي": حيث يتجنّب عوامل الازدحام والبروتينات بعضها كيميائياً، مما يفضّل بشكل غير مباشر حالات مطوية معينة لكنه قد يزعج أيضاً التفاعلات الحسّاسة التي تحافظ على استقرار بروتينات أخرى. باختصار، ليس الأمر مجرد ضغط مادي، بل دفع وجذب كيميائيان دقيقان يشكلان سلوك البروتينات.
ماذا يعني هذا لفهم كيمياء الحياة
الرسالة الأساسية لغير المتخصصين هي أن البروتينات داخل الخلايا لا يمكن فهمها بالكامل بمعزل، وهي تسبح في محلول صافٍ. يمكن أن تجعل الغابة الجزيئية الكثيفة من بعض البروتينات أكثر متانة ومن أخرى أكثر هشاشة، مغيرةً طريقة عمل شبكات التفاعلات بأكملها. تُظهر هذه الدراسة، من خلال قياس تغيّرات الاستقرار لمئات البروتينات دفعة واحدة، أن تأثيرات الازدحام مركبة ومحددة لكل بروتين، ومن المحتمل أن يقودها تفاعلات مباشرة بقدر ما يقودها التعبئة البسيطة. أثناء تصميم الباحثين للأدوية أو الإنزيمات الصناعية أو الميكروبات المُهندَسة، سيكون الاعتراف بهذه الحقيقة المزدحمة أمراً حاسماً للتنبؤ بكيفية تصرُّف البروتينات فعلاً في الأنظمة الحية.
الاستشهاد: McKeever, K., Dillon, E.T., Wynne, K. et al. Molecular crowding effects on protein stability in a bacterial proteome. Sci Rep 16, 5908 (2026). https://doi.org/10.1038/s41598-026-35990-9
الكلمات المفتاحية: الازدحام الجزيئي, استقرار البروتين, تحليل البروتيوم الحراري, بروتيوم بكتيري, البيئة الخلوية