Clear Sky Science · ar
نقص Negr1 يغيّر إشارات الجلوتامات ومسار الكينورينين في نموذج فأري للاضطرابات النفسية
لماذا تهم هذه الدراسة الدماغية
العديد من الأمراض العقلية الشائعة، من الاكتئاب إلى الفصام، ترتبط بتغيّرات دقيقة في كيفية تواصل خلايا الدماغ مع بعضها البعض. تدرس هذه الدراسة جين خطر واحد يُدعى NEGR1 في الفئران لمعرفة كيف يغيّر اختفاؤه كيمياء الدماغ والسلوك. من خلال تتبّع كيفية تحرك هذه الفئران بعد دواء يعطّل مؤقتًا مستقبلًا دماغيًا رئيسيًا، وقياس المواد الكيميائية المرتبطة في الدماغ، يكشف الباحثون كيف قد تتضافر العوامل الوراثية والجنس وحالة التمثيل الغذائي في الدماغ لتشكيل القابلية للإصابة بالاضطرابات النفسية.
جين يحافظ على توازن الإشارات الدماغية
ينتج جين NEGR1 بروتينًا على سطح الخلية يساعد الخلايا العصبية على تكوين الروابط وتثبيتها. أظهرت أعمال سابقة أن إزالة هذا الجين في الفئران تغيّر بنية الدماغ، وتقلل بعض التوصيلات المثبطة (GABA)، وتغيّر الاستجابات لأدوية مرتبطة بالدوبامين مثل الأمفيتامين. وبما أن هذه التغيّرات تشير إلى تحوّل نحو إشارات مثيرة أقوى، ركّز الفريق على نظام مثير رئيسي آخر: الجلوتامات ومستقبلات NMDA المرتبطة بها، والتي تلعب دورًا مركزيًا في التعلم والذاكرة والسلوك المرن. كما فحصوا "مسار الكينورينين"، وهو مسار أيضي يكسر الحمض الأميني التريبتوفان إلى مركبات قد تعزز أو تعرقل مستقبلات NMDA.
اختبار السلوك بدواء يغيّر العقل
لفحص وظيفة مستقبلات NMDA، استخدم الباحثون MK-801، دواء معروف يعيق هذه المستقبلات مؤقتًا ويمكن أن يحاكي جوانب اختلال الجلوتامات التي تُرى في الحالات النفسية. كانت الفئران ذكورًا وإناثًا، بعضها يحمل جين Negr1 الطبيعي وبعضها خالٍ منه بالكامل. تلقّت الحيوانات حقنًا يومية من MK-801 وتم اختبارها في ساحة مفتوحة، حيث تم تتبّع حركتها الإجمالية، ووقتها في الزوايا، ودورانها الشبيه بالدوران تلقائيًا. في الذكور غير المعرضة مسبقًا للدواء، أنتجت جرعة واحدة من MK-801 اندفاعًا أقوى من النشاط في الفئران الناقصة Negr1 مقارنةً بالفئران الطبيعية، مما يوحي بأن أدمغتها كانت حسّاسة بشكل غير عادي لهذا الخلل في إشارات الجلوتامات.
نمط مفاجئ من التسامح السريع
عند إعطاء MK-801 بشكل متكرر، تغيّر النمط. في الذكور، ارتفع النشاط في بعض الأيام لكنه انخفض في كل يوم ثاني، مكوّنًا نمطًا متذبذبًا أقترح تسامحًا سريعًا وجزئيًا مع تأثيرات الدواء. على مدى تسعة أيام، أظهر الذكور الطبيعيون استجابة متصاعدة تتماشى مع التحسس، في حين أظهر الذكور الناقصون لـ Negr1 تراكمًا مخففًا للنشاط وتغيّرات أخف من يوم لآخر، مما يشير إلى حساسية معدلة لمستقبلات NMDA. تأقلمت الإناث من كلا الجينوتيبين بسرعة أكبر: بحلول اليوم الخامس تقريبًا لم يعد MK-801 ينتج تأثيرات سلوكية قوية، فتوقّف العلاج. عبر المقاييس، كان للجنس تأثير كبير، وظهرت آثار الجينوتيب بوضوح أساسًا في الذكور.
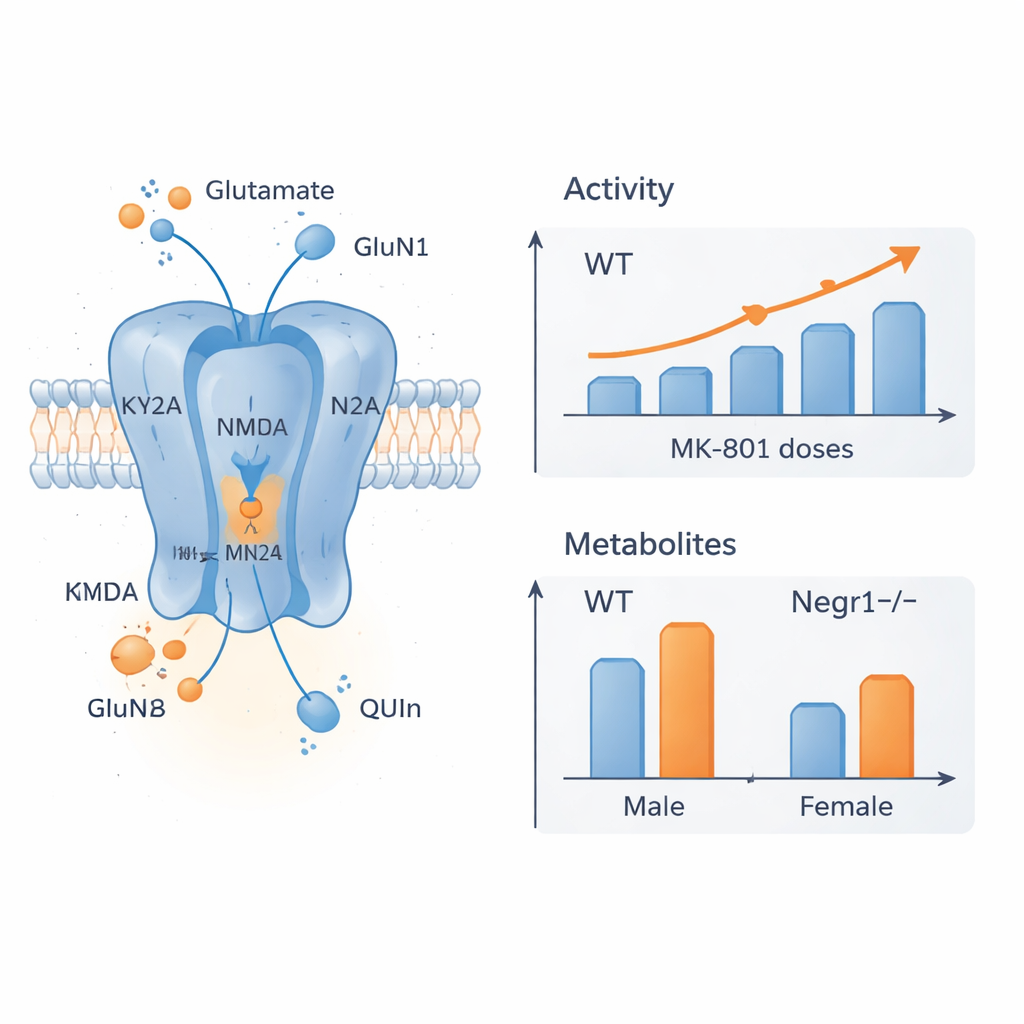
تحولات في المستقبلات والمواد الكيميائية الدماغية
لكشف ما يقف وراء هذه الاختلافات السلوكية، قاس الفريق نشاط الجينات لوحدات فرعية رئيسية من مستقبلات NMDA ولإنزيم ينتج الدي‑سيرين، وهو إشارة مشاركة لهذه المستقبلات. ركّزوا على مناطق دماغية حاسمة للمزاج والإدراك: القشرة الجبهية والحصين. في القشرة الجبهية، أظهرت إناث Negr1 الناقِصات المعالَجات بـ MK-801 انخفاضًا في تعبير وحدات مستقبلية أساسية، مما يوحي بأن أدمغتهن تعدّل تركيب المستقبلات استجابةً للمورِّث والدواء معًا. في حصين الذكور، أظهر الناقِصون لـ Negr1 تعبيرًا أساسياً أعلى لبعض وحدات NMDA، متسقًا مع أدلة سابقة على توافر مستقبلات أكثر؛ ثم أعادت معالجة MK-801 هذه المستويات نحو الطبيعي. بالتوازي، كشفت تحليلات كيميائية مفصّلة للدم ومناطق دماغية متعددة أن عدة مستقلبات من مسار الكينورينين والجلوتامات نفسها تغيّرت بطريقة تعتمد على الجنس والمنطقة، مع تأثر القشرة الجبهية أكثر، وبعض التغيّرات تصير أوضح مع التقدم في العمر.
ماذا يعني هذا لفهم الأمراض العقلية
مجتمعة، تصوّر هذه النتائج NEGR1 كمنظّم جزيئي يساعد في الحفاظ على توازن الإشارات المثبطة والمثيرة في الدماغ، جزئيًا من خلال تشكيل وظيفة مستقبلات NMDA وميتابوليزم التريبتوفان. عندما يغيب Negr1، تستجيب الفئران بشكل مختلف لحصار مستقبلات NMDA، وتظهر تغيّرات كيميائية دماغية تعتمد على الجنس، وتطوّر تدريجيًا تسامحًا بطرق غير معتادة. للقراء غير المتخصصين، الرسالة الأساسية أن جين خطر واحد لا يعمل منعزلًا: تعتمد آثاره على الجنس ومنطقة الدماغ والحالة الأيضية. يعزّز هذا العمل الفكرة القائلة بأن استهداف المسارات المرتبطة بـ NEGR1—بدلاً من التركيز على مستقبل واحد فقط—قد يساعد في النهاية على تصميم علاجات مخصّصة للأمراض العقلية المصحوبة بخلل في الجلوتامات.
الاستشهاد: Kuuskmäe, C., Mikheim, K., Mohammadrahimi, N. et al. Negr1 deficiency alters glutamate signalling and kynurenine pathway in a mouse model of psychiatric disorders. Sci Rep 16, 5317 (2026). https://doi.org/10.1038/s41598-026-35968-7
الكلمات المفتاحية: جين NEGR1, مستقبل NMDA, إشارات الجلوتامات, مسار الكينورينين, الاضطرابات النفسية