Clear Sky Science · ar
كين17 يسهل بدء وتقدم أورام الكِلى عبر مسار PI3K-AKT-mTOR
لماذا تهم هذه الدراسة حول سرطان الكِلية
يتم الآن اكتشاف سرطان الكِلية بمعدلات أعلى، لكن لدى كثير من المرضى تظل الحالة صعبة السيطرة عليها بمجرد أن ينتشر السرطان. تدرس هذه الدراسة الأمور تحت المجهر — حتى مستوى الجزيئات الفردية داخل الخلايا السرطانية — لفهم ما الذي يدفع أورام الكِلية للنمو والغزو، وما إذا كان دواء تجريبي يمكنه إيقاف هذا المسار. وتشير النتائج إلى بروتين غير معروف جيدًا يُدعى KIN17 كمسبب جديد للمشاكل في سرطان الكِلية وتعرض إمكانية استهدافه بشكل غير مباشر بواسطة علاج حبوب.
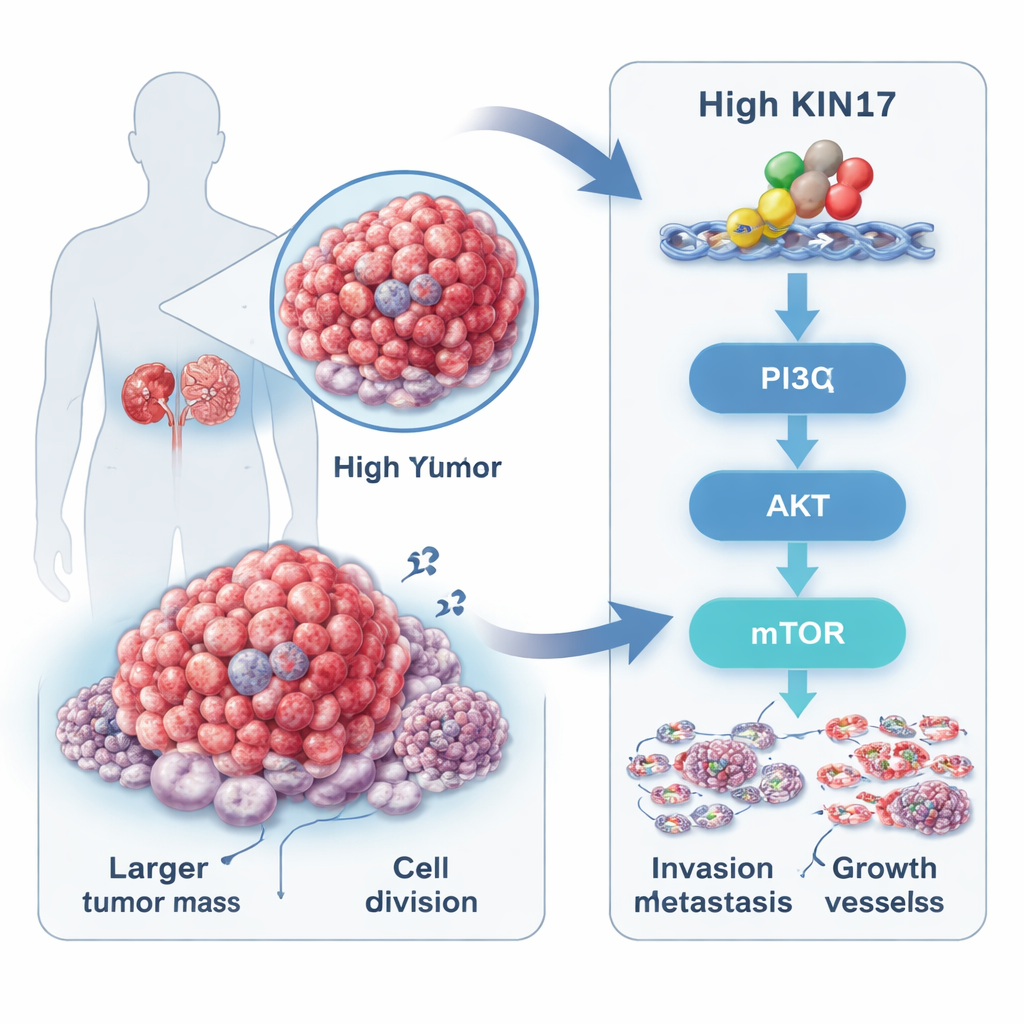
محفز خفي داخل أورام الكِلية
تبدأ سرطانة الخلايا الكلوية، الأكثر شيوعًا بين أنواع سرطان الكِلية، غالبًا بدون أعراض وغالبًا ما يُكتشف في مراحل متأخرة. ركز الباحثون على بروتين يدعى KIN17، المعروف منذ زمن بدوره في حماية ونسخ الحمض النووي، لكنه ارتبط فقط مؤخرًا بعدة أنواع سرطانية أخرى. من خلال تحليل قواعد بيانات سرطانية عامة وعينات أورام من 88 مريضًا، وجدوا أن مستويات KIN17 كانت أعلى بكثير في أورام الكِلية مقارنة بالنسيج المحيط غير السرطاني. المرضى الذين حملت أورامهم مستويات أعلى من KIN17 كانوا يميلون إلى وجود سرطانات أكبر، ودرجة مرض أعلى، ومرحلة أكثر تقدمًا، وانتشار بعيد أكثر، وعاشت فترة أقصر مقارنة بمن لديهم KIN17 منخفضًا. هذا النمط أوحى بأن KIN17 ليس مجرد عنصر عابر، بل مرتبط ارتباطًا وثيقًا بمدى عدوانية الورم.
اختبار KIN17 في الخلايا السرطانية
لاكتشاف ما الذي يفعله KIN17 فعلًا داخل خلايا سرطان الكِلية، صمّم الفريق خطوط خلايا مختبرية لتقليل KIN17 أو زيادته. عندما قللوا KIN17، نمت الخلايا ببطء أكبر، شكّلت مستعمرات أقل، وكانت أقل قدرة على الحركة والغزو عبر أغشية اصطناعية. دخلت نسبة أكبر من هذه الخلايا طور الراحة في دورة الخلية وماتت بمعدلات أعلى، مظهرة مستويات أعلى من الموت الخلوي المبرمج. وحدث العكس عندما زاد إنتاج KIN17: تضاعفت الخلايا بسرعة أكبر، ونسخت حمضها النووي بسهولة أكبر، أغلقت الفجوات الشبيهة بالخدش في طبقات الخلايا بسرعة أكبر، وغزت بشكل أكثر عدوانية. أظهرت هذه التجارب أن KIN17 يعمل كدواسة تسريع لنمو وانتشار خلايا سرطان الكِلية.
مسار نمو مُكتشف في عين الحدث
سأل الباحثون بعد ذلك كيف يمارس KIN17 هذه القوة. أشار مسح نشاط الجينات وقياسات البروتين إلى شبكة معروفة للنمو والبقاء داخل الخلايا تُسمى مسار PI3K–AKT–mTOR. يُشبه هذا المسار في كثير من الأحيان محور تحكم مركزي يخبر الخلايا متى تنمو وتنقسم وتتجنب الموت. كانت خلايا سرطان الكِلية ذات مستويات KIN17 العالية تُظهر إشارات "تشغيل" أعلى — علامات كيميائية تُسمى فوسفاتات — على مكونات رئيسية في هذا المسار، رغم أن الكمية الإجمالية لهذه البروتينات لم تتغير. عندما قلل الباحثون من KIN17، هبطت هذه علامات التفعيل، وتغيرت أيضًا جزيئات مرتبطة بحركة الخلايا والغزو. في تجارب الفئران، نمت الأورام المبنية من خلايا غنية بـ KIN17 أكبر وأسرع، وأظهر صبغ النسيج أن نفس مسار النمو كان مفعلًا بقوة في تلك الأورام.
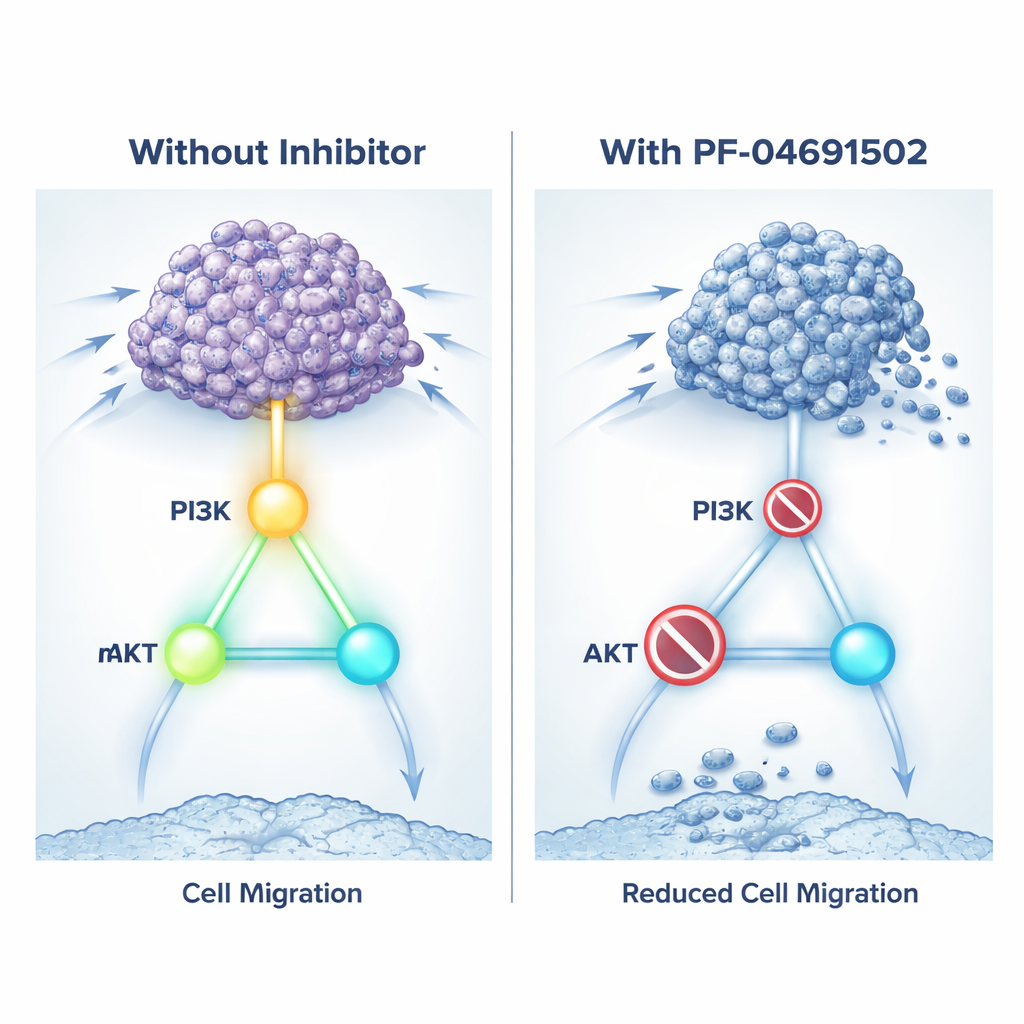
خفض الإشارة بعقار مزدوج الاستهداف
نظرًا لأن حجب KIN17 مباشرة غير ممكن بعد بالأدوية المتوفرة، اختبر الفريق استراتيجية مختلفة: إغلاق مسار النمو الذي يبدو أنه يسيطر عليه. استخدموا PF‑04691502، دواء تجريبي يحجب كلًا من PI3K و mTOR، وهما مفتاحان في المسار. في الأطباق المخبرية، أدى علاج خلايا سرطان الكِلية ذات KIN17 العالي بهذا المثبط إلى إبطاء نموها، وتقليل قدرتها على الهجرة وتشكيل المستعمرات، ودفع المزيد من الخلايا إلى الموت. كما قلل الدواء علامات التفعيل على PI3K وAKT وmTOR وخفض مستويات بروتينات مرتبطة بالغزو. في الفئران الحاملة لأورام كلوية، قلّصت جرعات يومية من PF‑04691502 الأورام التي كانت تفرط في إنتاج KIN17 وخفّضت علامات الانقسام الخلوي بينما زدّت إشارات الموت الخلوي. باختصار، تمكن الدواء من تهدئة التأثيرات الضارة لـ KIN17 عبر إسكات مسار النمو الذي يفضله.
ما الذي قد يعنيه هذا للمرضى
بالنسبة للأشخاص المصابين بسرطان الكِلية، تقترح هذه النتائج فكرتين واعدتين. أولًا، قد يساعد قياس KIN17 في عينات الأورام الأطباء على تقدير مدى عدوانية السرطان واحتمال انتشاره. ثانيًا، قد تكون الأورام التي تعتمد بشكل كبير على KIN17 عرضة بشكل خاص للأدوية التي تستهدف مسار PI3K–AKT–mTOR، مثل PF‑04691502 أو مثبطات مزدوجة مماثلة تجري بالفعل في تجارب سريرية لأنواع سرطانية أخرى. وبينما يبقى عمل كبير قبل أن يصل أي علاج جديد إلى العيادة، ترسم هذه الدراسة سلسلة واضحة من الأحداث — من KIN17، عبر مسار نمو رئيسي، إلى التوسع غير المنضبط للورم — وتظهر أن قطع هذه السلسلة يمكن أن يبطئ سرطان الكِلية في المختبر وفي الحيوانات.
الاستشهاد: Wen, Y., Lyu, L., Zhang, H. et al. KIN17 facilitates the initiation and progression of renal tumor progression through the PI3K-AKT-mTOR pathway. Sci Rep 16, 5721 (2026). https://doi.org/10.1038/s41598-026-35851-5
الكلمات المفتاحية: سرطانة الخلايا الكلوية, KIN17, PI3K AKT mTOR, العلاج المستهدف, PF-04691502