Clear Sky Science · ar
إطار تكاملي على مستوى الخلية الواحدة وتعلم الآلة يكشف عن أنواع ورّاقية متنبئة ويبني توقيع مخاطرة متعلق بالورّاق في سرطان غدي رئوي
لماذا تهم الخلايا «المساعدة» حول أورام الرئة
يعد السرطان الغدي الرئوي واحدًا من أكثر أنواع سرطان الرئة شيوعًا وما يسببًا للوفاة، ومع ذلك يمكن أن يختلف مسار المرض واستجابة العلاج كثيرًا بين مرضى لديهم أورام تبدو متشابهة. يتجاوز هذا البحث خلايا السرطان ذاتها للتركيز على الخلايا «المساعدة» المحيطة المسماة الورّاق، التي تساهم في بناء وإعادة تشكيل النسيج. من خلال دراسة هذه الخلايا خليةً فخلية ثم استخدام نماذج حاسوبية متقدمة، يُظهر الباحثون أن الورّاق تأتي بأنماط مميزة يمكنها التنبؤ بمآل المرضى وكيف قد تستجيب أورامهم للعلاجات المناعية الحديثة.
نظرة فاحصة على حي الورم
باستخدام تقنيات متقدمة لتسلسل الرنا أحادي الخلية، حلل الفريق أكثر من 140,000 خلية فردية مأخوذة من عينات سرطان غدي رئوي غير معالجة. تقرأ هذه التقنية أي الجينات نشطة في كل خلية، مما مكن المؤلفين من تصنيف الورم إلى السكان الرئيسيين: الخلايا المناعية، وخلايا السرطان، وخلايا الأوعية الدموية، والورّاق. وجدوا أن الأورام تختلف تمامًا في مقدار كل نوع خلوي لديها. بعض الأورام غنية بالخلايا المناعية، بينما يهيمن على أخرى الورّاق والنسيج البنيوي. أظهرت التحليلات اللاحقة أن كل نوع خلوي يؤدي أدوارًا متخصصة، بدءًا من تنسيق الهجمات المناعية إلى بناء السقالة البنيوية للورم.
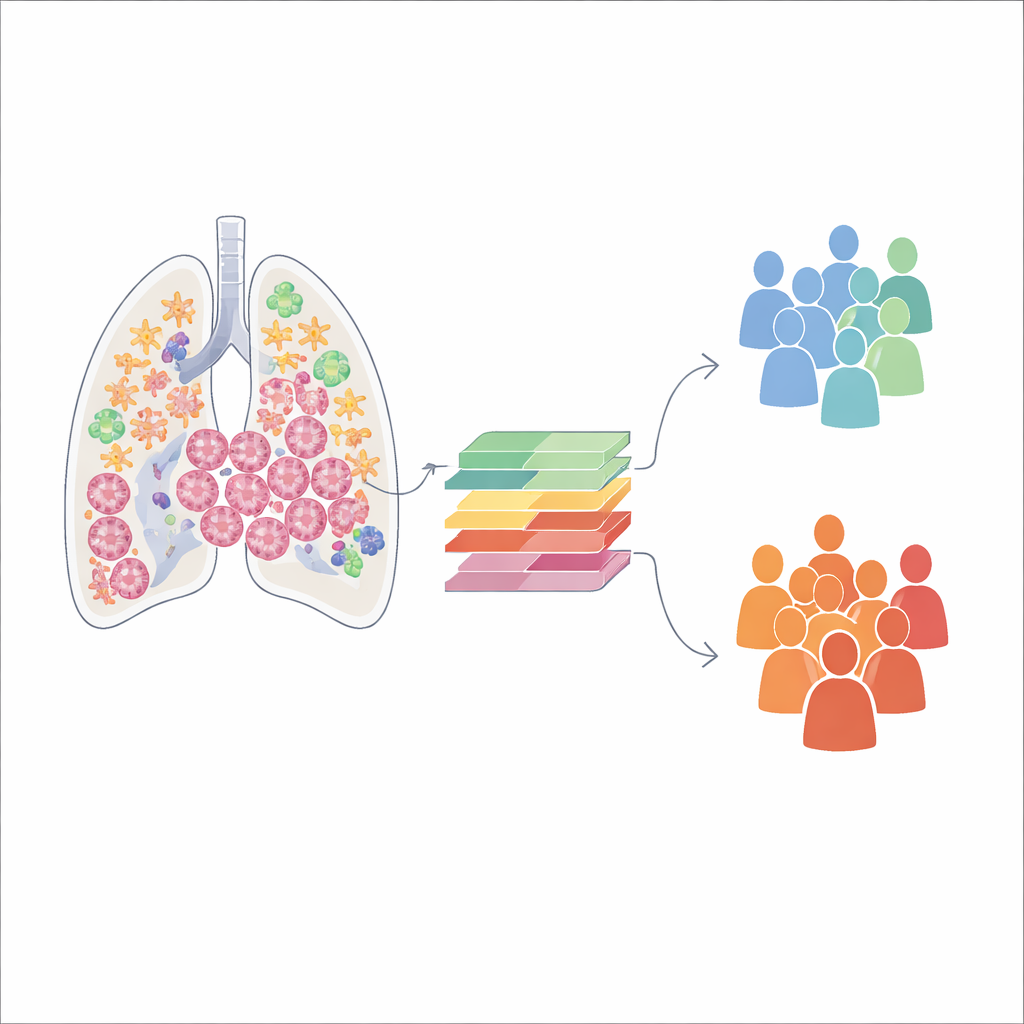
ليست كل الورّاق متشابهة
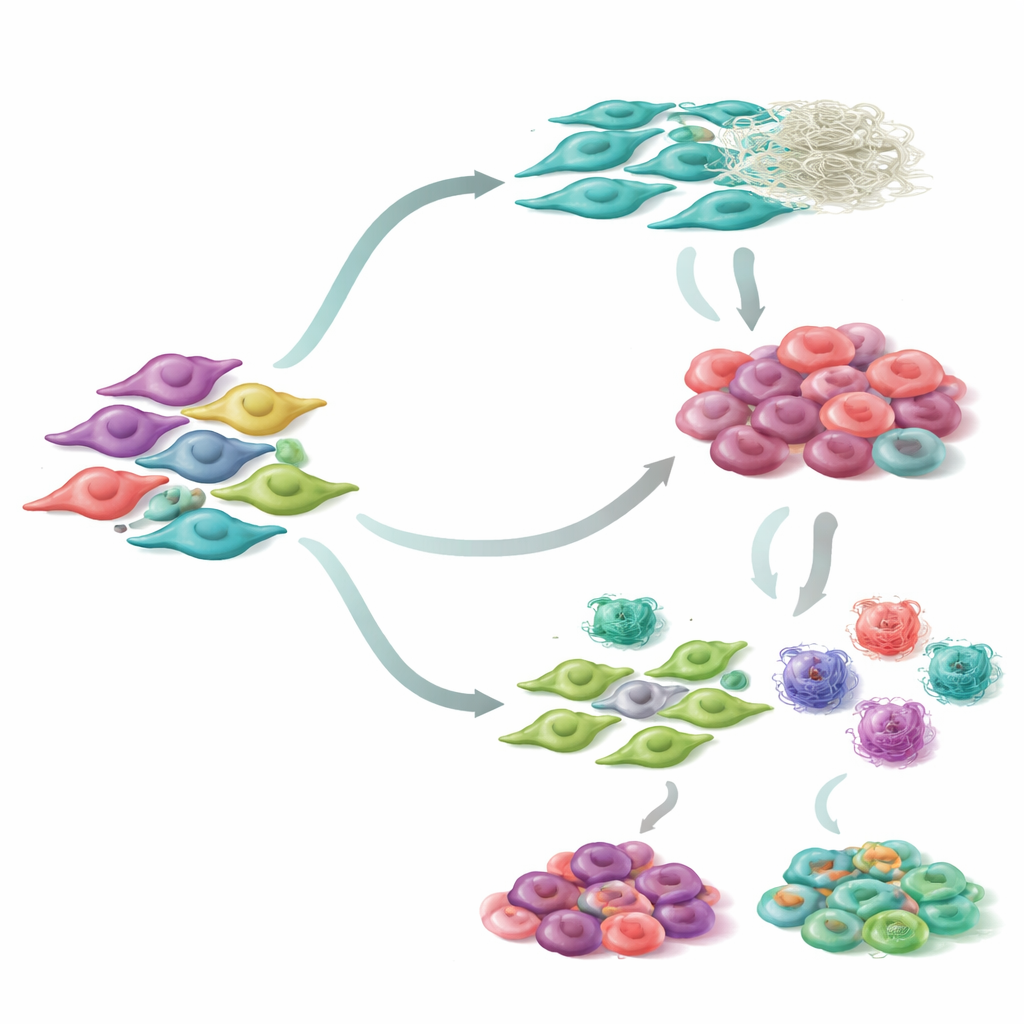
عندما ركز الباحثون تحديدًا على الورّاق، كشفوا عن سبع مجموعات فرعية مميزة من الورّاق داخل الأورام الرئوية. وعن طريق إعادة بناء كيفية تغير هذه الخلايا مع الزمن، لاحظوا مسارين رئيسيين للتطور. على أحد المسارين، تكتسب الورّاق تدريجيًا صفات خلايا قابضة ومُقسِّبة لتصلب النسيج تعيد تشكيل محيط الورم. وعلى المسار الآخر، تصبح الورّاق أكثر انخراطًا في التفاعل مع الجهاز المناعي، إما بجذب الخلايا المناعية أو كبحها. أظهرت كل مجموعة فرعية أنماطًا فريدة من نشاط الجينات وارتباطًا بمهام بيولوجية مختلفة مثل الانقباض الشبيه بعضلات، والحركة، أو تنظيم المناعة. والأهم، أن المرضى الذين كانت أورامهم غنية ببعض أنواع الورّاق كانوا يميلون إلى البقاء على قيد الحياة لفترات أطول، ما يعني أن تشكيلة حالات الورّاق ليست مجرد ظاهرة فضولية بل مرتبطة بنتائج سريرية حقيقية.
بناء درجة مخاطرة من إشارات الورّاق
لتحويل هذه الرؤى البيولوجية إلى أداة مفيدة في العيادة، جمع الفريق جينات وسمية للورّاق من بيانات أحادية الخلية مع بيانات مجمعة من مئات المرضى في قواعد بيانات عامة كبيرة. ثم طبقوا مجموعة مكونة من 10 طرق تعلم آلي مختلفة، واختبروا 101 تركيبة نموذجية، لاكتشاف أي مزيج من الجينات المتعلقة بالورّاق يتنبأ بشكل أفضل بالبقاء على قيد الحياة. النموذج الفائز، المسمى التوقيع المتعلق بالورّاق أو FRS، يستخدم 29 جينًا ليمنح كل مريض درجة مخاطرة. عبر مجموعة البيانات الأساسية وست مجموعات مرضى مستقلة، كان الأشخاص ذوو درجات FRS العالية يعانون باستمرار من بقاء أقل من ذوي الدرجات المنخفضة. كما بقي FRS مؤشرًا قويًا حتى عند أخذ العمر والجنس ومرحلة الورم في الاعتبار، وحسّن التنبؤ عند دمجه مع نظام الترقيم TNM القياسي.
دلالات الهروب المناعي واستجابة العلاج
نظرًا لأن العديد من المرضى يتلقون الآن العلاج المناعي، تساءل المؤلفون إن كانت الدرجة المبنية على الورّاق تلتقط ميزات بيئة الورم المناعية. وجدوا أن الأورام ذات درجات FRS المنخفضة تميزت بتغلغل أغنى للخلايا المناعية المقاتلة للسرطان مثل خلايا T CD8 والخلايا القاتلة الطبيعية، وكذلك بارتفاع تعبير الجينات المشاركة في عرض شظايا الورم للجهاز المناعي. أما الأورام ذات FRS المرتفع فبدت على النقيض أقل احتواءً للخلايا المناعية المفيدة، ومحتوية لنسبة أعلى من خلايا الورم، ومزيدًا من عدم الاستقرار الجيني وعلامات استبعاد مناعي، أي أن الخلايا المناعية تُبقى على مسافة. وأشارت مقاييس تحاكي الاستجابة المحتملة لأدوية نقاط التفتيش المناعية إلى أن المرضى ذوي درجات FRS المنخفضة قد يستفيدون أكثر من هذه العلاجات، بينما قد يكون المرضى ذوو FRS المرتفع أكثر مقاومة.
تسليط الضوء على جين هدف واعد
من بين الجينات التي شكلت FRS، أبرز الفريق جينًا اسمه TIMP1 كمؤشر قوي على سوء المآل. وُجد TIMP1 بمستويات مرتفعة في العديد من أنواع السرطان وكان مرتفعًا بصورة خاصة في نسيج السرطان الغدي الرئوي مقارنة بالأنسجة الرئوية السليمة المجاورة. في تجارب مخبرية، أدى خفض مستويات TIMP1 في خطوط خلايا سرطان الرئة إلى تقليل قدرة الخلايا على الغازي عبر مصفوفة وتشكيل مستعمرات جديدة، مما يوحي بأن TIMP1 يساهم في دفع نمو الورم وانتشاره. تشير هذه النتائج إلى TIMP1 كهدف مرشح لأدوية مستقبلية تهدف إلى إضعاف الآليات البنيوية والمشكِّلة للمناعة في الورم.
ماذا يعني هذا للمرضى
تُظهر هذه الدراسة أن الخلايا المساندة حول ورم الرئة، وخصوصًا الورّاق، تحمل معلومات قيّمة حول سلوك المرض وكيف قد يستجيب للعلاج. من خلال دمج قياسات أحادية الخلية مع تعلم الآلة، أنشأ المؤلفون درجة مخاطرة مبنية على الورّاق يمكنها تصنيف المرضى إلى مجموعات أعلى وأدنى خطر وتقديم دلائل حول أي الأورام أكثر احتمالًا لمقاومة العلاج المناعي. ومع حاجتها لمزيد من الاختبارات قبل أن تستخدم في الرعاية اليومية، تؤكد الدراسة أن علاج سرطان الرئة بفعالية سيتطلب ليس فقط مهاجمة خلايا السرطان نفسها، بل أيضًا كبح الورّاق المحيطة التي تساعد الورم على النمو والاختفاء من أعين الجهاز المناعي.
الاستشهاد: Cheng, S., Zhang, H., Mu, Q. et al. Integrative single-cell and machine learning framework reveals prognostic fibroblast subtypes and constructs a fibroblast-related risk signature in lung adenocarcinoma. Sci Rep 16, 7965 (2026). https://doi.org/10.1038/s41598-026-35830-w
الكلمات المفتاحية: سرطان غدي رئوي, الورّاق المرتبط بالسرطان, تسلسل الرنا أحادي الخلية, المحيط الورمي, استجابة المناعة العلاجية