Clear Sky Science · ar
نسخة خفيفة من SwiM-UNet مع محوّل متعدد الأبعاد لتقسيم صور طبية فعّال على الجهاز
فحوص أذكى بجانب السرير
يمكن لفحوص الدماغ أن تكشف عن أورام مهددة للحياة، لكن تحويل الصور الأولية إلى حدود واضحة يستطيع الأطباء الاعتماد عليها لا يزال بطيئاً ويتطلب حواسيب قوية. تقدّم هذه الدراسة SwiM‑UNet، خوارزمية جديدة قادرة على تقسيم أورام الدماغ من صور الرنين المغناطيسي ثلاثية الأبعاد بدقة متقدمة، مع تشغيل فعّال على أجهزة محلية، ما يقرب تحليل الصور الدقيق إلى جانب سرير المريض أو حتى إلى عيادات متنقلة. 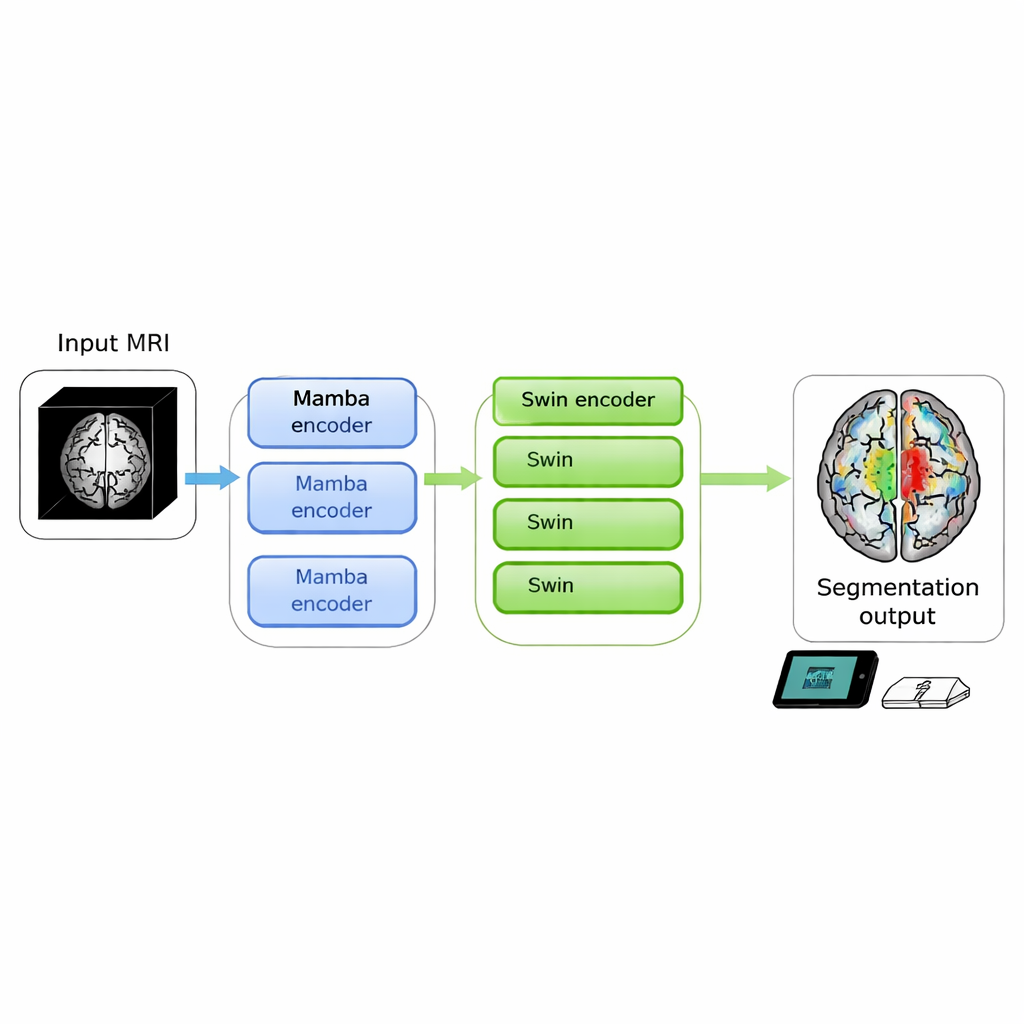
لماذا تهم الحدود الدقيقة للأورام
تعتمد الطب الحديث بدرجة كبيرة على التصوير لتخطيط الجراحة والعلاج الإشعاعي والأدوية. بالنسبة لأورام الدماغ، يحتاج الأطباء ليس فقط إلى رؤية وجود الورم، بل إلى تحديد مكان بداية ونهاية أجزائه بدقة. تُسمى هذه المهمة التقسيم، وعادة ما يقوم بها المتخصصون أو يقومون بصقلها شريحة بشريحة — وهي عملية تستغرق وقتاً قد تؤخر اتخاذ القرارات وتختلف من خبير لآخر. حسّنت أدوات التقسيم الآلية القائمة على التعلم العميق هذا الوضع، لكن الأدوات الأكثر دقة غالباً ما تتطلب معالجات رسومية كبيرة، مما يصعّب استخدامها مباشرة في العيادة، لا سيما على الأجهزة الأصغر أو المحمولة.
فكرتان قويتان لا تتناسبان بسهولة مع الأجهزة الصغيرة
تنبع الاختراقات الحديثة في رؤية الحاسوب بصورة رئيسية من عائلتين من النماذج. أنظمة قائمة على المحولات، مثل Swin Transformer، ممتازة في التقاط الأنماط الشاملة عبر مسح ثلاثي الأبعاد كامل وقد دفعت أدوات تقسيم أورام الدماغ المتفوقة. مع ذلك، العملية الأساسية لها، المسماة الانتباه الذاتي، تصبح مكلفة للغاية مع تزايد حجم الصورة، مما يقيّد استخدامها في الوقت الحقيقي أو على أجهزة مضغوطة. العائلة الأحدث، المعروفة باسم Mamba والمبنية على نماذج الحالة الزمنية، تقدم حلاً ذكيّاً: فهي تعالج المتتاليات بزمن خطي فعّال، ما يقلّل عدد العمليات الحسابية المطلوبة. أظهرت التجارب الأولية في التصوير الطبي أن نماذج نمط Mamba سريعة وموفّرة لكن عادة ما تتخلّف عن المحولات من حيث جودة التقسيم، خاصة مع الأشكال المعقدة للأورام.
مزج السرعة والدقة في تصميم واحد
سعى الباحثون لدمج نقاط القوة من العالمين في نموذج ثلاثي الأبعاد واحد. يحتفظ SwiM‑UNet بالبنية المألوفة على شكل حرف U المستخدمة على نطاق واسع في التصوير الطبي، مع مُشفّر يضغط المعلومات ومُفكّك يعيد بناء التقسيمات التفصيلية. في المراحل المبكرة، حيث تظل الصورة كبيرة وعالية الدقّة، يستخدمون بلوكات Mamba الفعّالة للحفاظ على قابلية العمليات الحسابية. أعمق في الشبكة، بعد أن تُخفض العينات، يتحولون إلى بلوكات Swin Transformer المبسطة التي تستطيع الآن نمذجة العلاقات بعيدة المدى دون إرهاق العتاد. جسر مخصّص يسمى MS‑adapter يربط بين هذين النمطين. ينظر هذا الجسر إلى الميزات عبر العرض والارتفاع والعمق للحجم بشكل منفصل، وكذلك عبر القنوات، ثم يتعلّم عبر وحدات بوّابة صغيرة مقدار تأثير كل منظور على التمثيل النهائي.
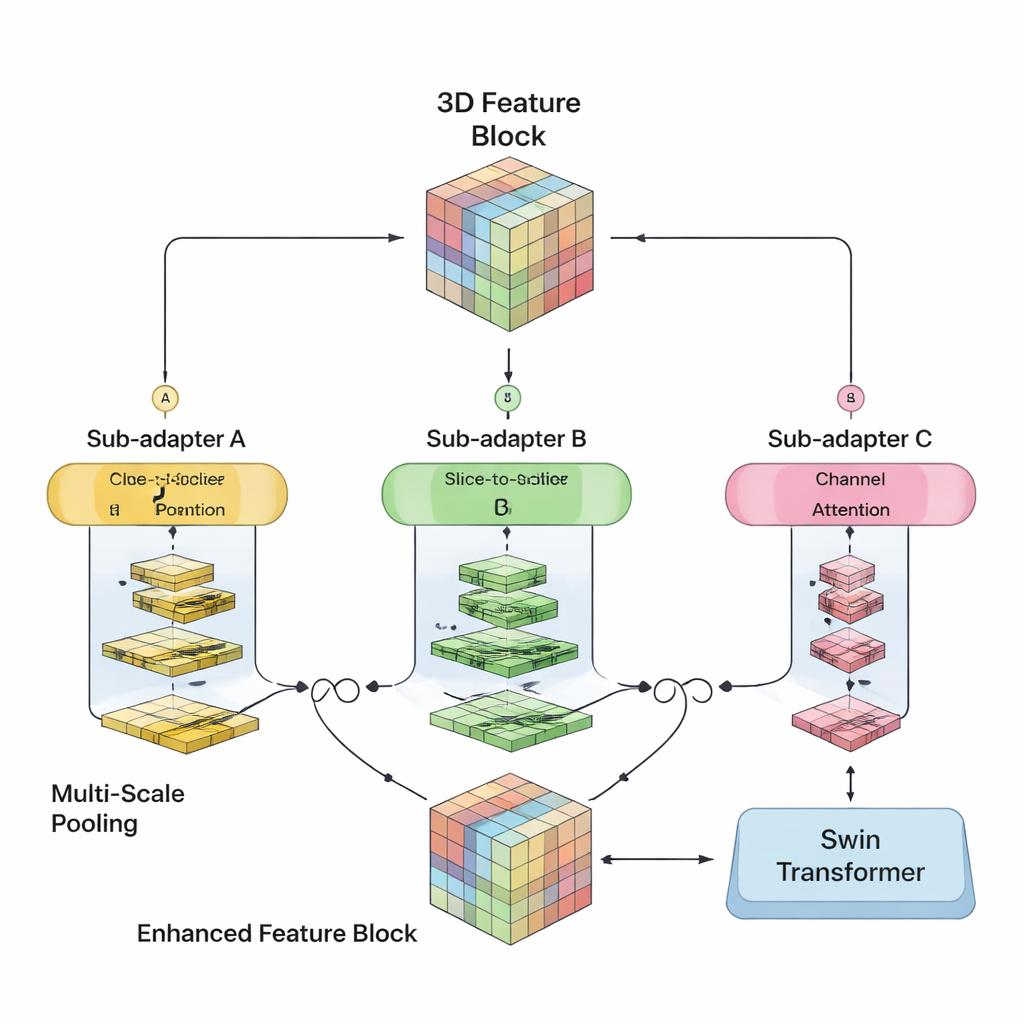
تحصيل المزيد بأقل عمليات حسابية
بعيداً عن هذا التصميم الهجين، يقلّص الفريق العمليات الحسابية الزائدة باستخدام طبقات متصلة بالكامل منخفضة الرتبة ومفكّك يقلص عمداً عدد القنوات التي يحتاج للتعامل معها. اختبروا عدة متغيرات بمزيجيات مختلفة من طبقات Mamba وSwin ووجدوا أن استخدام Mamba في المراحل الثلاث الأولى من المُشفّر وSwin فقط في أعمق مرحلة أعطى أفضل توازن بين السرعة والدقة. على مجموعتين عامتين كبيرتين لأورام الدماغ من تحديات BraTS 2023 و2024، حقق SwiM‑UNet دقة أعلى وحدوداً أكثر تحديداً من نماذج قائمة على المحولات فقط أو Mamba فقط أو النماذج الهجينة السابقة، بينما استخدم عدد عائم من العمليات الحسابية أقل بكثير وقلّل زمن الاستدلال إلى نحو 45 ملّي ثانية لكل رقعة مسح على بطاقة رسومية حديثة.
جاهز للأجهزة الواقعية
للتحقق مما إذا كانت هذه المكاسب مهمة خارج المختبر، قارن المؤلفون متطلبات النموذج الحاسوبية مع قدرات أنظمة الحافة السريرية النموذجية — وحدات التحكم المحمولة بالرنين المغناطيسي، حواسيب نقاط الرعاية، ومحطات عمل غرف العمليات. تشير تحليلاتهم إلى أن SwiM‑UNet، على عكس نماذج المحولات الأثقل، يتوافق بسهولة مع حدود الطاقة والذاكرة والسرعة لهذه الأجهزة، وغالباً ما يلبّي متطلبات الوقت الحقيقي. كما أدّى بشكل قوي على مجموعة بيانات مقطعية بطنية منفصلة، ما يدل على أن المنهج يمكن أن يعمم خارج أورام الدماغ وحتى خارج الرنين المغناطيسي.
ماذا يعني هذا للمرضى والأطباء
عملياً، يبيّن SwiM‑UNet أنه من الممكن الاقتراب من دقة أكثر نماذج التقسيم تطوراً مع الحفاظ على خفة الحوسبة بما يكفي للاستخدام على الجهاز. قد يمكّن ذلك من الحصول على حدود أورام أسرع وأكثر اتساقاً في غرف الطوارئ والمستشفيات الريفية أو وحدات التصوير المتنقلة دون إرسال الصور الحساسة إلى خوادم بعيدة. وبينما هناك حاجة لمزيد من العمل لتكييف الطريقة مع أجهزة مسح وحالات مختلفة، يشير هذا التصميم الهجين إلى مستقبل يمكن فيه تشغيل تحليل الصور عالي الجودة حيثما يتواجد المريض، وليس فقط في مراكز البيانات.
الاستشهاد: Noh, Y., Lee, S., Jin, S. et al. Lightweight SwiM-UNet with multi-dimensional adaptor for efficient on-device medical image segmentation. Sci Rep 16, 5807 (2026). https://doi.org/10.1038/s41598-026-35771-4
الكلمات المفتاحية: تقسيم أورام الدماغ, الذكاء الاصطناعي في التصوير الطبي, الشبكات العصبية الهجينة, الاستدلال على الجهاز, تحليل الرنين المغناطيسي ثلاثي الأبعاد