Clear Sky Science · ar
الأشكال الفسيولوجية ذات الصلة من متتبِعات البيروفوسفات المشعة للتكنيتيوم والرينيوم وأساس حساسيتها لأميلويد الترانستيرتين
لماذا تهمنا قصة تصوير القلب هذه
يتكوّن لدى كثير من الأشخاص ترسّبات صامتة لبروتينات مطوية بشكل غير طبيعي، تُعرف بالأميلويدات، في القلب مع التقدم في العمر. بعض هذه الترسبات، لاسيما تلك المصنوعة من بروتين الدم المسمى الترانستيرتين، يمكن أن تجعل جدار القلب أكثر صلابة وتؤدي إلى أمراض خطيرة. يعتمد الأطباء بشكل متزايد على متتبِع إشعاعي يُعرف ببَيرُوفوسفات التكنيتيوم‑99m (99mTc‑PYP) لرؤية هذه الترسبات في الصور. ومع ذلك، من المستغرب أن الشكل الدقيق لهذا المتتبِع في الجسم ولماذا يبدو أنه «يفضّل» أنواعًا معينة من الأميلويد لم يكن واضحًا إلى الآن. يجمع هذا البحث بين النظرية والتجربة لكشف الشكل الحقيقي للمتتبِع في ظروف شبيهة بالحياة وكيف قد يتيح هذا الشكل استهداف خيوط الترانستيرتين الضارة.
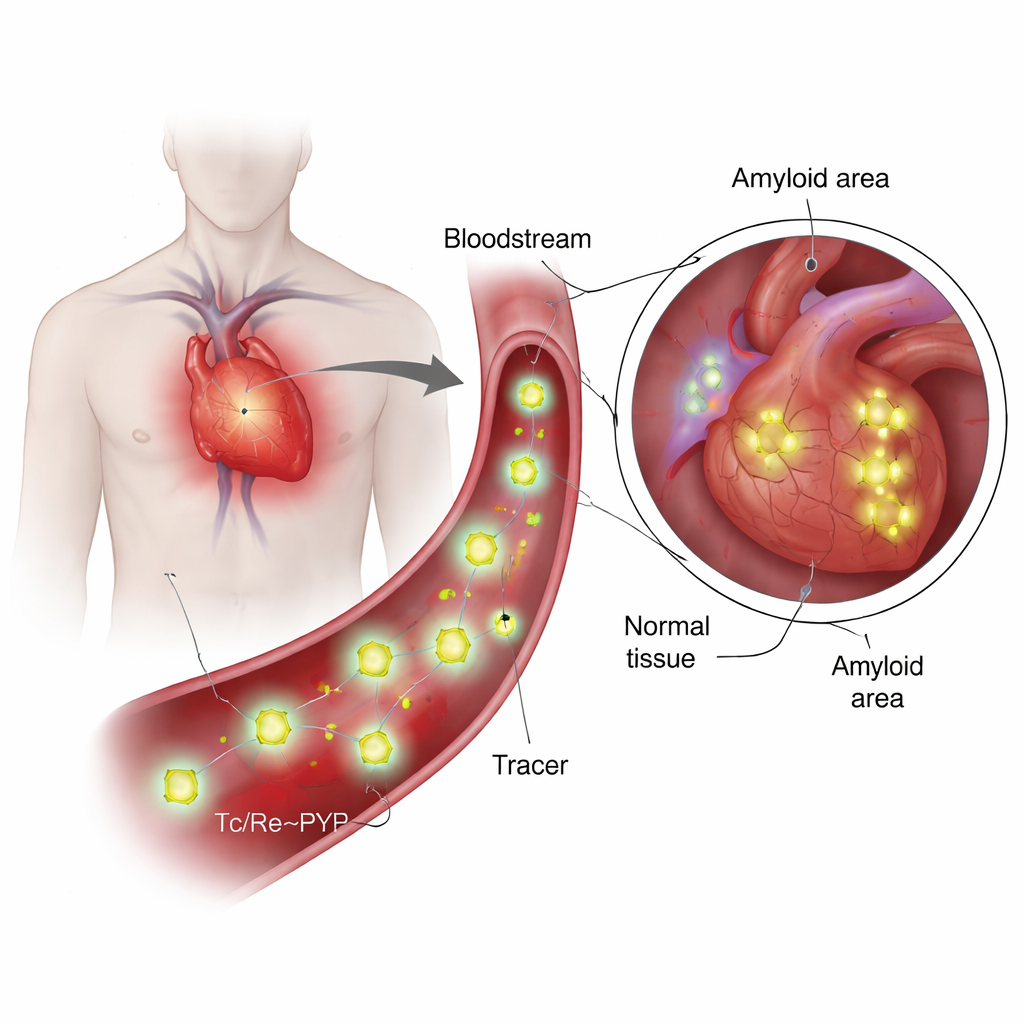
ما هذه المتتبِعات ولماذا هي مميزة؟
استُخدِم 99mTc‑PYP لعقود لتصوير العظام، لأنه يميل إلى التراكم حيث تكون عمليات تبادل الكالسيوم والمعادن عالية. ومؤخرًا اكتشف الأطباء أنه يمكنه أيضًا التمييز بين نوعين رئيسيين من أميلويد القلب: واحد مكوّن من سلاسل خفيفة من الأجسام المضادة (AL) وآخر من الترانستيرتين (ATTR). في حالات ATTR، يضيء القلب غالبًا بشدة في فحوص PYP، بينما تميل حالات AL إلى البقاء باهتة، حتى عندما يبدو تراكم الكالسيوم مشابهًا. أثار هذا التباين سؤالًا محوريًا: هل يلتصق المتتبِع بالكالسيوم فقط أم يتفاعل مباشرة مع بروتين الأميلويد نفسه؟ يتطلب الإجابة عن ذلك معرفة التركيب الكيميائي الحقيقي للمتتبِع في ظروف شبيهة بالدم، وهو أمر لم تتعدَّ الدراسات السابقة تقديمه إلا بمخططات عامة.
استخدام بديل أكثر أمانًا لرؤية غير المرئي
بما أن التكنيتيوم عنصر مشع ويتواجد بكميات ضئيلة فقط في التحضيرات الطبية، فمن الصعب دراسته مباشرة بالعديد من تقنيات المختبر. لذلك استخدم المؤلفون الرينيوم، وهو عنصر قريب جدًا في الحجم وتفضيلات الروابط ولكنه أسهل كيميائيًا، كبديل. حضّروا مخاليط رينيوم‑بيروفوسفات وفق شروط تحاكي مجموعات PYP السريرية ثم فحصوها بطيف من الأدوات: حسابات كيمياء كمية متقدمة، امتصاص الضوء فوق البنفسجي‑المرئي، طيفيات اهتزازية مختلفة (الأشعة تحت الحمراء والرaman)، الرنين المغناطيسي النووي، مطيافية الكتلة، وطيف Mössbauer للقصدير. أجرت هذه الأساليب معًا اختبارًا للعديد من التركيبات المحتملة وضاقت النتائج إلى أي الأنواع يحتمل أن توجد عند درجة الحموضة المحايدة، مثل تلك في الدم.
شكل جزيئي قابل للانثناء لكن يمكن التعرف عليه
تشير الأدلة المجمعة إلى بنية «نواة» شائعة: مركب ثماني السطوح تقريبًا حيث يكون ذرة التكنيتيوم أو الرينيوم في حالة أكسدة +4 مرتبطة بمجموعتين من البيروفوسفات وجزيئتا ماء. ببساطة، يجلس المعدن في مركز قفص شبه ثماني السطوح مكوّن من ذرات أكسجين، مع عمل البيروفوسفات كمرساة متعددة الأسنان وتملأ جزيئتا الماء المواقع المتبقية. هذه الوحدة الأساسية ذات جزيئين ماء وبي‑بيروفوسفات ليست صلبة. إذ يمكن لأذرع البيروفوسفات أن تلتف وتكوّن روابط هيدروجينية داخلية مع المياه المرتبطة، فيستكشف الجزيء العديد من الأشكال الطفيفة المختلفة في المحلول. تشير الحسابات والطرائق الطيفية إلى أن هذه الاختلافات تحرك بصماته الامتصاصية والاهتزازية، ما يفسّر لماذا تكون النطاقات التجريبية عريضة ولماذا كافحت الدراسات السابقة لتحديد بنية واحدة واضحة.
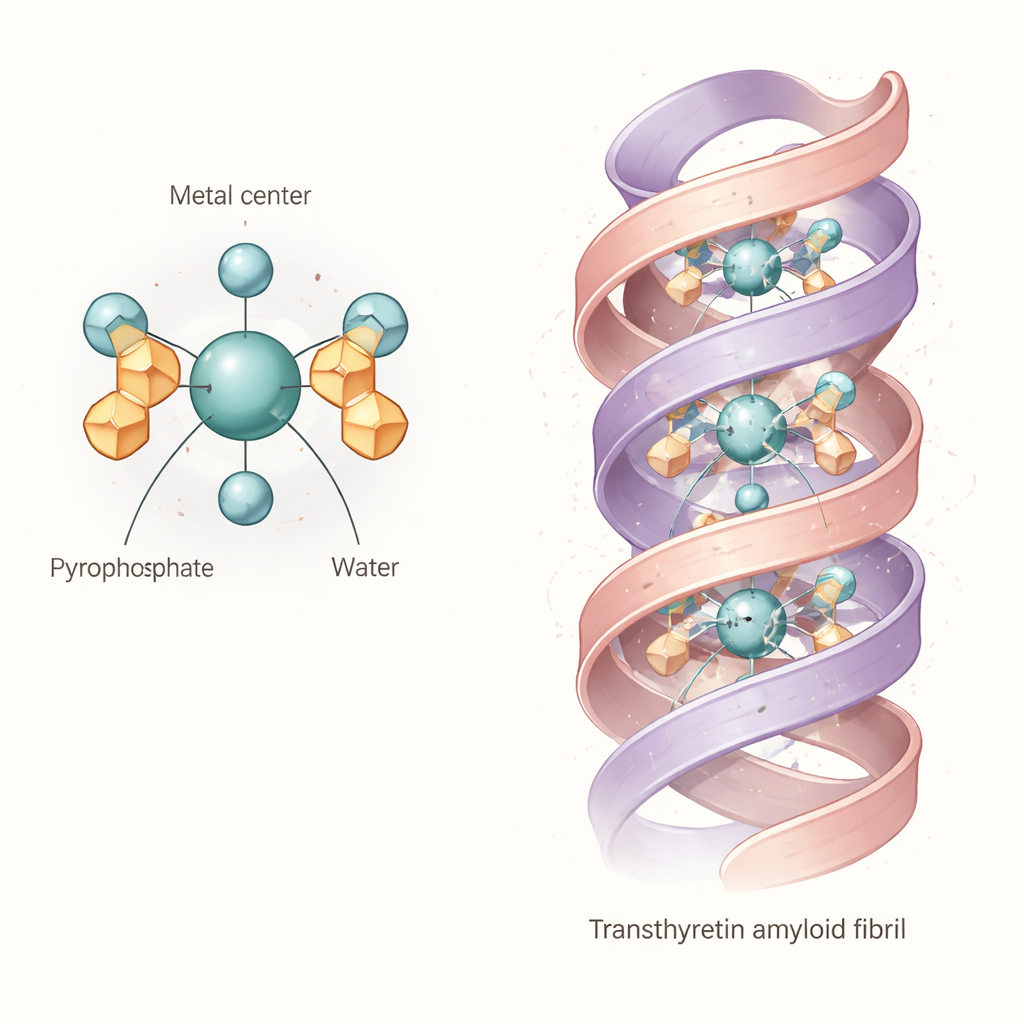
ماذا يعني هذا للارتباط بأميلويد القلب
سأل المؤلفون بعد ذلك ما إذا كان هذا المركب القابل للانثناء يمكنه منطقياً أن يستقر مباشرة داخل خيوط أميلويد الترانستيرتين. باستخدام بنية مفصّلة مجمدة بالتصوير المجهري الإلكتروني لخيط ترانستيرتين بشري، أجروا عمليات بحث للتثبيت الحاسوبي مع المركب النموذجي للتكنيتيوم‑بيروفوسفات. تُظهر النتائج أن وحدة «ثنائي الماء–ثنائي البيروفوسفات» يمكن أن تدخل في قناة مركزية تمتد على طول الخيط، مكوّنة عدة روابط هيدروجينية وجسور ملحية مع سلاسل جانبية مشحونة تبطّن التجويف. وهذا يوحي بأنه، على الأقل لشكلٍ ما من خيوط الترانستيرتين، المتتبِع لا يكتفي بوضع وسم على ترسبات معدنية مجاورة؛ بل قد يكون محتضناً مباشرةً بواسطة السقالة البروتينية نفسها. المرونة الهيكلية في المتتبِع على الأرجح تساعده على التكيّف مع جيوب وأنماط شحنة مختلفة في خيوط المرض الحقيقية.
الآثار على التشخيص والمتتبّعات المستقبلية
الخلاصة للقارئ العام هي أن فحص القلب الشائع PYP يستند إلى متتبِع أكثر دقة ووعياً بالبروتين مما كان مفهومًا سابقًا. في الظروف الفسيولوجية، يُفضَّل تصوّره كوحدة معدنية‑بيروفوسفات صغيرة حاملة للماء يمكنها الانثناء وتشكيل نقاط اتصال متعددة مع قنوات أميلويد الترانستيرتين. يساعد هذا الفهم في تفسير سبب إظهار المتتبِع إشارات قوية في بعض أمراض الأميلويد وليس في أخرى، وسبب أن تغييرات طفيفة في البروتين أو بيئته قد تسبب خسارة حساسية محيرة. من خلال توضيح الشكل العامل وأنماط الشحنة للمتتبِع، يضع البحث أساسًا لتصميم عوامل تصوير أو علاجية من الجيل القادم تتعرف بشكل أكثر انتقائية على الخيوط الممرضة في القلب وما وراءه.
الاستشهاد: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
الكلمات المفتاحية: أميلويد القلب, الترانستيرتين, بيروفوسفات التكنيتيوم, التصوير الجزيئي, كيمياء المتتبع الإشعاعي