Clear Sky Science · ar
أنشطة تآزرية مضادة للخلايا المستمرة، مثبطة للضخ وخافضة لتشكّل البيوفيلم لمستقلبات اللاكتوباسيلّس المهبليّة ضد E. coli المسببة لالتهاب المسالك البولية: نحو معالجة جديدة للالتهابات البولية
لماذا تهمّ الالتهابات البولية العنيدة
تُعدّ التهابات المسالك البولية من أكثر العدوى البكتيرية شيوعًا، خصوصًا لدى النساء، ويعاني كثيرون من تكرارها رغم استخدام المضادات الحيوية. تستكشف هذه الدراسة نهجًا جديدًا لتقليل الاعتماد على المضادات الحيوية في مواجهة تلك الالتهابات المتكررة والعنيدة: استثمار البكتيريا المهبلية المفيدة ونواتجها الكيميائية لمنع الإشريكية القولونية الممرِضة من الاستيطان والاختباء والعودة.
الناجون الخفيون وراء تكرار العدوى
يمكن للمضادات الحيوية التقليدية أن تقضي على معظم البكتيريا، ومع ذلك توجد فئة صغيرة تُعرف باسم «الخلايا المستمرة» (persister cells) تَنجو بدخولها حالة نمطية من الخمول والنشاط المنخفض. هذه الخلايا النائمة ليست مقاومة جينيًا، لكنها تتحمل جرعات عالية جدًا من المضادات الحيوية ويمكن أن تستيقظ لاحقًا مسببة التهابات مزمنة ومتكررة. عمل الباحثون مع سلالة شائعة ممرِضة للمسالك البولية، E. coli UTI89، وأظهروا أن مضادات قوية مثل الكوليستين والميروبينيم تحفز تكوّن هذه الخلايا المستمرة. في اختبارات مخبرية تحاكي البول، نجت كسور صغيرة من الإشريكية القولونية من تعرّض شديد للمضادات الحيوية، ما يؤكد سهولة نشوء الخلايا المستمرة وسبب فشل الأنظمة الدوائية التقليدية في تقديم راحة دائمة.
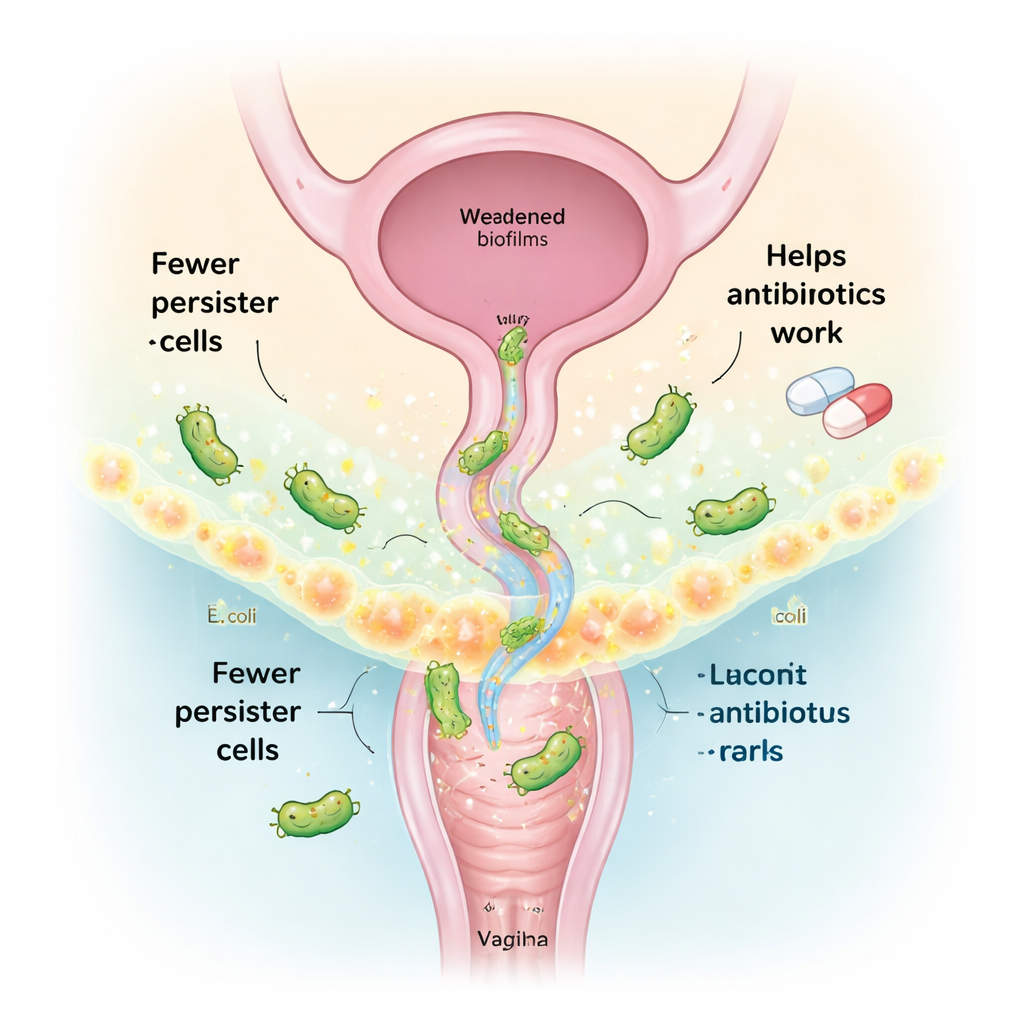
تحويل بكتيريا المهبل المفيدة إلى علاج
عادة ما يهيمن جنس اللاكتوباسيلّس على المهبل الصحي، وهو يساعد في كبح الميكروبات الضارة. بدلًا من استخدام بكتيريا حية «بروبيوتيك»، ركزت هذه الدراسة على المستنبت الخالي من الخلايا — أي مزيج الجزيئات التي تفرزها البكتيريا، والمعروفة بالمستقلبات النهائية (postbiotics). من سلالات لاكتوباسيلّس المهبلية المأخوذة من نساءٍ صحيّات، عزل الفريق وحلل هذه المركبات المفرزة. برزت مادتان أساسيتان، أنهيدريد الإيتاكونيك و(−)-تربينين-4-أول، لقدرتيهما على العمل معًا وتقليل عدد خلايا الإشريكية القولونية المستمرة بشكل حاد عند دمجهما مع المضادات الحيوية. أضيف مركب ثالث، التربتامين، الذي سبق إظهاره قادرًا على تحطيم مصفوفة البيوفيلم اللزجة التي تبنيها البكتيريا للحماية، لتعزيز الفعالية المضادة للبيوفيلم.
كيف يضعف الخليط الجديد البكتيريا الصعبة القتل
وجد العلماء أن هذه الجزيئات المشتقة من اللاكتوباسيلّس تهاجم خلايا الإشريكية القولونية المستمرة من جهات متعددة في آن واحد. أولًا، تزيد من إنتاج أنواع الأكسجين التفاعلية — أشكال أكسجين كيميائية التفاعل تُلحق ضررًا بمكونات البكتيريا — مما يجعل المضادات الحيوية أكثر فتكًا بالخلايا الخاملة. عند إضافة مضادات أكسدة انخفض هذا التأثير القاتل، مما يؤكد دور الإجهاد التأكسدي. ثانيًا، تجعل هذه المركبات الغشاء الخارجي للبكتيريا أكثر «تسرّبًا»، كما أظهرت صبغات فلورية تدخل الخلايا بصورة أسهل بعد المعالجة. ثالثًا، تثبط مضخات الطرد الخلوية، وهي آلات تصدير صغيرة تضخ المضادات الحيوية خارج الخلية عادة. مع حجب المضخات، تبقى كمية أكبر من الدواء داخل البكتيريا ويقلّ عدد الخلايا المستمرة التي تنجو. معًا أدت هذه التغيرات إلى تقليل البيوفيلومات المكوّنة مسبقًا للإشريكية القولونية بما يصل إلى عشرة أسس في الاختبارات المخبرية، دون أن تضر بالخلايا المناعية الثديية عند الجرعات المختبرة.
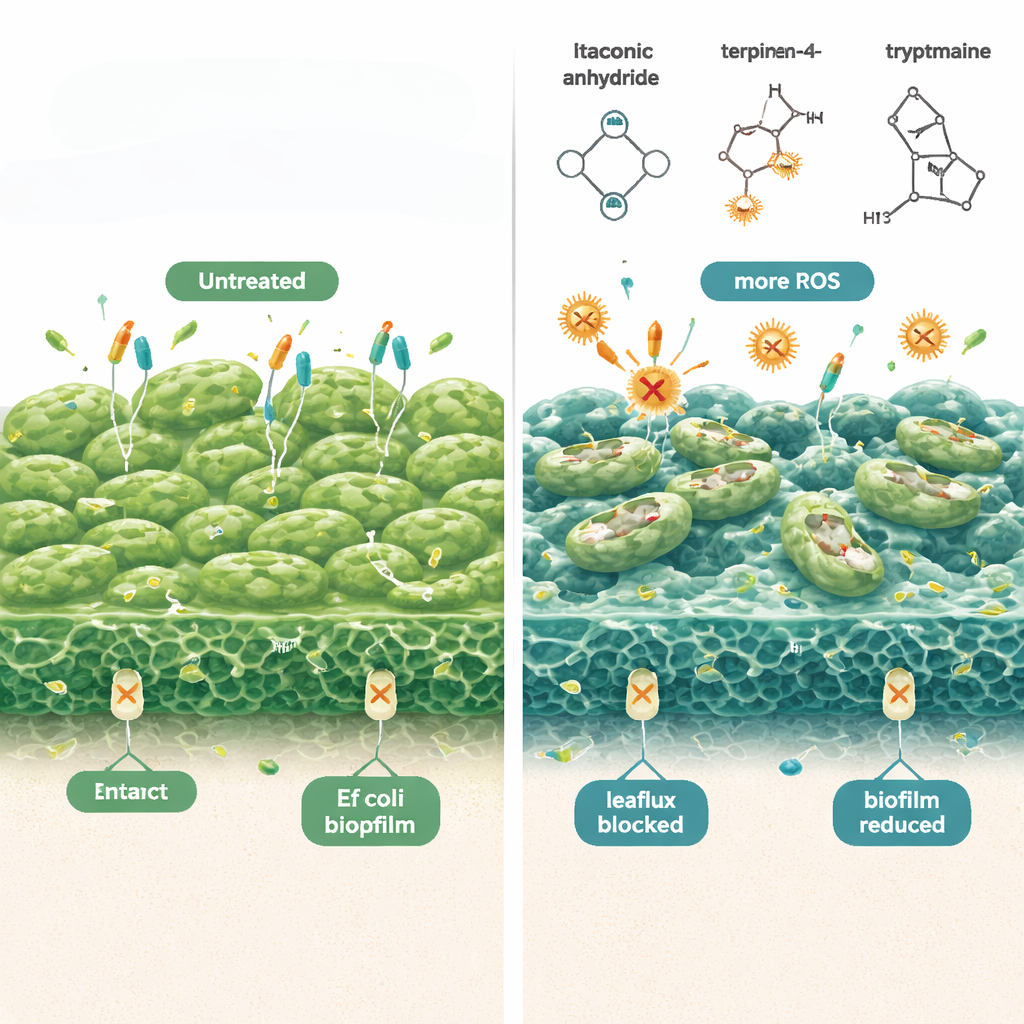
من المائدة المخبرية إلى غسول مهبلي عملي
لتحويل هذه الاكتشافات إلى منتج قابل للاستخدام اليومي، صمّم الفريق غسولًا مهبليًا مخصّصًا مستخدمًا قاعدة هلامية حساسة للحرارة تسمى بولوكسامر 407. عند درجة حرارة الغرفة يتصرف كسائل لتسهيل التطبيق، ثم يثخن بلطف عند درجة حرارة الجسم لتحسين التلامس مع جدران المهبل. يحمل الهلام مزيجًا محددًا وآمنًا من أنهيدريد الإيتاكونيك، (−)-تربينين-4-أول، والتربتامين. في أطباق المختبر عمل هذا التركيب ضمن نطاق قيم الأس الهيدروجيني المشابه لحالة المهبل، وكبح بقوة تكوّن بيوفيلم الإشريكية القولونية وخفض عدد البكتيريا الحية بنحو تسعة أسس. ظلّ مستقرًا ونشطًا بيولوجيًا لما لا يقل عن ثلاثة أشهر في التخزين البارد وأظهر أيضًا فعالية واسعة ضد بكتيريا مشكلة أخرى مثل الكلبسييلا وMRSA والزرقتية.
اختبار السلامة والحماية في الفئران
بعد ذلك قيّم الباحثون الغسول في نموذج فأري لعدوى الإشريكية القولونية المهبلية. حُقنت الفئران بإشريكية قولونية موسومة بالفلورسنت (GFP) ثم عولجت إما بالغسول الجديد المحتوي على المستقلبات، أو بغسول بروبيوتيك يحتوي على لاكتوباسيلّس حية، أو بغسول مهبلي تجاري، أو بقاعدة بلاسيبو. أظهرت الحيوانات التي تلقت الغسول المحتوي على المستقلبات المخصّص التهابًا مهبليًا أقل بكثير، وحافظت على وزنها، وسجّلت أعدادًا بكتيرية منخفضة جدًا في الإفرازات المهبلية مقارنة بالمجموعات الأخرى. والأبرز أن الفئران المعالجة لم تُظهر وجودًا قابلًا للكشف للإشريكية القولونية في البول أو المثانة أو الكليتين أو نسيج المهبل، وحافظت على وظيفة كلويّة طبيعية، ما يشير إلى أن التركيبة لم تقلل العدوى الموضعية فحسب، بل منعت أيضًا انتشارها نحو الجهاز البولي العلوي.
ماذا قد يعني هذا للأشخاص المصابين بالتهابات متكررة
تستخلص الدراسة أن غسولًا مهبليًا مبنيًا على مستقلبات دقيقة تُنتجها أنواع لاكتوباسيلّس الوقائية طبيعيًا يمكن أن يضعف الإشريكية القولونية المسببة لالتهابات المسالك البولية بطرق متعددة: تقليص مجموعات الخلايا المستمرة، تعطيل البيوفيلم، وجعل المضادات الحيوية التقليدية أكثر فعالية. وبما أن النهج يعتمد على جزيئات غير حية بدلًا من بكتيريا حية أو دورات مطولة من الأدوية الجهازية، فقد يكون أكثر أمانًا واستقرارًا وأسهل تنظيمًا. ومع أن التجارب البشرية لا تزال مطلوبة، يشير هذا الغسول القائم على المستقلبات إلى مستقبل يمكن فيه منع الالتهابات البولية المتكررة ليس فقط بمضادات أقوى، بل عبر تعزيز دفاعات الجسم الميكروبية في مصدرها.
الاستشهاد: Nair, V.G., Chellappan, D.R., Durai, R.D. et al. Synergistic antipersister, efflux inhibitory & antibiofilm activities of vaginal Lactobacillus-derived postbiotics against UPEC: toward a novel therapeutic for utis. Sci Rep 16, 5005 (2026). https://doi.org/10.1038/s41598-026-35736-7
الكلمات المفتاحية: التهاب المسالك البولية, ميكروبيوم المهبل, مستقلبات لاكتوباسيلّس, تحمل المضادات الحيوية, بلازات بكتيرية (بيوفيلم)