Clear Sky Science · ar
دراسة كمية للمركبات السامة للخلايا باستخدام موصّفات قائمة على الرسوم البيانية وتعلّم الآلة
لماذا تهمّ هذه الدراسة أدوية السرطان المستقبلية
تتفاوت أدوية السرطان التي تقتل خلايا الورم، والمعروفة بالأدوية السامة للخلايا، بين إنقاذ الأرواح والتسبّب في آثار جانبية خطيرة. ولكي نصمّم علاجات أكثر أمانًا وفعالية، يحتاج العلماء إلى طرق سريعة وموثوقة للتنبؤ بكيفية تحرك هذه الأدوية داخل الجسم — مدى امتصاصها، وسهولة عبورها لأغشية الخلايا، والأماكن التي تستقرّ فيها. توضح هذه الدراسة كيف أن الأوصاف الرياضية لجزيئات الأدوية، مرافقةً بتقنيات تعلّم الآلة الحديثة، يمكنها تقدير خاصية رئيسية تتحكم في هذا السلوك بدقة، ما قد يسرّع البحث عن علاجات سرطانية أفضل.
سطح رئيسي يتحكّم في وجهة الأدوية
فكرة مركزية في الورقة هي المساحة القطبية السطحية الطوبولوجية، أو Top_PSA. ببساطة، هذا رقم يعكس مقدار سطح الجزيء المكوّن من مناطق «قطبية» — أجزاء تحب الماء ويمكنها تكوين روابط هيدروجينية. الجزيئات ذات المساحة القطبية السطحية العالية غالبًا ما تجد صعوبة في عبور الأغشية الدهنية للخلايا وقد تُمتصّ ضعيفًا عند تناولها فمويًا. أما الجزيئات ذات المساحة القطبية السطحية المنخفضة جدًا فبإمكانها اجتياز الحواجز بسهولة مفرطة، مما يؤدي أحيانًا إلى آثار جانبية غير مرغوبة في أنسجة حسّاسة مثل الدماغ. أصبحت Top_PSA اختصارًا شائعًا لتقدير هذه الخصائص المتعلقة بالنقل لأنها تحسب بسرعة من رسم ثنائي البُعد للجزيء دون الحاجة لمحاكاة ثلاثية الأبعاد بطيئة.
تحويل رسومات الجزيئات إلى أرقام
جمع الباحثون مجموعة مُنقّحة مكوّنة من 156 مركبًا سامًا للخلايا مستمدة من أدوية مضادة للسرطان ومواد تجريبية فعلية. ثم حولوا كل جزيء إلى 58 ما يُسمى بالموصّفات — أرقام تلتقط خصائص مثل عدد الذرات، عدد الحلقات، مدى مرونة الروابط، عدد الذرات القادرة على تكوين روابط هيدروجينية، ومدى قطبية أو كهرسلبية أجزاء مختلفة من الجزيء. تأتي العديد من هذه الموصّفات من نظرية الرسوم البيانية، حيث يُعامَل الجزيء كشبكة من العقد والروابط. قدّم هذا البورتريه الرقمي الغني لكل جزيء مدخلاً لنماذج حاسوبية تحاول التنبؤ بقيم Top_PSA المحسوبة بواسطة مجموعات أدوات كيميائية مستخدمة على نطاق واسع.
اختبار مسارات متعددة للتنبؤ الدقيق
لإيجاد أفضل طريقة لربط هذه الموصّفات بـ Top_PSA، قارنت الفريق بين عدة استراتيجيات نمذجة. جربوا الانحدار الخطي القياسي بالإضافة إلى نسختين «منتظمتين» تُدعيان انحدار الريج وLASSO، المصممتين للتعامل بشكل أفضل مع معلومات ضوضائية ومتداخلة. كما استكشفوا مخططات مختلفة لتحضير البيانات: ملاءمة النماذج مباشرةً على الموصّفات الخام، ضغطها باستخدام تحليل المركبات الرئيسة (PCA)، مقياستها بطريقة تقلل تأثير القيم القصوى (مقياس متين)، تعديل القيم الشاذة، وتقليص المزايا عالية الارتباط باستخدام مقياس يُسمّى عامل تضخّم التباين. تم تقييم كل نهج بعناية باستخدام التحقق المتقاطع k‑fold، وهي طريقة تقسم البيانات مرارًا إلى مجموعات تدريب واختبار للحماية من الإفراط في الملاءمة.
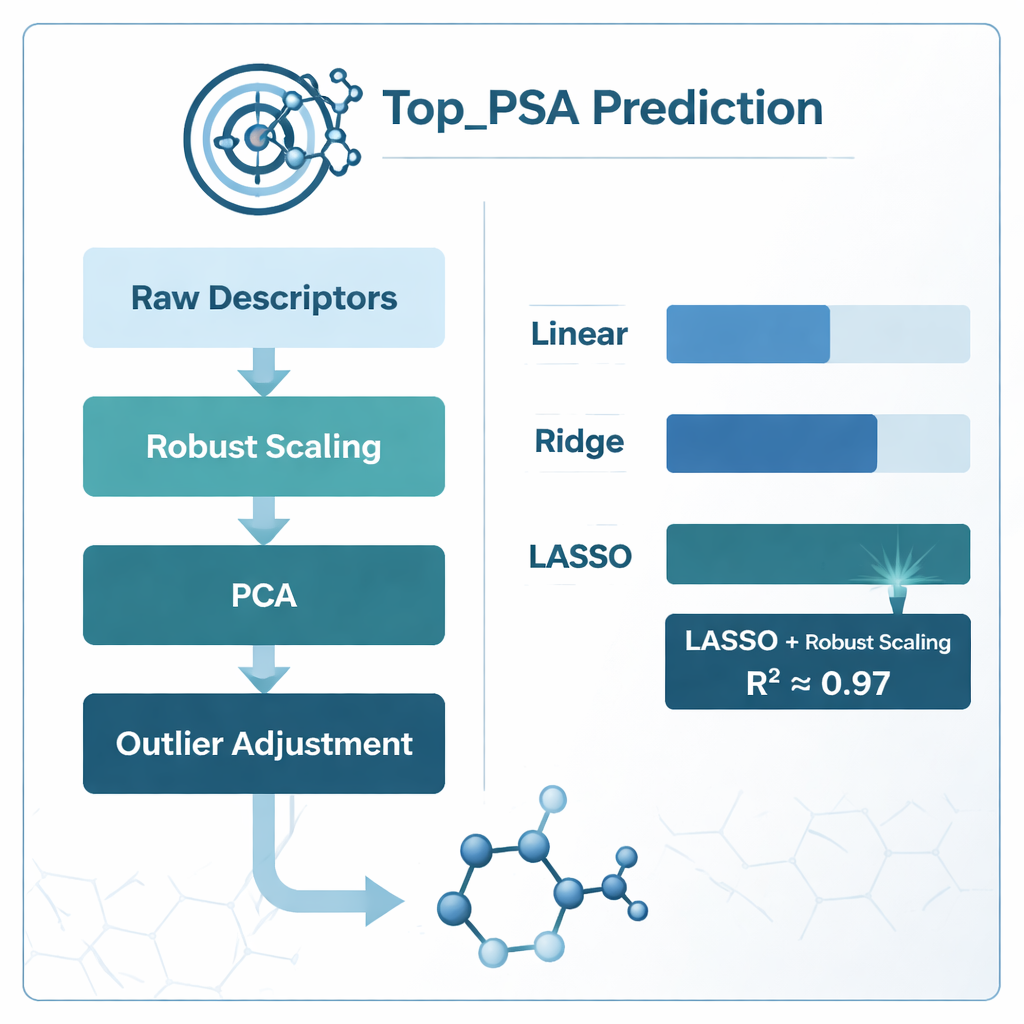
ما الذي نجح وما الذي تعلّمته النماذج
النتيجة الواضحة كانت مزيج مقياس متين مع انحدار LASSO، الذي حقق معامل تحديد (R²) حوالي 0.97 — ما يعني أنه قد يفسّر نحو 97% من التباين في Top_PSA عبر الـ 156 دواءً. اقتربت نماذج قائمة على PCA في الدقة الصافية لكنها كانت أصعب في التفسير الكيميائي لأن الموصّفات الأصلية تمّ دمجها في مكوّنات مجردة. أما التقليم البسيط للموصّفات المت correlation العالية باستخدام عامل تضخّم التباين فأساء الأداء فعليًا، مما يوحي بأن بعض المقاييس المتداخلة ما تزال تحمل معلومات كيميائية مفيدة. من خلال فحص أي أوزان الموصّفات احتفظت LASSO بأن تكون غير صفرية، وجد المؤلفون أن أهم العوامل كانت وجود ذرات غير متماثلة مثل النيتروجين والأكسجين، القدرة على إعطاء أو قبول الروابط الهيدروجينية، ومؤشرات تتعقّب كيفية ترتيب الذرات الكهربائية عبر الرسم البياني الجزيئي — جميعها ميزات تتوافق مع الفهم الكيميائي الحدسي للمساحة القطبية السطحية.
كيف يمكن أن يوجّه هذا تصميم أدوية أفضل
للقراء خارج المجال، الرسالة الرئيسة هي أن بصمات رياضية مُحضّرة بعناية للجزيئات، عند اقترانها بأساليب تعلّم آلة مختارة بعناية، يمكن أن تقدّم تقديرات سريعة وموثوقة لمدى «لزوجة» أو «انزلاق» أدوية السرطان أثناء تنقّلها في الجسم. تقدّم الدراسة إرشادات عملية للباحثين الآخرين حول كيفية تهيئة بيانات الموصّفات، أي نهج نمذجة يفضّل، وأي اختصارات ينبغي تجنّبها. على المدى البعيد، يمكن لمثل هذه النماذج المتينة والقابلة للتفسير لـ Top_PSA أن تساعد الكيميائيين في فرز مكتبات افتراضية ضخمة من المركبات المحتملة، مع تركيز جهودهم على المركبات ذات التوازن الصحيح لعبور الأغشية والسلامة — خطوة مهمة نحو علاجات سرطانية أكثر فعالية وأقل سمية.
الاستشهاد: Ahmad, S., Javed, S., Khalid, S. et al. A quantitative study of cytotoxic compounds using graph based descriptors and machine learning. Sci Rep 16, 5076 (2026). https://doi.org/10.1038/s41598-026-35728-7
الكلمات المفتاحية: أدوية سامة للخلايا, المساحة القطبية السطحية, موصّفات جزيئية, تعلّم الآلة, نفاذية الدواء