Clear Sky Science · ar
بروتين Vpr في فيروس نقص المناعة البشرية يسبب نزع مثيلة من محفز SNCA المضاد، ما يؤدي إلى خلل معرفي عصبي
لماذا لا يزال فيروس نقص المناعة البشرية يؤثر على الدماغ
يعيش الأشخاص المصابون بفيروس نقص المناعة البشرية لفترات أطول وبصحة أفضل بفضل الأدوية المضادة للفيروسات الحديثة. ومع ذلك، يعاني كثيرون منهم من مشاكل في الذاكرة والتركيز والحركة، حتى عندما يكون الفيروس في الدم تحت السيطرة الجيدة. تستكشف هذه الدراسة سبب حدوث ذلك من خلال التركيز على بروتين فيروسي صغير يُدعى Vpr وبروتين دماغي يُسمى ألفا‑سينوكلين، وهو أيضاً محوري في مرض باركنسون. قد يكشف فهم كيفية تفاعل هذين الجزيئين عن سبب تسارع شيخوخة الدماغ لدى المصابين بفيروس نقص المناعة البشرية ويقترح طرقاً جديدة لحماية الدماغ.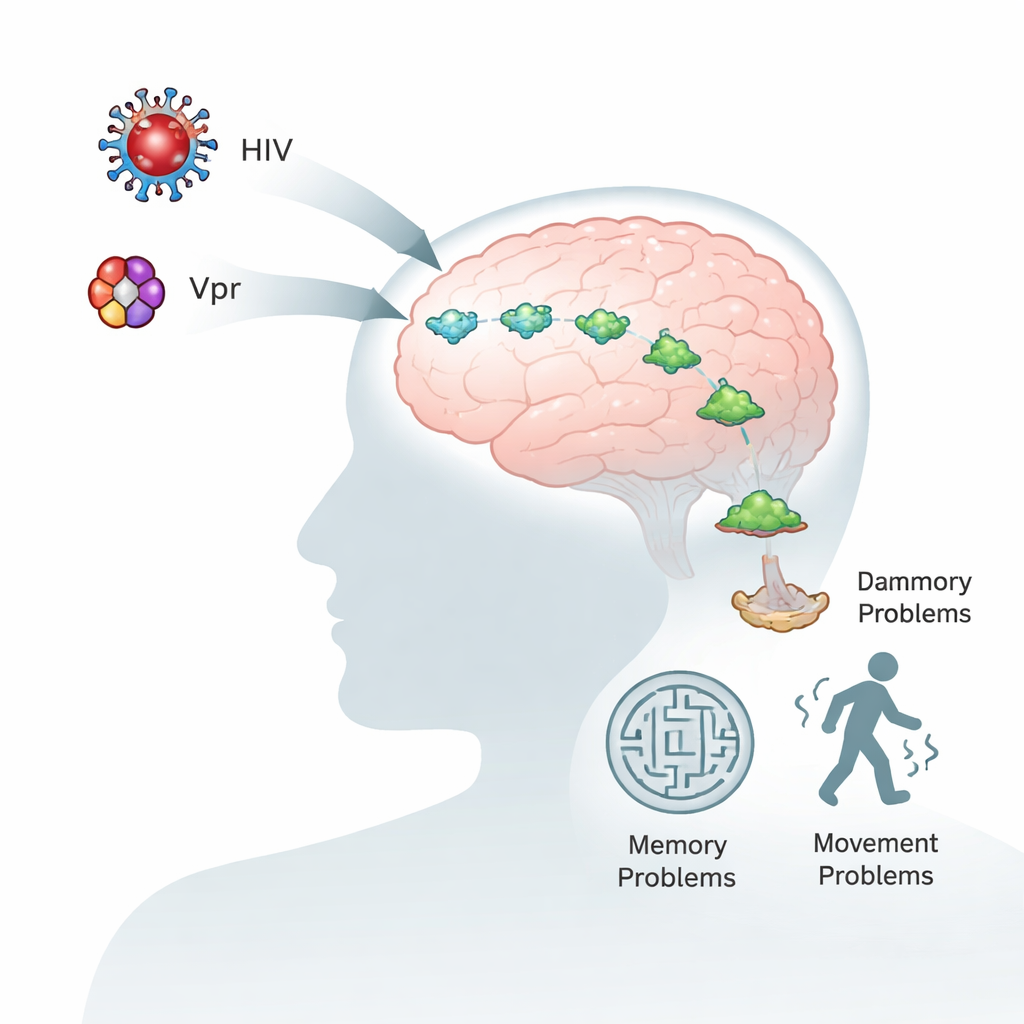
بروتين دماغي على مفترق طرق بين فيروس نقص المناعة وباركنسون
ألفا‑سينوكلين هو بروتين يساعد الخلايا العصبية على التواصل، لا سيما في المناطق الدماغية التي تتحكم في الحركة والذاكرة. عندما يتراكم الكثير من ألفا‑سينوكلين، يتجمع في تكتلات تُتلف المشابك، وتجهد الميتوكوندريا المولدة للطاقة، وتغذي الالتهاب. مثل هذه التكتلات تُعد سمة مميزة لمرض باركنسون. تُظهر الدراسة أن ألفا‑سينوكلين يتراكم أيضاً مع التقدم الطبيعي بالعمر في الفئران، وأن بروتين Vpr الفيروسي يرفع مستوياته أكثر في خلايا شبيهة بالعصب. هذا يضع ألفا‑سينوكلين عند تقاطع المشاكل الإدراكية المرتبطة بفيروس نقص المناعة والاضطرابات الحركية التقليدية.
كيف يعيد بروتين فيروسي كتابة «علامات الترقيم» الخلوية
تستخدم كل خلية علامات كيميائية على الحمض النووي—التي تُشَبَّه غالباً بعلامات ترقيم جزيئية—لتشغيل الجينات أو إيقافها. في هذا العمل، ركز الفريق على مفتاح تحكم قلّما نُظر إليه داخل جين ألفا‑سينوكلين يُدعى المحفز المضاد (antisense promoter). في الخلايا السليمة، يكون هذا المفتاح مثيلاً بكثافة، مما يبقيه هادئاً نسبياً. وجد الباحثون أن Vpr يزيل هذه العلامات عند مواقع محددة في هذه المنطقة، وهي عملية تُعرف بنزع المثيلة. بمجرد إزالة تلك العلامات، يصبح المحفز المضاد أكثر نشاطاً ويُحفز إنتاجاً إضافياً لألفا‑سينوكلين، مما يمهد الطريق لتكوّن التكتلات الضارة.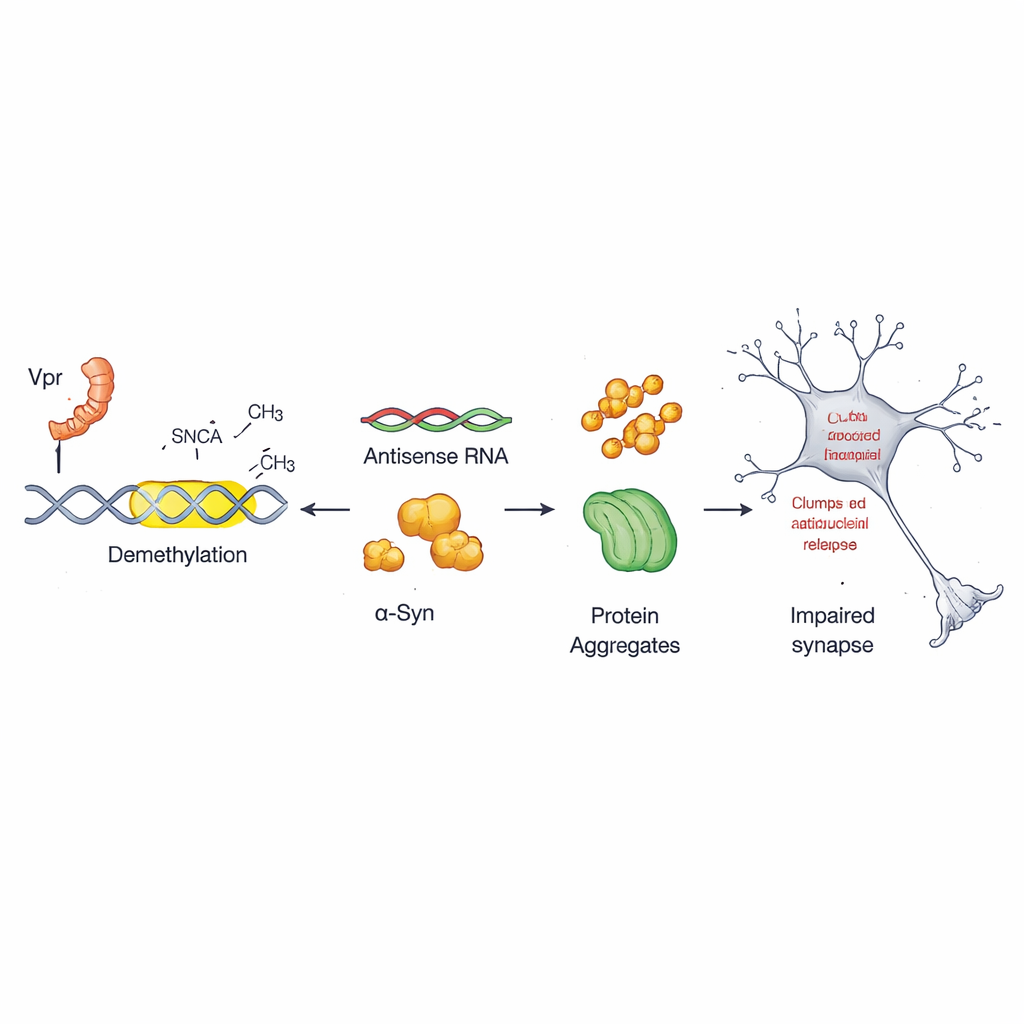
أدلة من الخلايا والفئران وأدمغة البشر
باستخدام خلايا بشرية مزروعة تشبه الخلايا العصبية وعصيات عصبية أولية من الفئران، أظهر الباحثون أن إضافة Vpr يزيد مستويات رسالة وأيضاً بروتين ألفا‑سينوكلين مع مرور الوقت. دواء يعزز نزع المثيلة على نطاق واسع مماثل بعض هذه التأثيرات، مما يؤكد دور الضبط الإيبيجينيتي. بالمقابل، مركب يُدعى DMOG، الذي يوقف إنزيمات نازعة المثيلة، منع Vpr من تنشيط المحفز المضاد بشكل كامل. ثم توجه الفريق إلى عينات أدمغة بشرية من أشخاص مصابين وغير مصابين بفيروس نقص المناعة البشرية. أظهرت أدمغة المتبرعين المصابين بالفيروس—سواء قبل أو بعد العلاج المضاد للفيروسات—علامات مثيلة أقل في نفس منطقة الحمض النووي ومستويات أعلى من ألفا‑سينوكلين ونصه المضاد، لا سيما في المتبرعين المصابين بالخرف المرتبط بفيروس نقص المناعة. وهذا يشير إلى أن الفيروس يترك ندبة إيبيجينية دائمة في الدماغ.
من التغيرات الجزيئية إلى مشاكل الذاكرة
لربط هذه التحولات الجزيئية بالسلوك، فحص الباحثون كيف يؤثر Vpr على دوائر الدماغ في الفئران. عندما طبقوا Vpr على شُرائح من قرن آمون في الفأر، وهي منطقة حيوية للذاكرة، لم يتغير قوة الإشارة الأساسية بين الخلايا العصبية، لكن قدرة تقوية الاتصالات—وهي عملية تُدعى التقوية طويلة الأمد (long‑term potentiation)—انخفضت. في الفئران الحية، أدى حقن Vpr المستهدف في قرن آمون إلى أداء أضعف في مهمة ذاكرة مكانية تُطلب فيها من الحيوانات تذكر مواقع الأشياء. مجتمعة، تشير هذه التجارب إلى أن تغيرات ألفا‑سينوكلين المدفوعة بـVpr ليست مجرد فضول كيميائي حيوي؛ بل تتحول إلى تضعف في المشابك ونقصات قابلة للقياس في الذاكرة.
ماذا يعني هذا للأشخاص المصابين بفيروس نقص المناعة البشرية
تقترح هذه الدراسة سلسلة واضحة من الأحداث: يفرج فيروس نقص المناعة البشرية عن Vpr، يعيد Vpr برمجة مفتاح DNA حاسم الذي يتحكم في ألفا‑سينوكلين، يتراكم البروتين ويتكتل، وتفقد الخلايا العصبية تدريجياً قدرتها على التواصل ودعم الذاكرة. ونظراً لأن مشاكل ألفا‑سينوكلين المماثلة تقوم بدور في مرض باركنسون، تلمح النتائج إلى أن فيروس نقص المناعة البشرية والأمراض التنكسية العصبية التقليدية قد تتشارك آليات متداخلة. والأهم من ذلك، تسلط النتائج الضوء على استراتيجيات محتملة جديدة—مثل أدوية تُثبّت مثيلة الحمض النووي عند المحفز المضاد أو تحد من تراكم ألفا‑سينوكلين—لإبطاء أو منع الانحدار المعرفي والحركي المرتبط بفيروس نقص المناعة البشرية.
الاستشهاد: Santerre, M., Wang, Y., Kalamarides, D. et al. HIV Vpr induces demethylation of the SNCA antisense promoter, leading to neurocognitive impairment. Sci Rep 16, 6078 (2026). https://doi.org/10.1038/s41598-026-35691-3
الكلمات المفتاحية: الاضطرابات المعرفية العصبية المرتبطة بفيروس نقص المناعة البشرية, ألفا-سينوكلين, علم التخلق الجيني (الإيبيجينيتكس), مثيلة الحمض النووي, أعراض شبيهة بباركنسون