Clear Sky Science · ar
التحقيق في السوائل الأيونية المبنية على أكوراميديس كمثبتات محتملة للترانستيريتين باستخدام حسابات DFT والتَرَسّخ الجزيئي ودراسات ADMET
لماذا من الصعب تصنيع حبة لعلاج قلب نادر
تراكم أميلويد الترانستيريتين (ATTR) هو مرض خطير يتراكم فيه بروتين دموي في القلب والأعصاب، ما يؤدي إلى تلفهما ببطء. دواء جديد، أكوراميديس، يمكن أن يساعد في إيقاف هذا التراكم، لكن هناك مشكلة عملية: الدواء لا يذوب جيداً في الماء، مما يصعّب امتصاصه من قبل الجسم عند تناوله على شكل حبة. تستقصي هذه الدراسة طريقة ذكية لإعادة تصميم أكوراميديس على شكل أملاح جديدة تُعرف بالسوائل الأيونية، قد تجعل الدواء أسهل في الابتلاع وأكثر فعالية.
تحويل دواء واعد إلى شكل قابل للشرب
لكي تعمل الحبة، يجب أولاً أن تذوب في السوائل المائية للمعدة والأمعاء، ثم تعبر جدار الأمعاء إلى مجرى الدم. أكوراميديس فعال في تثبيت بروتين الترانستيريتين (TTR)، ما يساعد على منع تكوّن تجمعات بروتينية ضارة مرتبطة بـATTR، لكنه ضعيف الذوبان ولديه توافر حيوي فموي منخفض. سعى الباحثون لمعالجة ذلك بقرينة أكوراميديس كيميائياً مع جزيئات شاردة مختلفة، فخلقوا ثلاث نسخ جديدة من السوائل الأيونية (IL1, IL2, وIL3). صُممت هذه النسخ لتتصرف أكثر كأملاح سائلة بدلاً من بلورات جامدة، مما قد يعزّز ذوبان الدواء وتوزعه داخل الجسم. 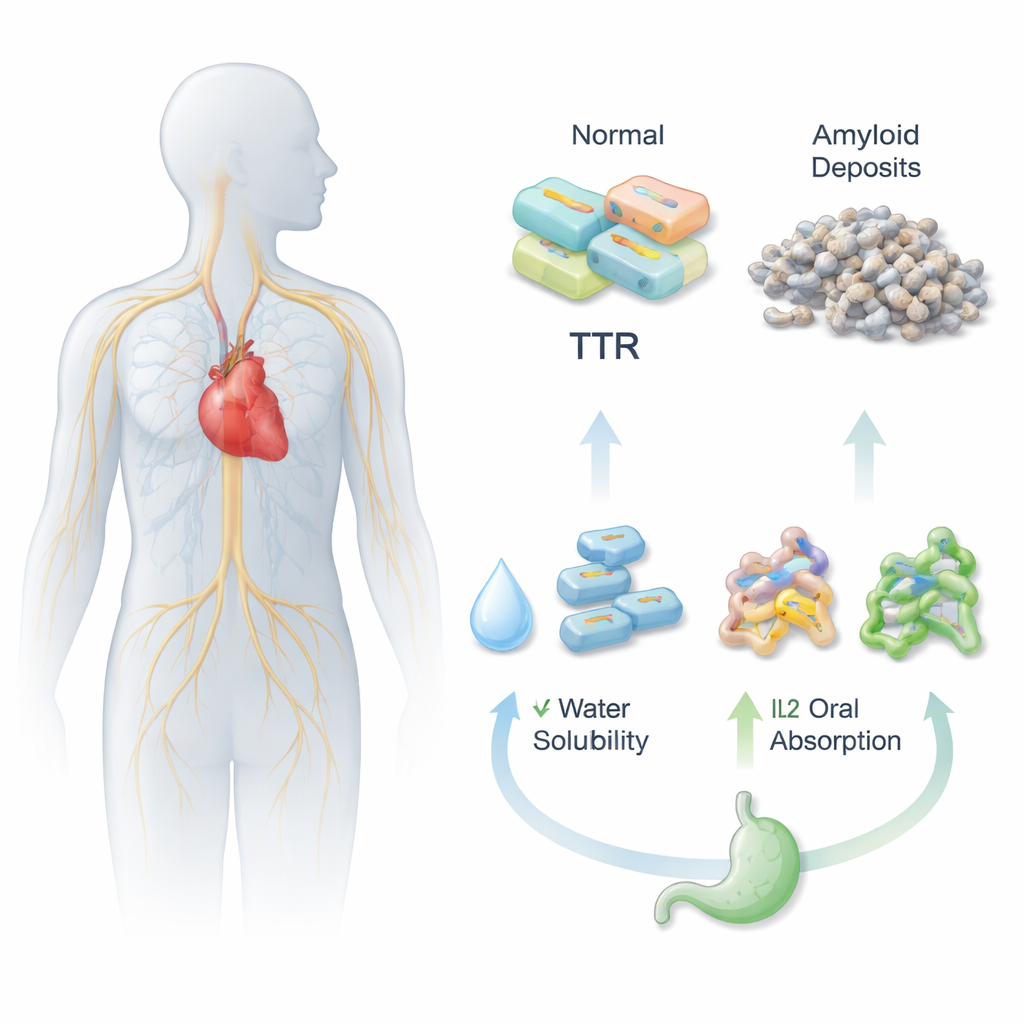
استكشاف الجزيئات الجديدة باستخدام الحاسوب
بدلاً من الانتقال مباشرة إلى تجارب على الحيوانات أو البشر، استخدم الفريق طرقاً حاسوبية متقدمة للتنبؤ بكيفية تصرّف هذه الأشكال الجديدة. قدّرت حسابات الكيمياء الكمومية قطبية كل جزيء — وهو مؤشر رئيسي على الذوبان في الماء — ومدى قابلية إلكتروناته للتباين، وهو ما يرتبط بكيفية تفاعله مع البروتينات. برز IL1 بامتلاكه أعلى عزم ثنائي وأقوى استجابة إلكترونية، ما يشير إلى أنه ينبغي أن يذوب أفضل في الماء ويكوّن تواصلاً أقوى وأكثر مرونة مع أهدافه. كما اقترحت حسابات الطاقة أن IL1 أكثر استقراراً حرارياً من الدواء الأصلي والنسختين الأخريين من السوائل الأيونية، مما يعني أنه أقل عرضة للتفكك قبل الوصول إلى هدفه.
مدى إحكام الدواء لالتصاقه بالهدف
بعد ذلك، استخدم الباحثون التَرَسّخ الجزيئي، وهو اختبار افتراضي «مفتاح-قفل»، لرؤية مدى ملاءمة أكوراميديس وأشكاله الأيونية الثلاثة لقناة الربط في بروتين TTR. ارتبطت المركبات الأربعة جميعها بالمنطقة الصحيحة من TTR، لكن IL1 شكّل الإحكام الأقوى، مع طاقة ارتباط أكثر تفضيلاً وعدة تواصلات مثبتة — خاصة روابط هيدروجينية — مع أحماض أمينية رئيسية في البروتين. يقترح هذا الترابط الأقوى أن IL1 قد يكون أفضل من الدواء الأصلي في إبقاء TTR في بنيته الرباعية الآمنة، مما يساعد على منع التفكك والطِيّ الضار الذي يؤدي إلى ترسّبات الأميلويد.
هل سيمتص الجسم هذه الأشكال الجديدة ويطهرها؟
أخيراً، استخدم الفريق أدوات صيدلانية عبر الإنترنت لاستكشاف كيفية تعامل الجسم المحتمل مع هذه المركبات — مدى ذوبانها، عبورها لجدار الأمعاء، دورانها في الدم، وطريقة تصفيتها في النهاية. تُنبئ التوقعات أن جميع السوائل الأيونية الثلاثة أكثر قابلية للذوبان في الماء من أكوراميديس، مع إظهار IL3 أعلى ذوبان خام. تحسنت مقاييس نفاذية الأمعاء والامتصاص الفموي الإجمالي لجميع السوائل الأيونية، مع تقديم IL1 وIL2 أفضل توازن بين اختراق الأمعاء والتوافر الحيوي المتوقع. كما تغيّرت ارتباط البروتين في الدم ومعدلات الإزالة وأنصاف العمر بطريقة تشير إلى أن أشكال السوائل الأيونية قد توفر تعرضاً أكثر موثوقية بعد الجرعات الفموية، مع تقديم IL1 مرة أخرى ملفاً ملائماً بشكل خاص. 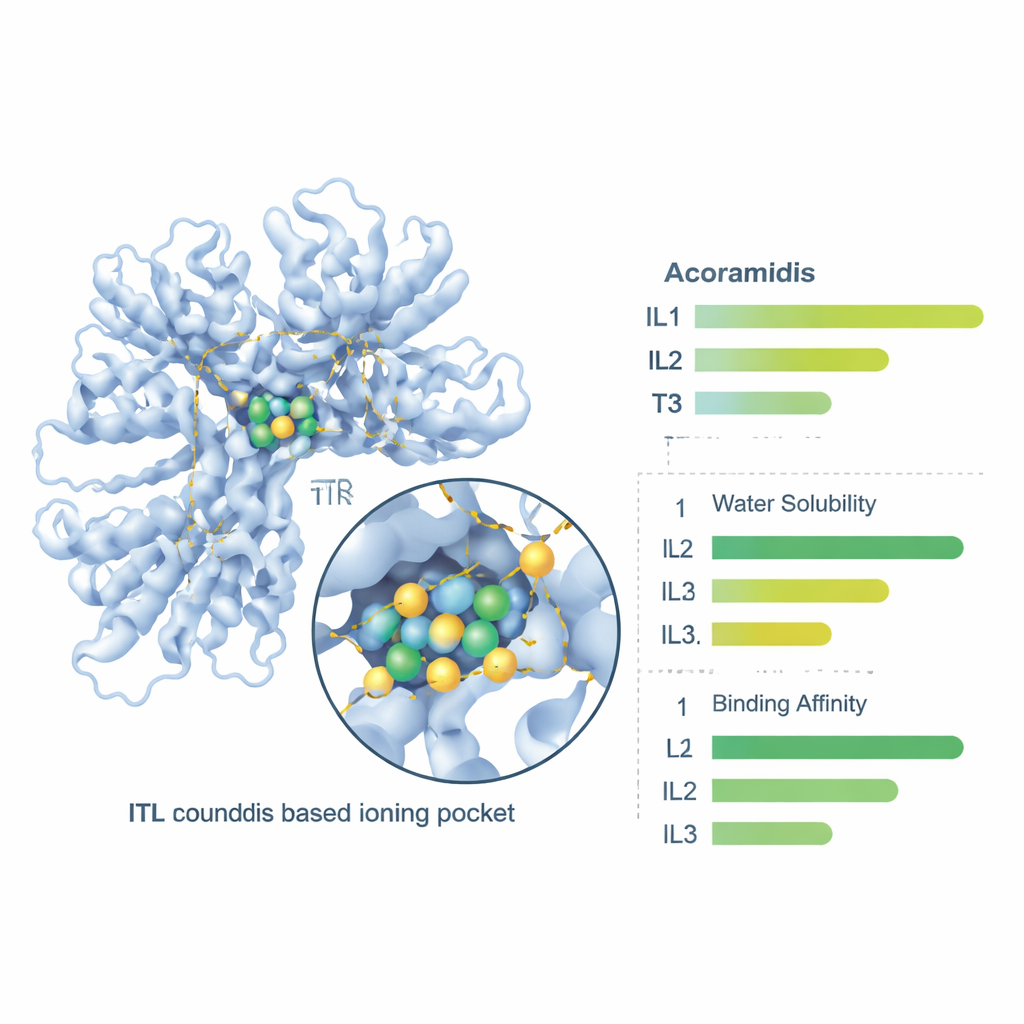
ماذا قد يعني هذا لعلاجات ATTR المستقبلية
لغير المتخصص، الرسالة الأساسية هي أن الدواء أكوراميديس يبدو واعداً بالفعل لعلاج مرض قلبي وعصبي نادر لكنه خطير، غير أن ضعف ذوبانه يقيد فعاليته عند التعاطي الفموي. تُظهر هذه الدراسة — كلياً عبر اختبارات حاسوبية — أنه قد يكون من الممكن تحويل أكوراميديس إلى سوائل أيونية مصمّمة خصيصاً تذوب أفضل، وترتبط بقوة أكبر بهدفها البروتيني، وتمتص بكفاءة أعلى. من بين المرشحين الثلاثة، يبدو أن IL1 يحقق أفضل توازن من حيث الاستقرار، وقوة الارتباط، والذوبان، والامتصاص الفموي المتوقع، مما يجعله خياراً قوياً للتطوير المختبري والسريري المستقبلي نحو علاجات أكثر فاعلية وسهولة في الاستخدام لـATTR.
الاستشهاد: Mostaghni, F., Mahani, N.M. Investigation of Acoramidis-based ionic liquids as potential stabilizers of transthyretin using DFT calculations, molecular docking, and ADMET studies. Sci Rep 16, 6540 (2026). https://doi.org/10.1038/s41598-026-35684-2
الكلمات المفتاحية: تراكم أميلويد الترانستيريتين, أكوراميديس, السوائل الأيونية, طِيّ البروتين, الإعطاء الدوائي الفموي