Clear Sky Science · ar
تحليل تكاملي للبروتيوميات والميتوبولوميات يكشف اضطرابًا في أيض الأحماض الأمينية في خلايا اللوكيميا النخاعية الحادة المقاومة للأدريا
لماذا تتوقف فعالية بعض أدوية اللوكيميا
غيّرت العلاج الكيميائي بشكل جذري معالجة اللوكيميا النخاعية الحادة (AML)، وهو سرطان دم سريع النمو. ومع ذلك يعود المرض لدى كثير من المرضى لأن خلايا السرطان تتعلّم النجاة من الأدوية نفسها المصممة لقتلها. تطرح هذه الدراسة سؤالًا بسيطًا لكنه محوري: ما الذي يتغير داخل خلايا اللوكيميا عندما تصبح مقاومة للأدرياميسين، أحد أدوية العلاج الكيميائي القياسية، وهل يمكن أن تشير تلك التغييرات إلى طرق جديدة لاستعادة فعالية الدواء؟
نظرة داخل خلايا اللوكيميا
لاستكشاف ذلك، قارن الباحثون خط خلايا بشري شائع للـ AML يُدعى HL60 مع خط شقيق جُعل مقاومًا للأدرياميسين (HL60/R). بدلًا من فحص جين أو بروتين واحد في كل مرة، استخدموا مقاربَتَين واسعتين ومتكاملتين. قيست البروتيوميات آلاف البروتينات المختلفة — جزيئات الفعل التي تقوم بمعظم مهام الخلية. وقاسَت الميتابولوميات مئات الجزيئات الصغيرة التي تشكّل أيض الخلية، بما في ذلك الدهون والسكريات والأحماض الأمينية. من خلال دمج هاتين الطبقتين «الأوميكسيتين» بنى الفريق صورة مفصّلة لكيفية اختلاف الخلايا المقاومة عن نظيراتها الحساسة.
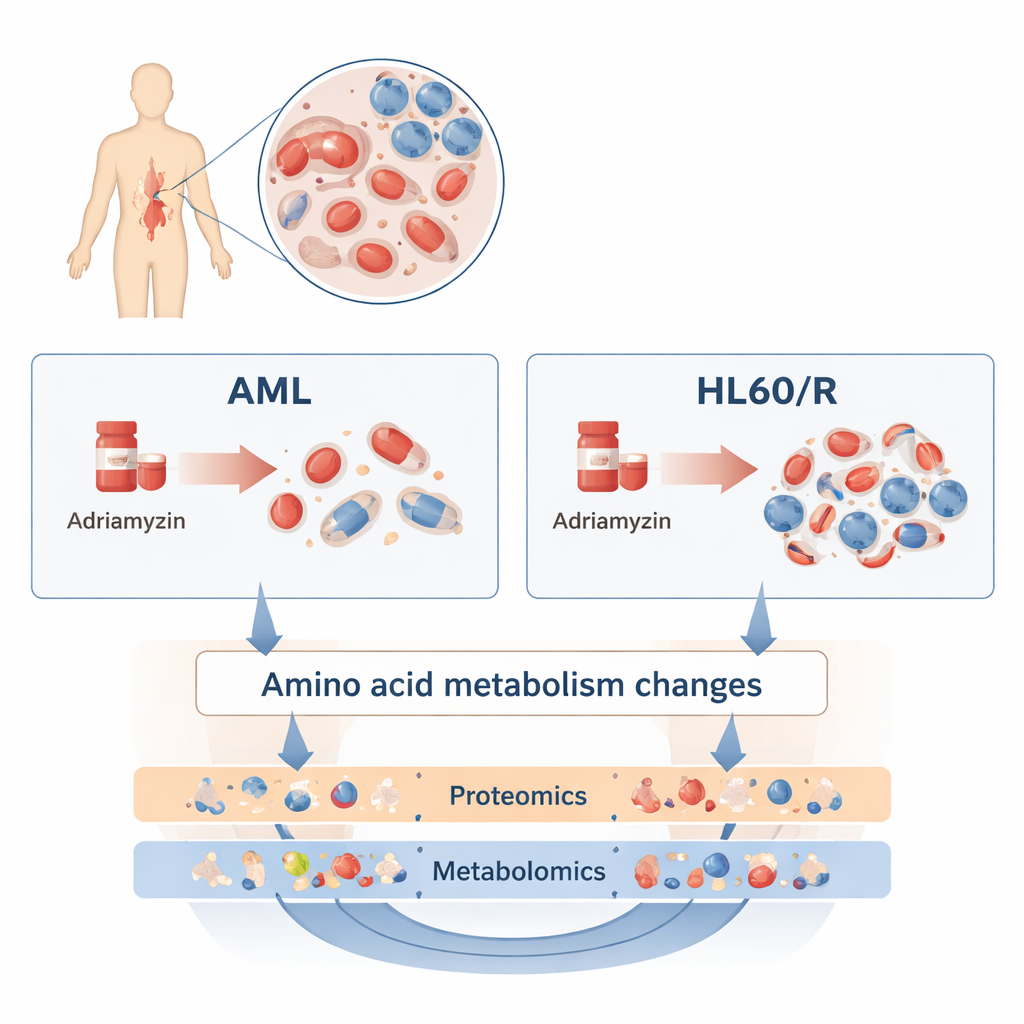
إعادة توصيل واسعة لآليات الخلية
كشفت مسح البروتيوميات عن تغييرات واسعة النطاق: أكثر من 3200 بروتين وُجدت بمستويات أعلى أو أقل في الخلايا المقاومة للأدرياميسين مقارنةً بخلايا HL60 الطبيعية. تراكمت العديد من هذه البروتينات في مسارات تتحكم بكيفية استخدام الخلايا للطاقة والاستجابة للضغط. على وجه الخصوص، تغيّرت بروتينات في مسار إشارة cAMP، ومسار HIF‑1 (الذي يساعد الخلايا على التأقلم مع نقص الأكسجين)، والتنفس التأكسدي (عملية رئيسية لإنتاج الطاقة في الميتوكوندريا). تشير هذه التحولات إلى أن خلايا اللوكيميا المقاومة تعيد برمجة كيفية تنفسها ونموها وإرسال الإشارات فيما بينها لتتحمّل العلاج الكيميائي.
تحول الأيض نحو الأحماض الأمينية
قدمت تحليلات الميتابولوميات سردًا مُكمّلًا. من بين نحو 1400 مستقلب مكتشف، تغير 260 بشكل ملحوظ في الخلايا المقاومة. فرّقت النماذج الإحصائية بوضوح بين الخلايا المقاومة وغير المقاومة، موضحةً بصمة أيضية ثابتة للمقاومة. عندما رُسِمت المستقلبات المتغيرة على المسارات الحيوية المعروفة، برزت عدة مسارات. كان العديد من المسارات المتأثرة مرتبطًا بالأحماض الأمينية، وحدات بناء البروتينات — خصوصًا تلك المتعلقة بالألانين، الأسبارتات، الغلوتامات، السيستين، الميثيونين، والغلوتاثيون. كما تعطلت شبكات أخرى مثل أيض البيورين والبيريميدين (المهمة للحمضين النووي والريبي النووي) ومعالجة بعض الدهون، ما يؤكد أن المقاومة مرتبطة بإعادة تشكيل أيضية واسعة النطاق.
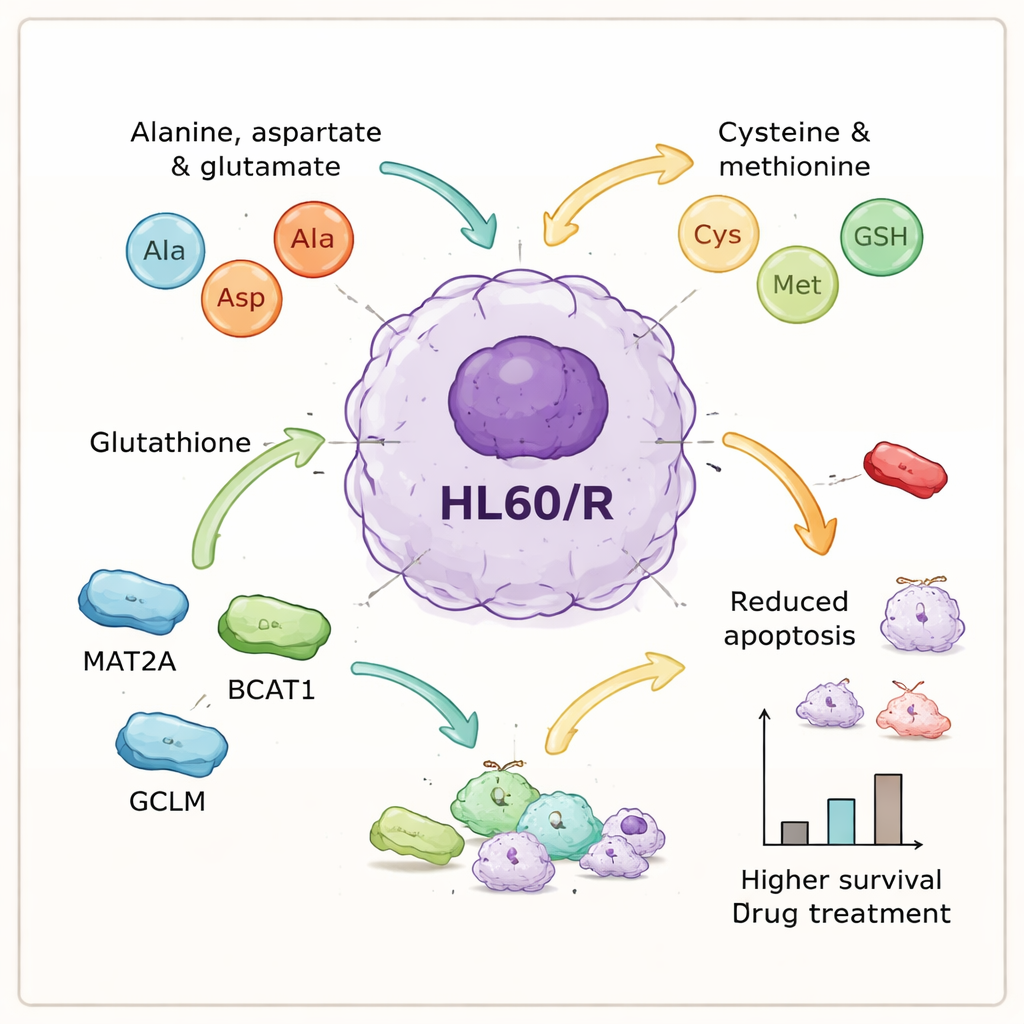
العناصر الجزيئية الرئيسية التي تساعد الخلايا السرطانية على التحمل
بدمج بيانات البروتينات والمستقلبات، ركّز المؤلفون على مجموعة من العمليات المرتبطة بالأحماض الأمينية التي بدت مركزية للمقاومة. اختاروا ستة بروتينات مرتبطة بهذه المسارات — GOT1، GPX1، AHCY، MAT2A، BCAT1، وGCLM — للفحص الأكثر قربًا. أكدت الاختبارات المخبرية أن خمسة منها كانت أكثر وفرة في الخلايا المقاومة، متسقة مع فكرة أن معالجة الأحماض الأمينية مُفعّلة، بينما كان أحد إنزيمات مضادات الأكسدة، GPX1، أقلّ وفرة. لاستقصاء العلاقة السببية، استخدم الفريق حمضيات رنا متداخلة صغيرة لخفض تعبير ثلاثة من البروتينات المرتفعة — MAT2A، BCAT1، وGCLM — في الخلايا المقاومة. عندما أُنهِكت هذه البروتينات، خضعت الخلايا لمعدلات أعلى بكثير من الموت الخلوي المبرمج بعد العلاج، ما يعني أنها فقدت جزءًا كبيرًا من الحماية التي اكتسبتها ضد الأدرياميسين.
ماذا يعني ذلك لعلاجات المستقبل
تشير هذه النتائج مجتمعة إلى أن خلايا AML المقاومة للأدرياميسين تبقى على قيد الحياة ليس فقط بسبب طفرات مفردة، بل لأنها تعيد تشكيل كيميائها الداخلية، مع كون أيض الأحماض الأمينية محورًا مركزيًا. من خلال تحويل مزيد من الموارد إلى مسارات معينة للأحماض الأمينية والغلوتاثيون، تبدو الخلايا أفضل قدرة على إدارة الإجهاد، وإصلاح الضرر، وتجنّب الموت عند التعرض للعلاج الكيميائي. للقراء غير المتخصصين، الرسالة الأساسية أن المقاومة ليست عشوائية: فهي تتبع أنماطًا قابلة للقياس وربما للاستهداف. على المدى الطويل، قد تُدمَج أدوية تعيّق بروتينات معالجة الأحماض الأمينية مثل MAT2A، BCAT1، أو GCLM مع الأدرياميسين أو عوامل مشابهة، مما يوفر لأطباء السرطان أدوات جديدة لمنع المقاومة أو التغلب عليها لدى مرضى اللوكيميا النخاعية الحادة.
الاستشهاد: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
الكلمات المفتاحية: اللوكيميا النخاعية الحادة, مقاومة الدواء, أدرياميسين, أيض الأحماض الأمينية, متعدد الأوميكس