Clear Sky Science · ar
التوليف، التوصيف، تحليل DFT، الإرساء الجزيئي والتحقيقات المضادة للسرطان في سرطان القولون والمستقيم لمركب زنك(II) جديد من البيرازول-الهيدرازون
لماذا قد يقاوم دواء قائم على معدن سرطان القولون بلطف أكبر
تُبنى العديد من الأدوية القوية لمكافحة السرطان حول معادن ثقيلة مثل البلاتين. قد تكون فعالة لكنها غالبًا ما تصحبها آثار جانبية قاسية ومقاومة مع مرور الوقت. تستكشف هذه الدراسة نهجًا مختلفًا: مرشح دوائي جديد مبني حول الزنك، وهو مغذٍ أساسي موجود بالفعل في أجسامنا، مرتبطٌ بهيكل عضوي يسمى بيرازول–هيدرازون. طرح الباحثون سؤالًا عما إذا كان تضمين الزنك في هذا الهيكل قد يولد مركبًا يهاجم خلايا سرطان القولون بفعالية مع الحفاظ على الخلايا السليمة.
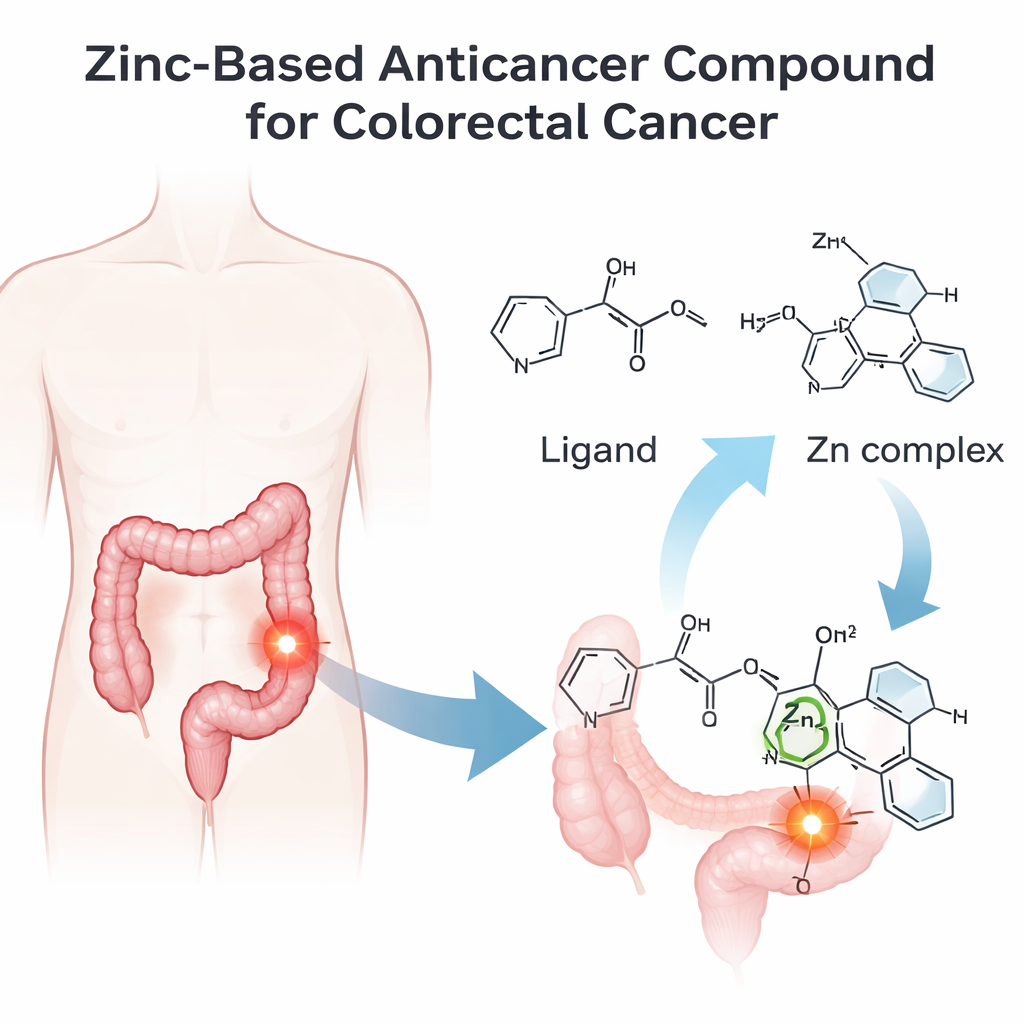
بناء جزيء زنك أذكى
صممت المجموعة أولًا وركبت جزيئًا عضويًا جديدًا أطلقوا عليه اسم IMP، ثم ربطوه بأيون زنك ليصنعوا مركب الزنك المسمى IMP-Zn. أكدوا البنية الدقيقة لكليهما باستخدام مجموعة من التقنيات التي تكاد تشكل «بصمة» للجزيئات: طيف الأشعة تحت الحمراء لرصد الروابط الكيميائية، والرنين المغناطيسي النووي لرسم مواقع الذرات، ومطيافية الكتلة للتحقق من الكتلة الجزيئية، وامتدت الأشعة فوق البنفسجية–المرئية لدراسة تفاعل المركبات مع الضوء. هذه التجارب، جنبًا إلى جنب مع اختبارات الموصلية الكهربائية، أظهرت أن الزنك مُنسق بإحكام مع ثلاثة ذرات رئيسية في IMP وذرتي كلوريد، مكوّنًا مركبًا مركزه الزنك واحدًا ومحدّد البنية.
التعمق في الجزيء بكيمياء افتراضية
لتكملة قياسات المختبر، أجرى الباحثون محاكاة حاسوبية مفصلة باستخدام نظرية الدالة الكثافية (DFT). مكنت هذه الحسابات من التنبؤ بكيفية توزيع الإلكترونات داخل IMP وIMP-Zn، ومدى استقرار كل شكل، ومدى سهولة مشاركة الجزيئات في تفاعلات كيميائية. أظهرت النتائج أنه عند ارتباط الزنك تنكمش الفجوة الطاقية بين المدارين «الحدوديين» للجزيء، مما يعني أن الإلكترونات يمكنها التحرك بسهولة أكبر داخل البنية. عادةً ما يُترجم ذلك إلى تفاعل كيميائي أعلى. كما أبدى مركب الزنك مؤشرًا أعلى لما يسمى بالإلكتروفيلية، ما يشير إلى أنه مجهز بشكل أفضل للتفاعل مع الأهداف البيولوجية مقارنة بالليجاند الحر IMP بمفرده.
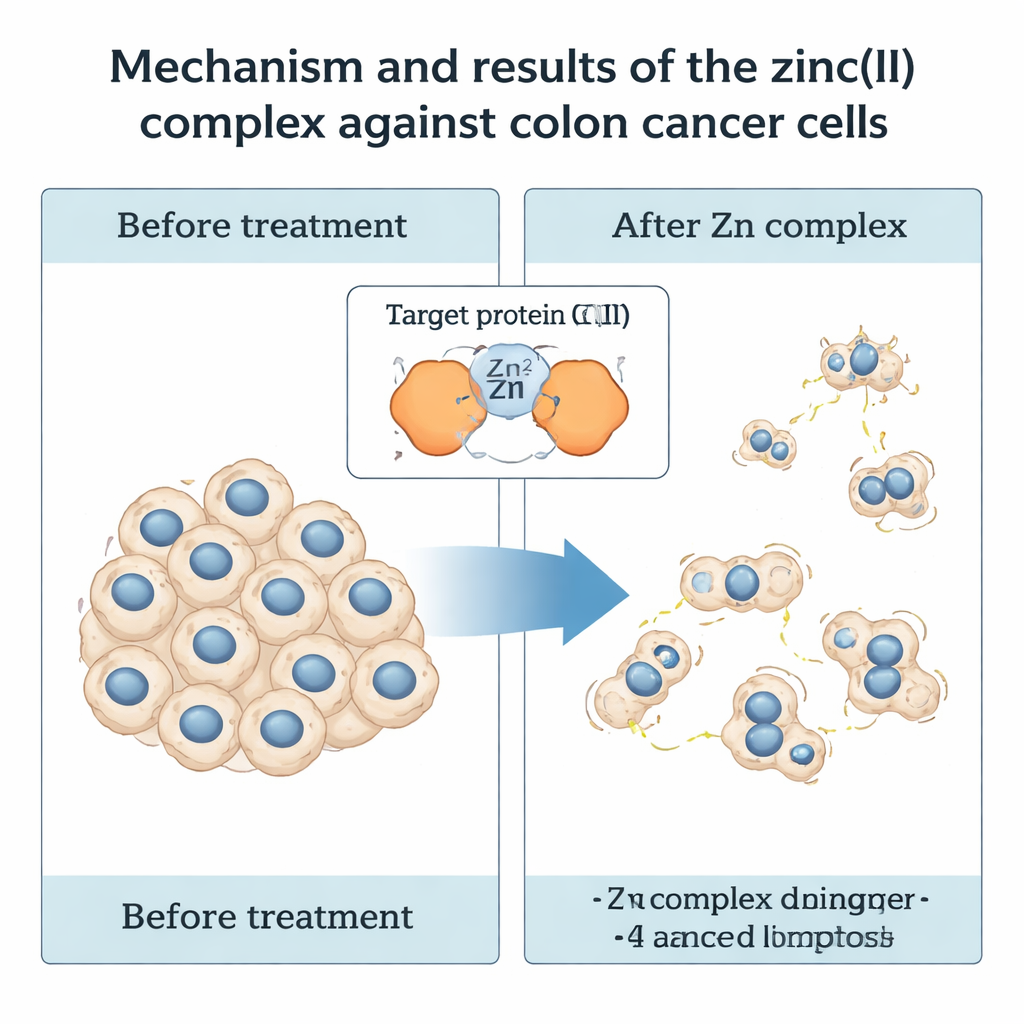
كيف يهاجم مركب الزنك خلايا سرطان القولون
كان الاختبار الحقيقي حيويًا. عالج الباحثون خلايا سرطان القولون والمستقيم البشرية (HCT116) بـ IMP وIMP-Zn بجرعات وأزمنة مختلفة، ثم قاسوا نسبة الخلايا الناجية. أبطأ المركبان نمو الخلايا السرطانية، لكن مركب الزنك كان أقوى بوضوح: بعد 48 ساعة خفّض IMP-Zn قابلية الخلايا للبقاء إلى النصف عند حوالي 25 ميكرومولار، بينما احتاج الليجاند وحده إلى جرعة أعلى بكثير. وعلى نحوٍ لا يقل أهمية، لم تظهر نفس تراكيز IMP-Zn تأثيرًا سامًا يمكن اكتشافه على خط خلايا كلوية بشرية طبيعية (HEK293)، مما يشير إلى درجة من الانتقائية لخلايا السرطان. عندما تتبع الفريق الخلايا المعالجة على مدار أسبوعين، وجدوا أن IMP-Zn قلل بشدة كلًا من عدد وحجم المستعمرات التي يمكن للخلايا تشكيلها، مما يدل على أنه يتداخل مع قدرتها على التكاثر على المدى الطويل.
دلائل على دفع الخلايا نحو الموت المبرمج
لفهم كيفية إضرار مركب الزنك بالخلايا السرطانية، فحص العلماء دورة الخلية—سلسلة المراحل التي تمر بها الخلايا أثناء نموها وانقسامها. بعد التعرض لـ IMP-Zn، انتقال جزء أكبر بكثير من خلايا HCT116 إلى طور «SubG0»، وهو بصمة للخلايا ذات الحمض النووي المتجزئ. يرتبط هذا النمط عادة بالاستماتة المبرمجة، وهي شكل مسيطر عليه من موت الخلايا يستهدفه كثير من الأدوية المضادة للسرطان. قدمت محاكيات الإرساء الجزيئي قطعة أخرى من الأحجية: اقترحت النماذج الافتراضية أن IMP-Zn يرتبط بقوة أكبر من IMP بعدد من البروتينات المرتبطة بالسرطان، بما في ذلك كيناز مستقبل عامل النمو، وكيناز منظم لدورة الخلية، وإنزيم يقوم بتحويل الأدوية. تدعم هذه التفاعلات الأوثق فكرة أن تنسيق الزنك يساعد المركب على التمسك بآلات خلوية حرجة وتعطيل بقاء الخلايا السرطانية.
ما الذي قد يعنيه ذلك للعلاجات المستقبلية
مجملًا، تُظهر الدراسة أن «تزيين» هيكل بيرازول–هيدرازون بالزنك يفعل أكثر من مجرد تعديل كيميائه: إنه يحول IMP إلى عامل أكثر تفاعلًا، وأكثر فعالية، وعلى ما يبدو أكثر انتقائية ضد خلايا سرطان القولون والمستقيم. وبينما لا يزال IMP-Zn بعيدًا عن أن يكون دواءً جاهزًا—فلم يتم اختباره بعد على الحيوانات أو البشر—تُعد قدرته على إبطاء نمو خلايا سرطان القولون بشكل كبير، ودفع الخلايا نحو الاستماتة، والحفاظ على سلامة الخلايا الطبيعية علامة على أنه مرشح واعد ضمن فئة متنامية من الأدوية المعدنية القائمة على الزنك. تشير هذه العمل إلى أن المركبات الزنك المصممة بعناية قد توفر بدائل أو مكمّلات مستهدفة ولطيفة للعلاج الكيماوي التقليدي القائم على المعادن في المستقبل.
الاستشهاد: Mermer, A., Bayrak, A.M., Bolat, Z.B. et al. Synthesis, characterization, DFT analysis, molecular docking and anticancer investigations in colorectal carcinoma of a novel pyrazole-hydrazone zinc(II) complex. Sci Rep 16, 6391 (2026). https://doi.org/10.1038/s41598-026-35664-6
الكلمات المفتاحية: عوامل مضادة للسرطان قائمة على الزنك, سرطان القولون والمستقيم, مركب بيرازول هيدرازون, الإرساء الجزيئي, الاستماتة المبرمجة