Clear Sky Science · ar
التأثيرات المحسِّنة للإشعاع لجسيمات الفضة النانوية المستهدفة لتكوّن الأوعية وإشارات البروتينات المصفافية في خطوط خلايا سرطان الثدي الثلاثي السلبية
جعل سرطانات الثدي القاسية أكثر عرضة للعلاج
يُعد سرطان الثدي الثلاثي السلبي أحد أصعب أنواع سرطان الثدي في المعالجة. يميل إلى النمو السريع والانتشار المبكر، ويعوزها "مقابض" جزيئية معتادة تستهدفها العديد من الأدوية الحديثة. كثيراً ما يكون الإشعاع جزءًا من العلاج، لكن هذه الأورام قد تُظهر مقاومة عنيدة. تطرح هذه الدراسة سؤالاً بسيطاً ومثيراً: هل يمكن لجسيمات الفضة الصغيرة أن تجعل الإشعاع أكثر فعالية، وفي الوقت نفسه تبطئ قدرة الورم على تكوين أوعية دموية جديدة والانتشار؟
مساعدات فضية دقيقة للإشعاع
ركز الباحثون على جسيمات الفضة النانوية—كرات فضية صغيرة للغاية تقاس بالمليارات من المتر. ونظراً لكثافة الفضة وتفاعلها القوي مع أشعة إكس، يمكن لهذه الجسيمات تركيز تأثيرات الإشعاع في المواقع التي تتراكم فيها. عمل الفريق مع نموذجين مخبريين شائعين لسرطان الثدي الثلاثي السلبي، وقارنها بخط خلوي ثديي غير سرطاني. اختبروا أولاً سمية جسيمات الفضة بمفردها ووجدوا أن الخلايا السرطانية تُقتل بجرعات أقل بكثير من الخلايا الطبيعية، مما يشير إلى نافذة علاجية مفيدة. باستخدام أساليب رياضية لتحليل تداخل الجسيمات مع الإشعاع، أظهروا أن الجمع بين العلاجين يولد تأثيرًا أقوى بوضوح في قتل السرطان مقارنة بكل علاج بمفرده.
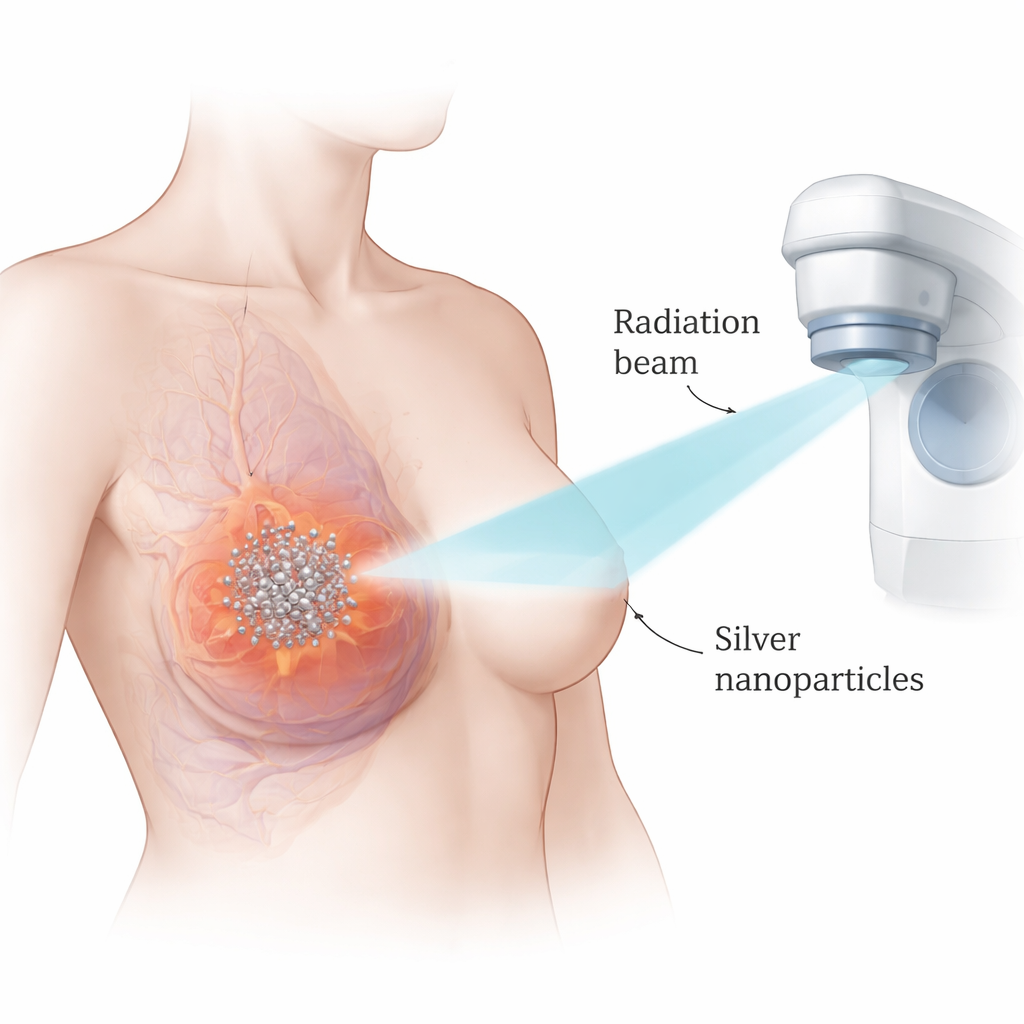
دفع الخلايا السرطانية نحو الانتحار المبرمج
بعد ذلك، فحص العلماء كيف يقتل العلاج المركب الخلايا. قاسوا الاستماتة المبرمجة (الأبوبتوسيس)، وهي شكل من أشكال انتحار الخلايا المبرمج، وتتبّعوا تراكم جزيئات شديدة التفاعل تُعرف بأنواع الأكسجين التفاعلية (ROS). من المعروف أن الإشعاع يعمل جزئياً عن طريق توليد ROS التي تُتلف الحمض النووي. في كلا خطي الخلايا السرطانية الثلاثية السلبية، رفعت جسيمات الفضة بمفردها مستويات الاستماتة وROS، وكذلك فعل الإشعاع بمفرده—لكن الجمع بينهما دفع كلا المقياسين إلى ارتفاع كبير. يعني هذا أن مزيداً من الخلايا السرطانية دُفعت إلى وضع الانتحار المنظم بدلاً من البقاء في حالة تالفة قد تشجع أحياناً الانتكاس أو المقاومة.
قطع إمدادات الدم وإبطاء الانتشار
تعتمد الأورام على الأوعية الدموية لجلب الأكسجين والمغذيات، ويمكن للسرطانات العدوانية حتى أن تُحاكي الأوعية الدموية بنفسها. نظر الفريق إلى مفتاحين جزيئيين رئيسيين يشاركان في بناء واستقرار أوعية الورم، وهما VEGFR2 وTie2. في كلا خطي الخلايا، خفضت جسيمات الفضة نشاط هذين الجينين، وأدى الجمع مع الإشعاع إلى تعطيلهما بشكل أكبر. كما فحصوا إنزيمين، MMP-2 وMMP-9، اللذين يساعدان الخلايا السرطانية على قضم النسيج المحيط والهجرة. في أحد النماذج الخلوية، خفّض كل من الإشعاع وجسيمات الفضة هذه الإنزيمات، بينما كان للت tratamiento المركب أقوى تأثير. عندما راقب العلماء حركة الخلايا السرطانية نحو "خدش" صناعي في طبق زراعة، وعندما اختبروا مدى تكوين أنابيب شبيهة بالأوعية في نظام زراعة مشترك، بدا أن العلاج المركب هو الأوضح في إبطاء الهجرة وبناء الأنابيب.
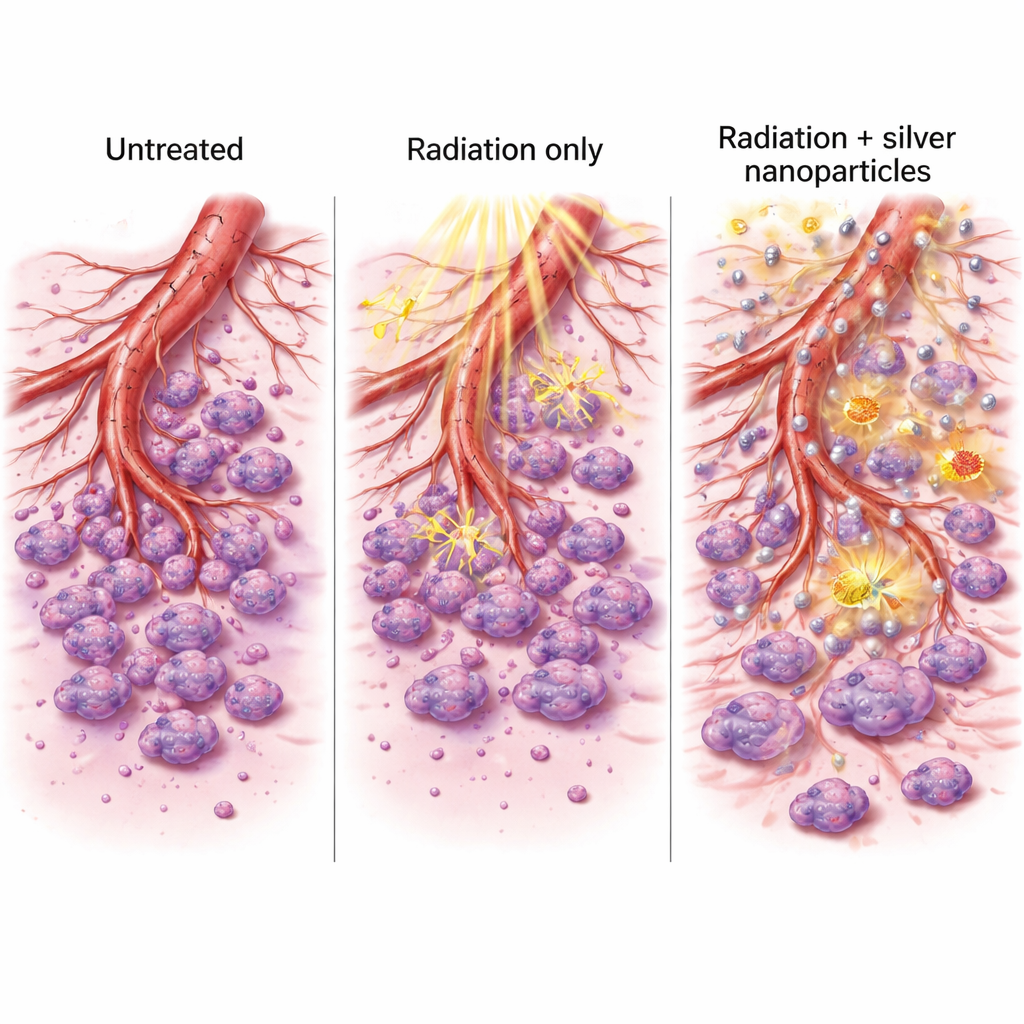
لماذا تهم هذه التغييرات
من خلال تقليل التعبير عن الجينات التي تعزز تكون أوعية دموية جديدة والإنزيمات التي تساعد الخلايا على الغزو، قام زوج الفضة والإشعاع بأكثر من مجرد قتل الخلايا السرطانية. فقد عطل أيضاً أنظمة الدعم التي تستخدمها الأورام للتوسع والانتشار. كانت الخلايا المعالجة أقل قدرة على إغلاق الجروح في أطباق المختبر وأكثر عجزاً عن التنظيم إلى شبكات متفرعة تشبه الأوعية الدموية المبكرة. ومع التعزيز القوي في موت الخلايا وإنتاج ROS، تشير هذه التأثيرات إلى فائدة ذات مسارين: هجوم مباشر أقوى على الورم وأدوات أضعف للنمو والانتشار المستقبلي.
ما الذي قد يعنيه ذلك للمرضى
حتى الآن، جاءت هذه النتائج من خلايا سرطانية نُميت في المختبر، وليس من مرضى. ومع ذلك، ترسم صورة مبشرة. عملت جسيمات الفضة النانوية كعوامل محسِّنة للإشعاع، مما جعل العلاج الإشعاعي التقليدي أكثر فاعلية ضد خلايا سرطان الثدي الثلاثي السلبي. وفي الوقت نفسه، بدا أنها تخنق قدرة الورم على بناء خطوط إمداد دموية والغزو المحيط. إذا أكدت دراسات مستقبلية على الحيوانات والسريرية أنه يمكن توصيل هذه الجسيمات بأمان وبانتقائية إلى الأورام، فقد تساعد الأطباء على استخدام جرعات إشعاع أقل مع تحقيق نتائج أفضل، مقدمًة طريقة جديدة لمواجهة أحد أكثر أشكال سرطان الثدي تحدياً.
الاستشهاد: Montazersaheb, S., Farahzadi, R., Mansouri, E. et al. Radiosensitizing effects of silver nanoparticles targeting angiogenesis and matrix metalloproteinase signaling in triple negative breast cancer cell lines. Sci Rep 16, 6820 (2026). https://doi.org/10.1038/s41598-026-35662-8
الكلمات المفتاحية: سرطان الثدي الثلاثي السلبي, جسيمات الفضة النانوية, العلاج الإشعاعي, تكوّن الأوعية الدموية, الانتشار (النقائل)