Clear Sky Science · ar
استجابة الحِس الكيميائي لأدوية العلاج الكيميائي القائمة على البلاتين عبر مستقبلات الطعم المرّ في المختبر تكشف آلية جديدة لاضطرابات الطعم المرّ
لماذا قد يصبح طعم كل شيء فجأة مريرًا لدى مرضى السرطان
غالبًا ما يبلّغ مرضى السرطان أن الطعام يبدأ بطعم غريب مرّ أو معدني بعد بدء العلاج الكيميائي بفترة قصيرة. هذا لا يُفسد الوجبات فحسب: بل يمكن أن يقلل الشهية، ويؤدي إلى فقدان الوزن، ويضعف جودة الحياة في وقت يحتاج فيه المرضى إلى قوة أكبر. تطرح هذه الدراسة سؤالًا بسيطًا في ظاهره لكنه ذا عواقب عملية كبيرة: كيف تتداخل أدوية العلاج الكيميائي الشائعة القائمة على البلاتين مع حاسة التذوق لدينا بالضبط، وهل يمكن تخفيف هذا التأثير بأمان دون إضعاف العلاج؟
الدور الخفي "لمستشعرات المرارة" في الفم والمعدة
تنتشر مستقبلات الطعم المرّ على اللسان وطول الجهاز الهضمي، صممت لتحذرنا من مواد قد تكون ضارة. هذه المستشعرات، المعروفة باسم TAS2Rs، لا تقتصر على براعم التذوق؛ بل توجد أيضًا في خلايا المعدة. استخدم الباحثون خط خلايا معدية بشرية (HGT-1) يتصرف ككاشف مرارة في المختبر: عند تنشيط مستقبلات المرارة، تقوم الخلايا بضخ مزيد من البروتونات (الحمض)، ويمكن قياس ذلك كتغير في مؤشر البروتون داخل الخلية. من خلال تعريض هذه الخلايا لدوائين شائعين قائمين على البلاتين—الكاربوبلاتين والسيسبلاتين—تمكّن الفريق من فحص مدى "مرارة" هذه الأدوية للخلايا البشرية بأمان دون مطالبة أي شخص بتذوق مركب سام. 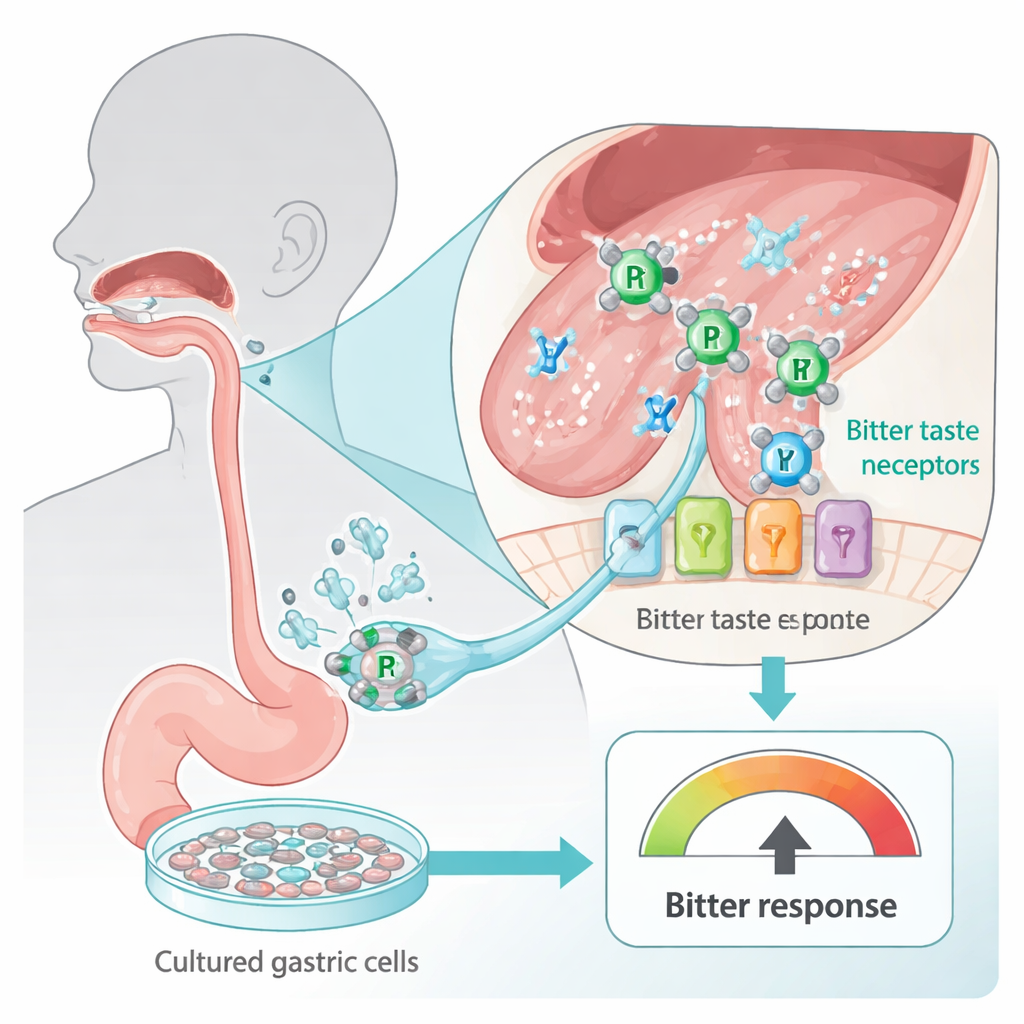
أدوية العلاج الكيميائي التي تبدو مرّة للخلايا
عند معالجة خلايا المعدة بتركيزات ذات صلة سريرية من الكاربوبلاتين والسيسبلاتين، أطلق كلا الدواءين استجابة شبيهة بالمرارة واضحة وتعتمد على الجرعة: فكلما ارتفعت الجرعة، ازدادت الاستجابة الخلوية. ومع ذلك، أظهر السيسبلاتين استجابة أكثر شدة من الكاربوبلاتين عند أخذ نسبة الجرعات العلاجية المعتادة بينهما (حوالي 1:4) في الاعتبار، ما يشير إلى أنه قد يساهم بقوة أكبر في مشكلات الطعم المرّ لدى المرضى. على المستوى الجيني، غيّر التعرض لهذه الأدوية نشاط عدة جينات لمستقبلات المرّ، ما يدل على أن أدوية البلاتين لا تعمل عبر "مفتاح مرّ" واحد بل تعيد تشكيل نظام استشعار المرارة على نحو واسع. ومن بين هذه المستقبلات، برزت TAS2R4 وTAS2R5 كمستقبلين نشيطين للغاية ومتأثرين بشدة بالعلاج.
إيقاف إشارات المرارة واختبار مانع مرارة طبيعي
لتحديد أي المستقبلات هي الأكثر أهمية، قام الفريق بكبح مستقبلات مرارة محددة بشكل انتقائي. أدى تعطيل TAS2R4 أو خفض تعبير TAS2R5 إلى تقليل الاستجابة الشبيهة بالمرارة للكاربوبلاتين والسيسبلاتين، مؤكّدين أن هذه المستقبلات تساهم في استشعار الأدوية. ثم اختبر العلماء تدخلاً واعدًا: ملح الصوديوم لهوموأريوديكتيول (Na-HED)، وهو فلافانون استُخْلِص أصلاً من نبات Herba Santa الأمريكي الشمالي ومعروف سابقًا بقدرته على إخفاء المرارة لمركبات أخرى. عندما أضيف Na-HED مع أدوية البلاتين، قلّل بشكل ملحوظ الاستجابة الخلوية للمرارة—بما يقارب ثلاثة أرباع الاستجابة لكل من الكاربوبلاتين والسيسبلاتين—دون أن يضر الخلايا بمفرده. هذا يوضح أن Na-HED يمكن أن يعمل مباشرة على مستقبلات المرارة لتخفيف الإشارة التي تثيرها أدوية العلاج الكيميائي.
حين يتقاطع استشعار المرارة ودخول الدواء إلى الخلايا
بعيدًا عن تفسير سبب مرارة أدوية البلاتين، تكشف الدراسة عن مفارقة غير متوقعة: يبدو أن نفس مستقبلات المرارة تؤثر أيضًا في مقدار دخول هذه الأدوية إلى الخلايا. باستخدام مطيافية كتلة حساسة للغاية، قاس الباحثون محتوى البلاتين داخل الخلايا بعد المعالجة. تراكمت كميات أكبر من البلاتين في الخلايا التي تفتقر إلى مستقبلات معينة، مثل TAS2R4 أو TAS2R43، مقارنة بالخلايا الطبيعية، ما يوحي بأن وجود هذه المستقبلات يساعد على الحد من دخول أو احتفاظ الخلايا بهذه العوامل السامة. لم يغيّر Na-HED من مقدار دخول الكاربوبلاتين، لكنه خفّض كمية السيسبلاتين التي دخلت الخلايا وأظهر تفاعلًا جزيئيًا مباشرًا مع السيسبلاتين في المحلول. هذا يُلمّح إلى أن مركبًا يخفي المرارة قد يغير أحيانًا أيضًا مدى تأثير الدواء على الأنسجة المحلية، مثل خلايا التذوق أو الغدد اللعابية. 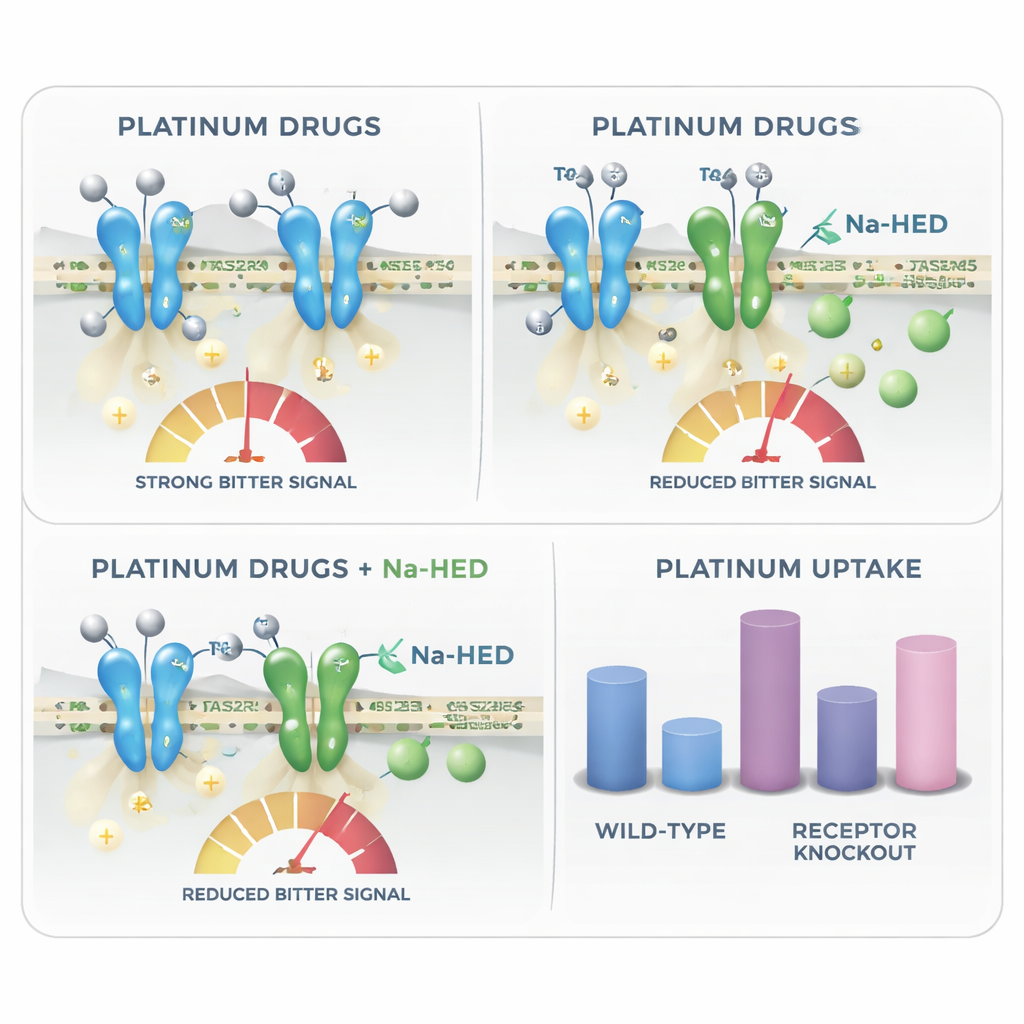
نحو تجارب ذوق ألطف أثناء العلاج الكيميائي
لدى المرضى، الخلاصة المشجعة واضحة: يبدو أن أدوية البلاتين تثير مشكلات الطعم المرّ من خلال تنشيط مستقبلات المرارة الموجودة ليس فقط على اللسان بل أيضًا في خلايا تشبه خلايا الأمعاء والمعدة. يبدو أن السيسبلاتين أقوى في هذا التأثير. تُظهر الدراسة أن Na-HED يمكن أن يخفت هذه الإشارة المرارية بشكل كبير في نظام خلوي مسيطر عليه وقد يحد أيضًا محليًا من دخول السيسبلاتين. بينما تحتاج هذه النتائج إلى تأكيد في التجارب البشرية، فإنها تشير إلى احتمالية تطوير علاجات فموية موضعية (مضمضة وبصق) تحتوي Na-HED قد تخفف الأحاسيس المرّة والمعدنية الشديدة دون التدخل في الفاعلية العلاجية للأدوية على مستوى الجسم بأكمله.
الاستشهاد: Zehentner, S., Mistlberger-Reiner, A., Pirkwieser, P. et al. Chemosensory response to Pt-based chemotherapeutics via bitter taste receptors in vitro reveals a new mechanism for bitter taste disorders. Sci Rep 16, 2634 (2026). https://doi.org/10.1038/s41598-026-35636-w
الكلمات المفتاحية: تغيرات الطعم أثناء العلاج الكيميائي, مستقبلات الطعم المرّ, سيسبلاتين وكاربوبلاتين, مركبات إخفاء الطعم المرّ, تغذية مرضى السرطان