Clear Sky Science · ar
حسابات DFT لتكوُّن مركبات Ac3+ و Bi3+ مع المِخلَب الهجين 3p-C-DEPA للعلاج الموجَّه بجسيمات ألفا
لماذا يهم هذا البحث لعلاج السرطان
تعتمد طب السرطان الحديث بشكل متزايد على أدوية مشعة قادرة على تعقب الأورام خلية بخلية. نهج قوي يُسمى العلاج الموجَّه بجسيمات ألفا يستخدم جزيئات عالية الطاقة يمكنها قتل خلايا السرطان المفردة بدقة ملحوظة. لكن لإيصال هذه الجسيمات بأمان، يجب تثبيت المعدن المشع داخل "قفص" جزيئي صغير حتى لا يتجول إلى الأنسجة السليمة. تستكشف هذه الدراسة جزيء قفص جديدًا، 3p‑C‑DEPA، مصممًا لحمل معادن صعبة بشكل خاص مثل الأكتينيوم‑225 والبيزموث‑213، وتطرح السؤال: هل يمكنه ربطها بشكل أكثر أمانًا من المِخلَب الشائع اليوم، DOTA؟
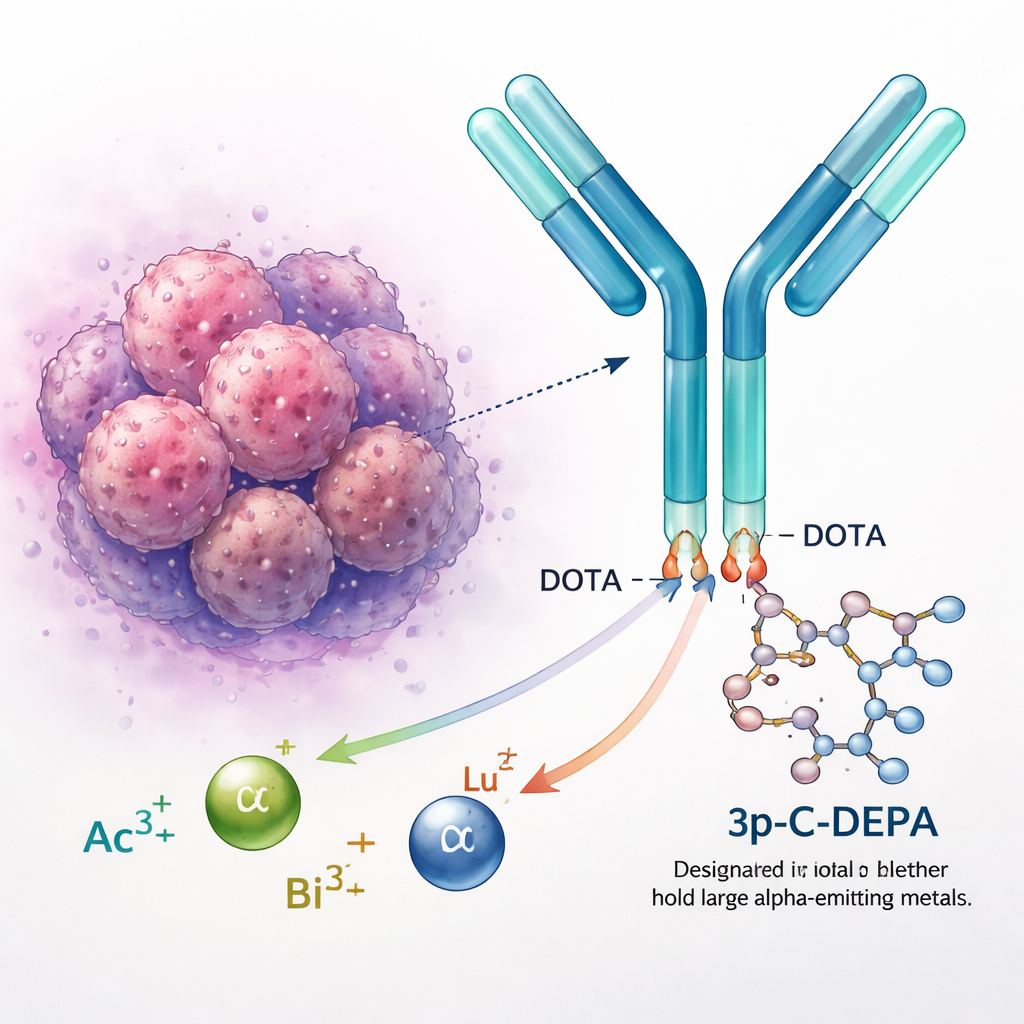
تثبيت المعادن المشعة بأمان
تُستخدم معادن مشعة مثل الأكتينيوم والبيزموث واللوتيتيوم في تشخيص وعلاج السرطان. ومع ذلك، فإن أيونات المعادن الموجبة هذه ستتفاعل بحرية داخل الجسم إذا تُركت بمفردها، مما قد يضر الأعضاء السليمة. لذلك يقوم الكيميائيون بربطها بـ "مِخلِبات"، جزيئات حلقية تلتف حول المعدن وتثبته في مكانه. يُعد المِخلَب المعياري الذهبي DOTA مستخدمًا في عدة أدوية معتمدة، لكنه يواجه صعوبة مع الأيونات الأكبر والأكثر مشتتة مثل الأكتينيوم‑225. هذه المعادن قد تنزلق مع مرور الوقت، مما يثير مخاوف بشأن السلامة طويلة الأمد ويحد من نطاق استخدام العلاج الموجَّه بجسيمات ألفا.
قفص هجين مُصمم لذرات أكبر
يجمع المِخلَب الجديد، 3p‑C‑DEPA، بين ميزات تصميمين معروفين: الهيكل الصلب الشبيه بالحلقات لـ DOTA والبنية الأكثر مرونة والانفتاح لمِخلَب آخر يُدعى DTPA. يمنح هذا الهيكل الهجين 3p‑C‑DEPA عشر "أيدٍ" ربط قوية (ذرات نيتروجين وأكسجين) مقارنةً بثمانية في DOTA، وتجويفًا أوسع يمكنه استيعاب أيونات معدنية كبيرة بشكل أفضل. أشارت أعمال مخبرية سابقة إلى أن 3p‑C‑DEPA يمكنه وسم الأجسام المضادة بسرعة عند درجات حرارة معتدلة والحفاظ على استقرار النويدات المشعة المعتمدة على البيزموث في مصل الدم. تأخذ الدراسة الحالية الخطوة التالية باستخدام حسابات على المستوى الكمي لمقارنة منهجية مدى قدرة 3p‑C‑DEPA وDOTA على ربط اللوتيتيوم‑177 والبيزموث‑213 والأكتينيوم‑225.
نظرة في المصافحة الجزيئية
نظراً لصعوبة العمل المباشر مع نواقل ألفا قصيرة العمر، لجأ الباحثون إلى نظرية الدالة الكثافية (DFT)، وهي طريقة حاسوبية قوية تُقدِّر كيف تُرتَّب الإلكترونات في الجزيئات ومدى قوة جذب الذرات لبعضها. نمذَجَوا كل أيون معدني في الماء، ثم معقده مع إما DOTA أو 3p‑C‑DEPA، وحسبوا التغير في الطاقة الحرة عندما ينتقل المعدن من الماء إلى قفص المِخلَب. يُترجم هذا التغير في الطاقة إلى "ثابت الاستقرار": كلما زادت القيمة، زاد تمسك المِخلَب بالمعدن. استُخدِم نهجان مختلفان في DFT ونموذجان للذوبان لمحاكاة ظروف محاليل واقعية والتحقق من أن الاتجاهات متينة وليست ناتجة عن إعداد حاسوبي واحد فقط.
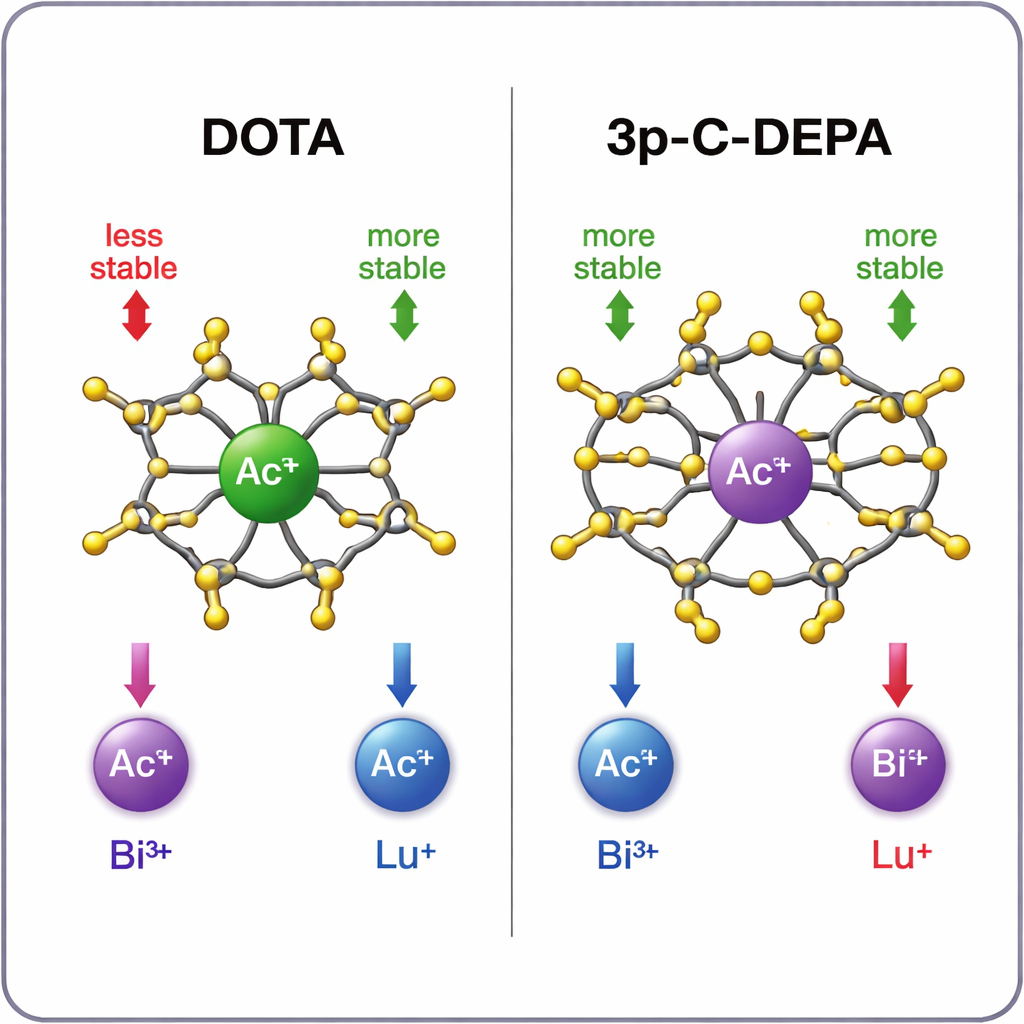
أي قفص يمسك أي معدن أفضل؟
تعرض المحاكيات نمطًا واضحًا. بالنسبة لأيون الأكتينيوم الكبير، يُشكِّل 3p‑C‑DEPA معقدًا أكثر استقرارًا بشكل ملحوظ من DOTA، بفضل تجويفه الأكبر وعدد أكبر من المانحين الأكسجينيين الذين يمكنهم الإمساك بالمعدن. كما تستوعب 3p‑C‑DEPA البيزموث‑213 جيدًا، مستفيدة من كل من حجمه وطابع قبوله للإلكترونات، الذي يتوافق مع مجموعات التبرع بالإلكترون في المِخلَب. على النقيض من ذلك، ينسجم اللوتيتيوم‑177 الأصغر بشكل أكثر راحة مع بيئة DOTA الأضيق ذات الذراعين الثمانية. في 3p‑C‑DEPA، تُحدث مجموعات المانحين الزائدة ازدحامًا حول الأيون الصغير، مولدة تفاعلات تنافرية تبدو أنها تبطئ وسمه وتضعف قليلاً المتعضد النهائي. تتفق اتجاهات الاستقرار المحسوبة جيدًا مع البيانات التجريبية المتاحة وعوائد الوسم الإشعاعي، مما يمنح مصداقية للتنبؤات النظرية.
ماذا يعني هذا لعلاجات السرطان المستقبلية
بعبارات بسيطة، تقترح الدراسة أن DOTA ليس قفصًا يناسب الجميع: فهو يعمل جيدًا جدًا للمعادن الأصغر مثل اللوتيتيوم، لكنه دون المستوى بالنسبة للمصدِرات الألفا الأكبر مثل الأكتينيوم‑225. أما 3p‑C‑DEPA، فيتصرف كحامل مُصمم خصيصًا لهذه الأيونات الأكبر، ممسكًا بها بقوة وتحت ظروف ألطف تناسب جزيئات الاستهداف الحساسة مثل الأجسام المضادة. ومع حاجة المزيد من العمل التجريبي والسريري، تشير الحسابات إلى أن 3p‑C‑DEPA قد يكون هيكلًا واعدًا لعلاجات ألفا موجَّهة أكثر أمانًا وفعالية — مما قد يوسع إمكانية الوصول إلى علاجات سرطانية شديدة الفاعلية قادرة على القضاء على الأورام مع الحفاظ على الأنسجة السليمة المحيطة.
الاستشهاد: Ramdhani, D., Watabe, H., Ahenkorah, S. et al. DFT calculation of Ac3+ and Bi3+ complexation with hybrid chelator 3p-C-DEPA for targeted alpha therapy. Sci Rep 16, 6587 (2026). https://doi.org/10.1038/s41598-026-35633-z
الكلمات المفتاحية: العلاج الموجَّه بجسيمات ألفا, الأدوية المشعة, تصميم المخلِبات, الأكتينيوم-225, نظرية الدالة الكثافية